Clear Sky Science · de
Bioaktiv vermittelte Lipid‑abhängige strukturelle und funktionelle Regulation des essentiellen menschlichen Kaliumkanals Kir7.1
Warum winzige Tore in unseren Zellen wichtig sind
In den Membranen vieler unserer Zellen sind mikroskopische Tore verborgen, die den Fluss von Kaliumionen hinein und heraus erlauben. Eines dieser Tore, Kir7.1 genannt, ist für gesundes Sehen, Hirnfunktionen und sogar die zeitliche Steuerung der Geburt entscheidend. Wenn dieses Tor defekt ist, können Menschen früh erblinden und Tiere Probleme mit Fütterung und Schwangerschaft entwickeln. Diese Studie zeigt im atomaren Detail, wie natürliche Fette und hormonähnliche Moleküle an Kir7.1 andocken und als Ein‑/Ausschalter dienen, und eröffnet damit neue Wege für die Arzneimittelentwicklung.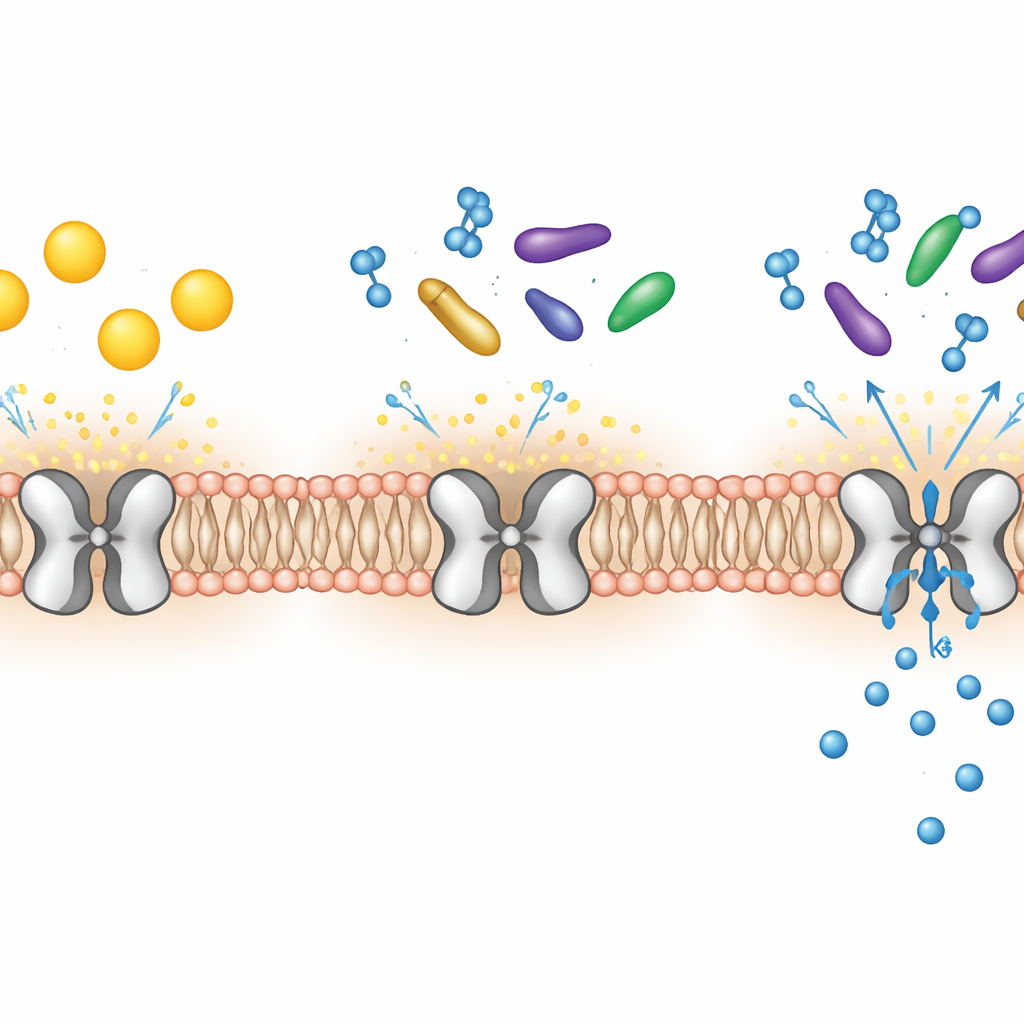
Ein besonderes Tor für das elektrische Gleichgewicht
Kir7.1 gehört zu einer Familie von Kanälen, die üblicherweise den Einstrom von Kaliumionen in eine Zelle leichter ermöglichen als den Ausstrom und damit helfen, das elektrische Gleichgewicht über die Zellmembran herzustellen. Im retinalen Pigmentepithel des Auges hält Kir7.1 die Umgebung der lichtempfindlichen Zellen stabil; fehlt er, sterben Photorezeptoren allmählich ab und das Sehvermögen schwächt sich. Kir7.1 formt zudem neuronale Schaltkreise, die Appetit steuern, und trägt dazu bei, die Gebärmutter während der Schwangerschaft ruhig zu halten. Diese vielseitigen Funktionen machen den Kanal zu einem attraktiven, aber schlecht verstandenen Arzneimittelziel, zumal seine natürlichen Regulatoren — abgesehen von einigen bekannten Membranlipiden — weitgehend unbekannt waren.
Den Kanal in drei verschiedenen Stellungen sehen
Um zu entschlüsseln, wie Kir7.1 funktioniert, stellten die Forschenden große Mengen des menschlichen Proteins in Säugerzellen her, reinigten es und bildeten es mittels hochauflösender Kryo‑Elektronenmikroskopie ab. Sie erfassten den Kanal in drei Hauptkonformationen. Im „gestreckten“ Zustand liegt der untere, zytoplasmatische Teil des Kanals weiter von der Membran entfernt, und der zentrale Tunnel für Ionen ist lang und vergleichsweise eng — ein wahrscheinlich nicht leitender Zustand. Im „angedockten“ Zustand rotiert diese untere Domäne und bewegt sich nach oben zur Membran, wodurch der Tunnel verkürzt und leicht verbreitert wird. In einem dritten Zustand ist der Kanal an ein stark wirkendes synthetisches Steroid sowie an ein Signallipid namens PIP2 gebunden und zeigt eine Konfiguration, die als „vorgeordnet“ für das Öffnen erscheint. Eine kleine Veränderung einer einzelnen Aminosäure in der Nähe des Selektivitätsfilters hilft zu erklären, warum Kir7.1 im Gegensatz zu den meisten verwandten Kanälen Cäsiumionen leiten kann.
Wie Fette und Hormone gemeinsam die Kontrolle ausüben
Die strukturellen Momentaufnahmen zeigten, dass Kir7.1 ständig ein PIP2‑Molekül an einer konservierten Stelle trägt, an der auch andere Familienmitglieder dieses Lipid binden. PIP2 allein reicht jedoch nicht aus, um Kir7.1 vollständig zu öffnen. Eine zweite Tasche, die zwischen den membranüberspannenden Helices liegt, enthält eine andere Art von Lipid. Im ruhenden gestreckten Zustand ist diese Tasche mit Cholesterin gefüllt, einem vertrauten Membransterol. Elektrophysiologische Experimente zeigten, dass zusätzliches Cholesterin die Kir7.1‑Ströme dämpft, während bestimmte Steroide, darunter das Schwangerschaftshormon Progesteron und das Neurosteroid DHEA, sie stark verstärken. Die Daten stützen ein Modell, in dem Cholesterin als natürlicher Bremsmechanismus wirkt: Aktivierende Steroide müssen zuerst Cholesterin aus der Tasche verdrängen, und wenn sie dies in Anwesenheit von PIP2 tun, kann die untere Domäne rotieren und der Ionenweg sich verbreitern.
Stärkere molekulare Schlüssel entdecken
Um diese Einsicht in praktische Werkzeuge zu überführen, testete das Team ein breites Panel natürlicher und synthetischer Steroide sowie deren Spiegelbildformen. Sie fanden mehrere neue Moleküle, die Kir7.1 aktivieren, viele bei niedrigen Mikromolar‑ oder sogar Submikromolarkonzentrationen. Ein auffälliger Kandidat, ein Enantiomer des Medikaments 17‑Hydroxyprogesteron‑caproat, band sich fest in dieselbe hydrophobe Tasche, die normalerweise Cholesterin beherbergt. In der Struktur mit diesem Aktivator bildete die polare Spitze des Steroids eine enge Wasserstoffbrücke zu einer wichtigen Threoninseitenkette, während sein fettiger Rumpf sich an die Helices des Kanals schmiegte. Diese enge Passung erklärt seine Wirksamkeit und seine Fähigkeit, den Kanal auch in Anwesenheit eines Standard‑Kir7.1‑Blockers aktiv zu halten.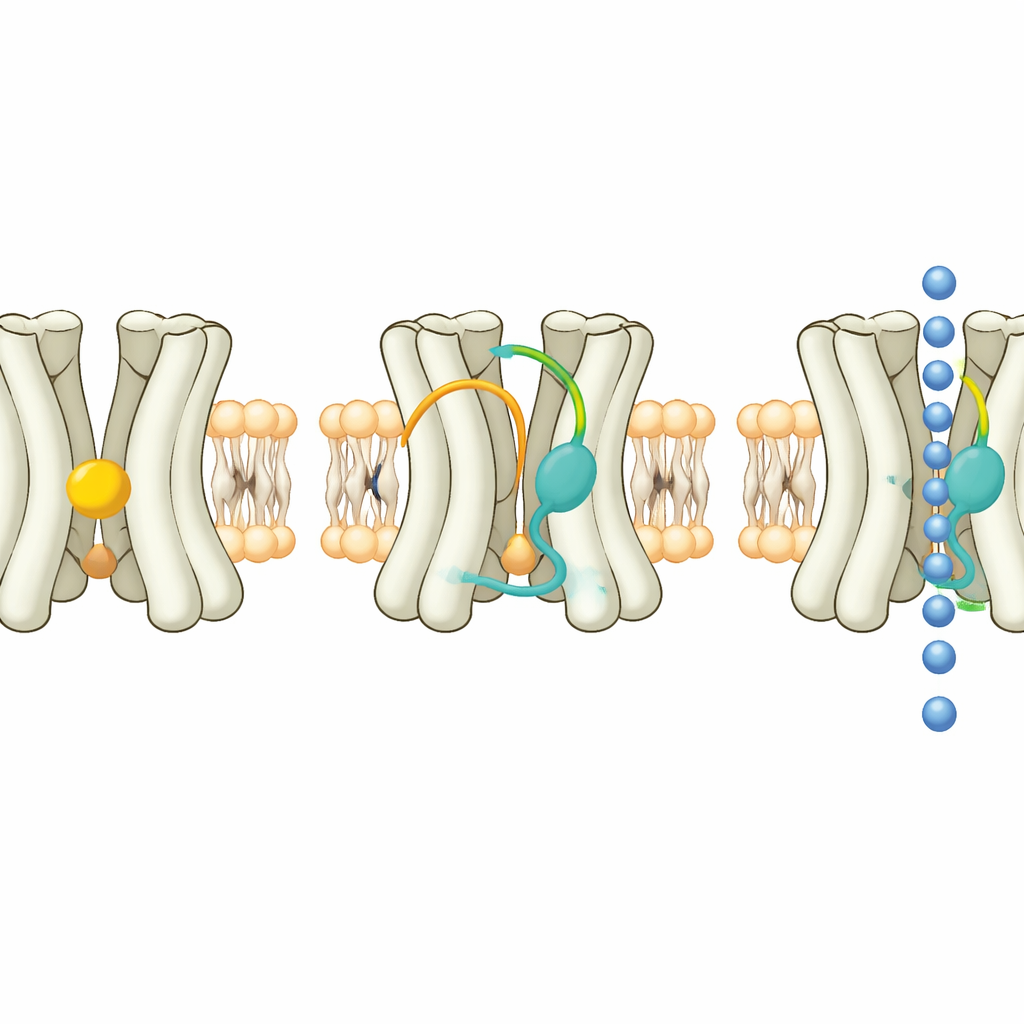
Von der Strukturkarte zum therapeutischen Versprechen
Insgesamt zeigt die Arbeit, dass Kir7.1 durch eine kooperative Partnerschaft zwischen PIP2, hemmendem Cholesterin und ausgewählten aktivierenden Steroiden gesteuert wird. PIP2 verankert und organisiert den Kanal teilweise; Cholesterin hält ihn in einer gestreckten, weniger leitfähigen Form; und Steroide, die Cholesterin verdrängen, lockern die Helices und erlauben der unteren Domäne, in einen offeneren, leitfähigen Zustand zu wechseln. Indem diese Wechselwirkungen Atom für Atom aufgelöst und aufgezeigt werden, wie kleine chemische Änderungen die Steroidpotenz verändern, liefert die Studie eine Blaupause für die Entwicklung neuer Wirkstoffe, die die Kir7.1‑Aktivität bei Erkrankungen des Auges, des Gehirns und der Gebärmutter wiederherstellen oder feinjustieren können.
Zitation: Niu, Q., Vu, S., Xu, Y. et al. Bioactive lipid-mediated structural and functional regulation of the essential human potassium channel Kir7.1. Nat Commun 17, 2764 (2026). https://doi.org/10.1038/s41467-026-68819-0
Schlüsselwörter: Kir7.1-Kaliumkanal, Cholesterinregulation, Steroide als Modulatoren, cryo‑EM-Struktur, retinale Pigmentepithel