Clear Sky Science · es
Regulación estructural y funcional mediada por lípidos bioactivos del canal de potasio humano esencial Kir7.1
Por qué importan las puertas diminutas en nuestras células
Enterradas en las membranas de muchas de nuestras células hay puertas microscópicas que permiten el paso de iones potasio. Una de estas puertas, llamada Kir7.1, es crucial para una visión saludable, la función cerebral e incluso el momento del parto. Cuando esta puerta falla, las personas pueden perder la visión tempranamente y los animales presentan problemas con la alimentación y el embarazo. Este estudio revela, con detalle atómico, cómo grasas naturales y moléculas con apariencia hormonal se acoplan a Kir7.1 y actúan como sus interruptores de encendido y apagado, abriendo nuevas vías para el diseño de fármacos.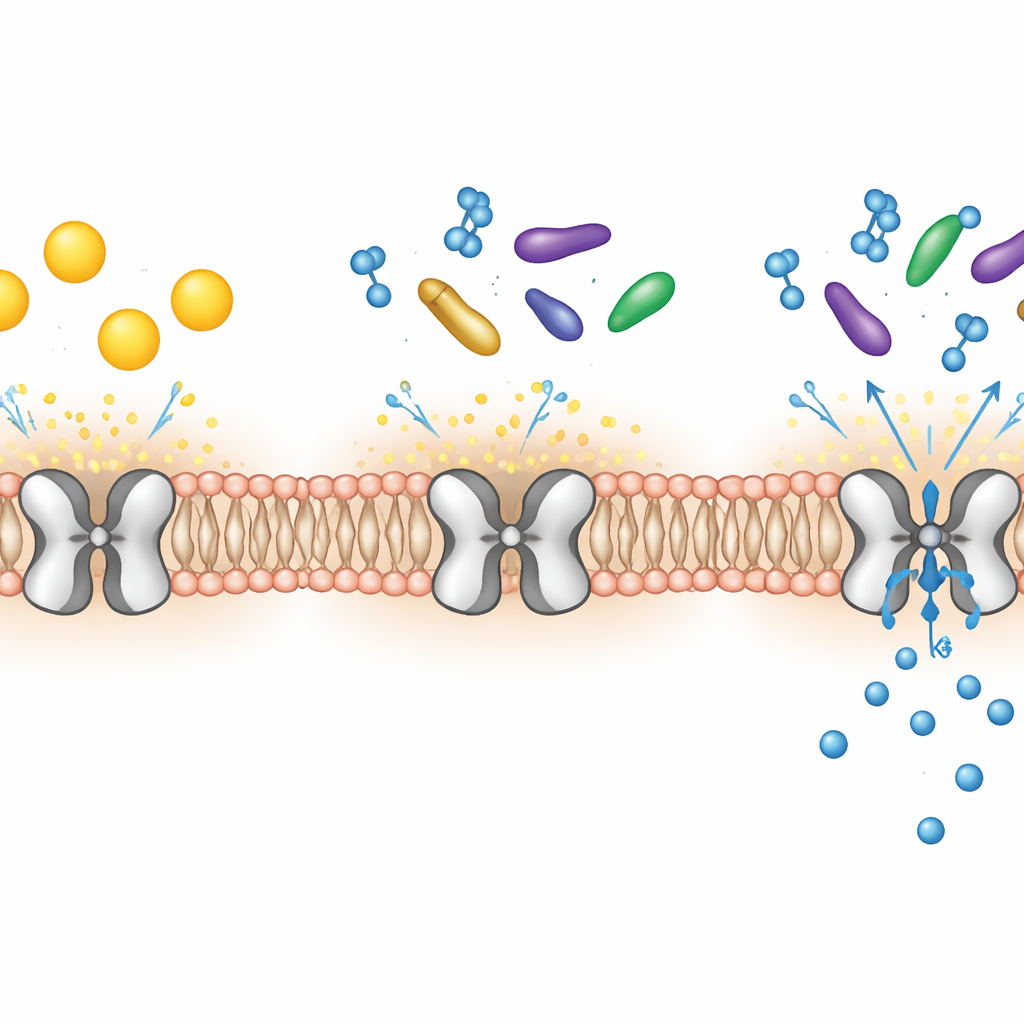
Una puerta especial para el equilibrio eléctrico
Kir7.1 pertenece a una familia de canales que habitualmente permiten que los iones potasio entren en la célula con más facilidad de la que salen, ayudando a establecer el equilibrio eléctrico a través de la membrana celular. En el epitelio pigmentario retinal, Kir7.1 mantiene estable el entorno alrededor de las células fotorreceptoras; sin él, los fotorreceptores mueren lentamente y la visión se degrada. Kir7.1 también configura circuitos nerviosos que controlan el apetito y contribuye a mantener el útero en calma durante el embarazo. Estos roles amplios han convertido al canal en un objetivo farmacológico atractivo pero poco comprendido, especialmente porque sus reguladores naturales, más allá de algunos lípidos conocidos de membrana, eran enigmáticos.
Ver la puerta en tres posturas distintas
Para descubrir cómo funciona Kir7.1, los investigadores produjeron grandes cantidades de la proteína humana en células de mamífero, la purificaron y la visualizaron mediante crio–microscopía electrónica de alta resolución. Capturaron al canal en tres formas principales. En el estado “extendido”, la parte inferior, citoplásmica, del canal queda más alejada de la membrana y el túnel central para los iones es largo y relativamente estrecho, una postura probablemente no conductora. En el estado “anclado” (docked), este dominio inferior rota y se desplaza hacia arriba en dirección a la membrana, acortando y ensanchando ligeramente el túnel. En un tercer estado, el canal está unido a un esteroide sintético potente junto con un lípido señalizador llamado PIP2, produciendo una configuración que parece “preparada” para abrirse. Un pequeño cambio en un único aminoácido cerca del filtro de selectividad ayuda a explicar por qué Kir7.1 puede conducir iones cesio, a diferencia de la mayoría de canales relacionados.
Cómo las grasas y las hormonas comparten el control
Las instantáneas estructurales revelaron que Kir7.1 porta constantemente una molécula de PIP2 en un sitio conservado donde otros miembros de la familia también se unen a este lípido. Sin embargo, PIP2 por sí sola no es suficiente para abrir totalmente a Kir7.1. Un segundo bolsillo, encajado entre sus hélices transmembrana, contiene otro tipo de lípido. En el estado extendido de reposo, este bolsillo alberga colesterol, un esterol de membrana familiar. Experimentos electrofisiológicos mostraron que añadir colesterol extra reduce las corrientes de Kir7.1, mientras que ciertos esteroides, incluyendo la hormona del embarazo progesterona y el neuroesteroide DHEA, las aumentan con fuerza. Los datos apoyan un modelo en el que el colesterol actúa como un freno natural: los esteroides activadores deben primero desalojar el colesterol del bolsillo, y cuando lo hacen en presencia de PIP2, el dominio inferior del canal puede rotar y la vía iónica puede ensancharse.
Descubriendo llaves moleculares más potentes
Para convertir este hallazgo en herramientas prácticas, el equipo seleccionó un amplio panel de esteroides naturales y sintéticos y sus formas enantiómeras. Encontraron varias moléculas nuevas que activan Kir7.1, muchas a concentraciones micromolares bajas o incluso submicromolares. Una destacada, un enantiómero del fármaco 17-hidroxiprogesterona caproato, se unió con alta afinidad en el mismo bolsillo hidrofóbico que normalmente aloja colesterol. En la estructura con este activador presente, la punta polar del esteroide formó un estrecho enlace de hidrógeno con una cadena lateral de treonina clave, mientras que su cuerpo oleoso se acomodó junto a las hélices del canal. Este encaje ceñido ayuda a explicar su potencia y su capacidad para mantener el canal activo incluso en presencia de un bloqueador estándar de Kir7.1.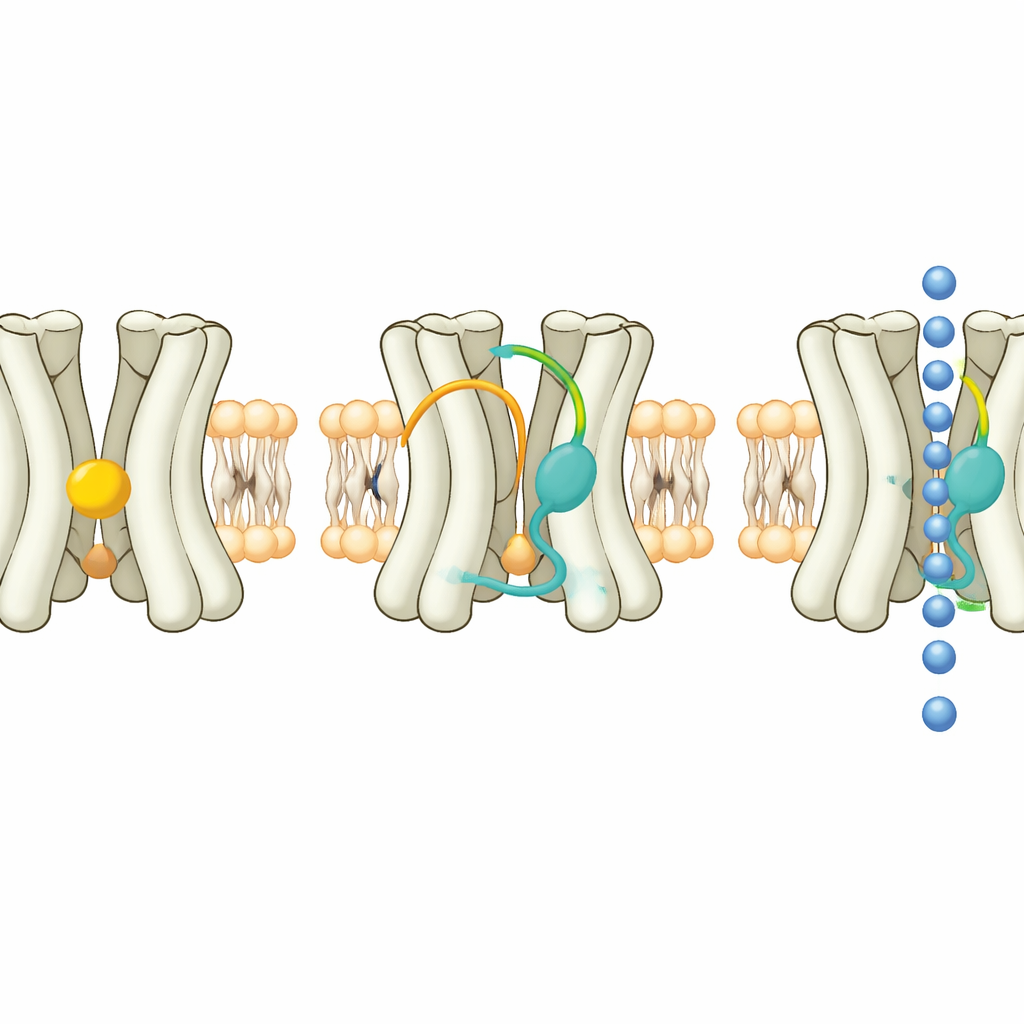
Del mapa estructural a la promesa terapéutica
En conjunto, el trabajo muestra que Kir7.1 está gobernado por una asociación cooperativa entre PIP2, el colesterol inhibidor y ciertos esteroides activadores. PIP2 ancla y organiza parcialmente el canal; el colesterol lo mantiene en una forma extendida y menos conductora; y los esteroides que desalojan el colesterol aflojan las hélices y permiten que el dominio inferior se desplace hacia un estado más abierto y conductor. Al resolver estas interacciones átomo por átomo y describir cómo pequeños ajustes químicos modulan la potencia de los esteroides, el estudio ofrece un plano para diseñar nuevos fármacos que restauren o modulen la actividad de Kir7.1 en enfermedades del ojo, el cerebro y el útero.
Cita: Niu, Q., Vu, S., Xu, Y. et al. Bioactive lipid-mediated structural and functional regulation of the essential human potassium channel Kir7.1. Nat Commun 17, 2764 (2026). https://doi.org/10.1038/s41467-026-68819-0
Palabras clave: canal de potasio Kir7.1, regulación por colesterol, moduladores esteroides, estructura por crio-EM, epitelio pigmentario retinal