Clear Sky Science · pt
Regulação estrutural e funcional do canal de potássio humano essencial Kir7.1 mediada por lipídios bioativos
Por que portinhas minúsculas em nossas células importam
Enterradas nas membranas de muitas de nossas células estão comportas microscópicas que permitem o fluxo de íons potássio para dentro e fora. Uma dessas comportas, chamada Kir7.1, é crucial para a visão saudável, a função cerebral e até o momento do parto. Quando essa comporta se danifica, pessoas podem perder a visão precocemente, e animais desenvolvem problemas de alimentação e gravidez. Este estudo revela, em detalhe atômico, como gorduras naturais e moléculas semelhantes a hormônios se ligam à Kir7.1 e funcionam como seus interruptores on–off, abrindo novas vias para o desenvolvimento de fármacos.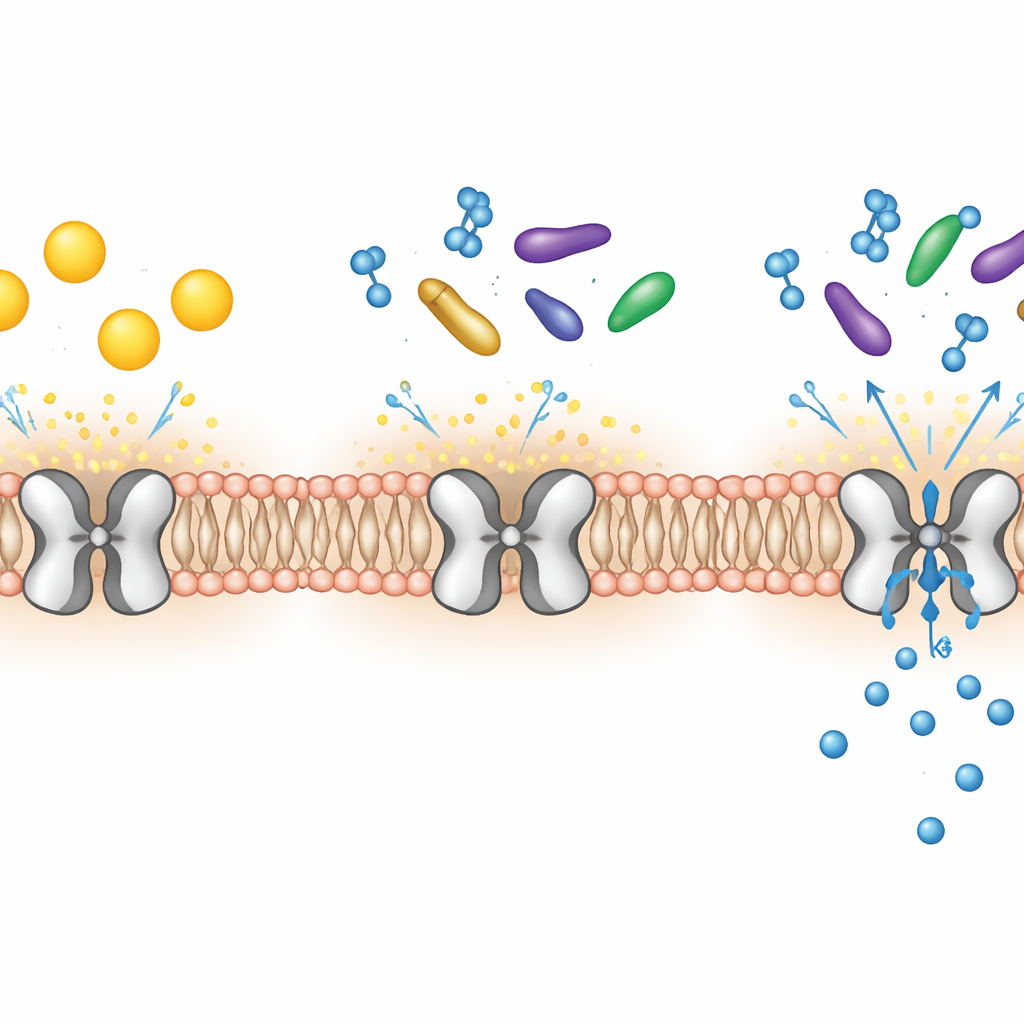
Uma comporta especial para equilíbrio elétrico
Kir7.1 pertence a uma família de canais que normalmente permitem que íons potássio entrem na célula com mais facilidade do que saiam, ajudando a estabelecer o equilíbrio elétrico através da membrana celular. No epitélio pigmentado da retina, Kir7.1 mantém o ambiente ao redor das células fotossensíveis estável; sem ele, os fotorreceptores morrem lentamente e a visão se perde. Kir7.1 também molda circuitos nervosos que controlam o apetite e ajuda a manter o útero silencioso durante a gravidez. Esses papéis amplos tornaram o canal um alvo farmacológico atraente, porém pouco compreendido, especialmente porque seus reguladores naturais, além de alguns lipídios de membrana conhecidos, eram misteriosos.
Ver a comporta em três poses distintas
Para descobrir como a Kir7.1 funciona, os pesquisadores produziram grandes quantidades da proteína humana em células de mamífero, purificaram‑na e a imageram usando crio‑microscopia eletrônica de alta resolução. Eles capturaram o canal em três conformações principais. No estado “estendido”, a parte inferior citoplasmática do canal repousa mais distante da membrana e o túnel central para os íons é longo e relativamente estreito, uma conformação provavelmente não condutora. No estado “encaixado”, esse domínio inferior gira e se move para cima em direção à membrana, encurtando e alargando ligeiramente o túnel. Em um terceiro estado, o canal está ligado a um esteroide sintético potente juntamente com um lipídio sinalizador chamado PIP2, produzindo uma configuração que parece “preparada” para abrir. Uma pequena alteração em um único aminoácido próximo ao filtro de seletividade ajuda a explicar por que Kir7.1 pode conduzir íons césio, ao contrário da maioria dos canais relacionados.
Como gorduras e hormônios dividem o controle
As imagens estruturais revelaram que a Kir7.1 transporta constantemente uma molécula de PIP2 em um sítio conservado onde outros membros da família também se ligam a esse lipídio. Contudo, o PIP2 sozinho não é suficiente para abrir completamente a Kir7.1. Um segundo bolso, alojado entre seus helices transmembranares, contém um tipo diferente de lipídio. No estado estendido de repouso, esse bolso abriga colesterol, um esterol de membrana familiar. Experimentos eletrofisiológicos mostraram que adicionar colesterol extra reduz as correntes da Kir7.1, enquanto certos esteroides, incluindo o hormônio da gravidez progesterona e o neuroesteróide DHEA, as aumentam fortemente. Os dados sustentam um modelo em que o colesterol atua como um freio natural: esteroides ativadores devem primeiro desalojar o colesterol do bolso e, quando o fazem na presença de PIP2, o domínio inferior do canal pode girar e a via iônica pode alargar.
Descobrindo chaves moleculares mais potentes
Para transformar esse insight em ferramentas práticas, a equipe testou um amplo painel de esteroides naturais e sintéticos e suas formas imagem‑espelho. Eles encontraram várias moléculas novas que ligam a Kir7.1, muitas em concentrações micromolares baixas ou mesmo submicromolares. Um destaque foi um enantiômero do fármaco 17‑hidroxiprogesterona caproato, que se ligou firmemente no mesmo bolso hidrofóbico que normalmente abriga colesterol. Na estrutura com esse ativador presente, a ponta polar do esteroide formou uma ligação de hidrogênio próxima com a cadeia lateral de uma treonina chave, enquanto seu corpo oleoso se acomodou junto aos hélices do canal. Esse encaixe apertado ajuda a explicar sua potência e sua capacidade de manter o canal ativo mesmo na presença de um bloqueador padrão da Kir7.1.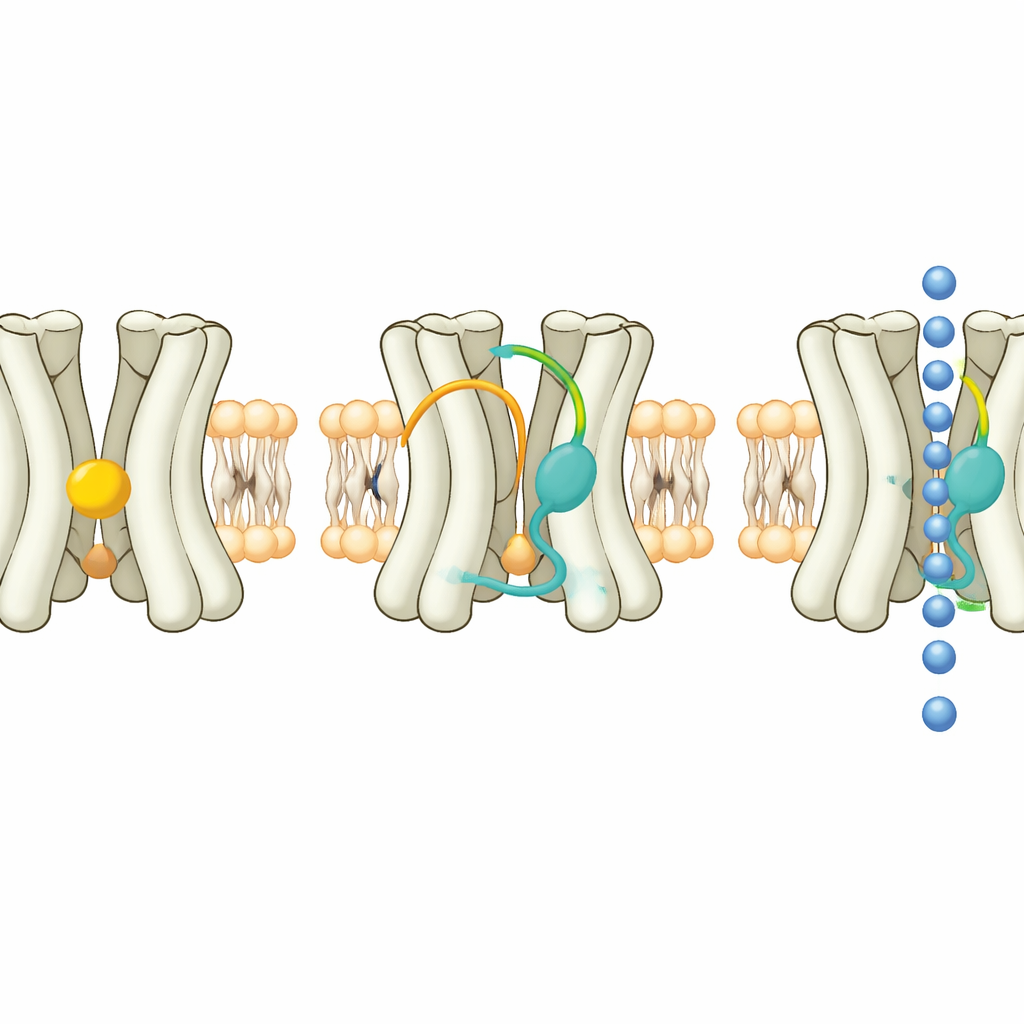
Do mapa estrutural à promessa terapêutica
Em conjunto, o trabalho mostra que a Kir7.1 é governada por uma parceria cooperativa entre PIP2, colesterol inibitório e esteroides ativadores seletos. O PIP2 ancora e organiza parcialmente o canal; o colesterol o mantém em uma forma estendida e menos condutiva; e esteroides que expulsam o colesterol afrouxam os hélices e permitem que o domínio inferior se desloque para um estado mais aberto e condutivo. Ao resolver essas interações átomo por átomo e delinear como pequenas alterações químicas modificam a potência dos esteroides, o estudo oferece um roteiro para projetar novos fármacos que restaurem ou ajustem a atividade da Kir7.1 em doenças do olho, cérebro e útero.
Citação: Niu, Q., Vu, S., Xu, Y. et al. Bioactive lipid-mediated structural and functional regulation of the essential human potassium channel Kir7.1. Nat Commun 17, 2764 (2026). https://doi.org/10.1038/s41467-026-68819-0
Palavras-chave: canal de potássio Kir7.1, regulação por colesterol, moduladores esteroides, estrutura por crio‑EM, epitélio pigmentado da retina