Clear Sky Science · nl
Bioactieve lipiden-gemedieerde structurele en functionele regulatie van het essentiële menselijke kaliumkanaal Kir7.1
Waarom kleine poorten in onze cellen ertoe doen
In de membranen van veel van onze cellen zitten microscopische poorten die kaliumionen in- en uitlaten. Een van deze poorten, Kir7.1 genaamd, is cruciaal voor gezond zicht, hersenfunctie en zelfs de timing van de bevalling. Als deze poort defect raakt, kunnen mensen vroeg in hun leven blind worden en ontwikkelen dieren problemen met voeden en zwangerschap. Deze studie onthult, tot op atomaire detail, hoe natuurlijke vetten en hormoonachtige moleculen aan Kir7.1 binden en fungeren als aan/uit-schakelaars, wat nieuwe wegen opent voor geneesmiddelontwerp.
Een speciale poort voor elektrische balans
Kir7.1 behoort tot een familie kanalen die gewoonlijk kaliumionen gemakkelijker een cel in laten dan eruit, en zo helpen de elektrische balans over het celmembraan vast te leggen. In het retinale pigmentepitheel van het oog houdt Kir7.1 de omgeving rond lichtgevoelige cellen stabiel; zonder dit kanaal sterven fotoreceptoren geleidelijk en neemt het gezichtsvermogen af. Kir7.1 beïnvloedt ook zenuwcircuits die de eetlust regelen en helpt de baarmoeder rustig te houden tijdens de zwangerschap. Deze brede functies maken het kanaal tot een aantrekkelijk maar weinig begrepen doelwit voor medicijnen, vooral omdat zijn natuurlijke regulatoren, afgezien van enkele bekende membraanfosfolipiden, grotendeels onduidelijk waren.
De poort in drie verschillende houdingen zien
Om te begrijpen hoe Kir7.1 werkt, produceerden de onderzoekers grote hoeveelheden van het humane eiwit in mammacellen, zuiverden het en beelden het af met hoogresolutie cryo-elektronenmicroscopie. Ze legden het kanaal vast in drie hoofdvormen. In de “uitgerekte” toestand bevindt het lagere, cytoplasmatische deel zich verder van het membraan en is de centrale tunnel voor ionen lang en relatief smal, een waarschijnlijk niet-geleidende houding. In de “gedockte” toestand roteert dit lagere domein en beweegt het omhoog richting het membraan, waardoor de tunnel korter en iets wijder wordt. In een derde toestand is het kanaal gebonden aan een krachtige synthetische steroïde samen met het signaallipide PIP2, wat een configuratie oplevert die ogenschijnlijk “geprimed” is voor opening. Een kleine wijziging in één aminozuur vlak bij het selectiviteitsfilter helpt verklaren waarom Kir7.1 cesiumionen kan geleiden, in tegenstelling tot de meeste verwante kanalen.
Hoe vetten en hormonen gezamenlijk de controle hebben
De structurele snapshots toonden aan dat Kir7.1 continu een PIP2-molecuul draagt op een geconserveerde plaats waar ook andere familieleden dit lipid binden. PIP2 alleen is echter niet voldoende om Kir7.1 volledig te openen. Een tweede pocket, klem tussen zijn membraan-doorstekende helices, bevat een ander type lipid. In de rustende uitgerekte toestand bevat deze pocket cholesterol, een bekend membraansterol. Elektrofysiologische experimenten toonden aan dat extra cholesterol toevoegen de Kir7.1-stromen dempt, terwijl bepaalde steroïden, waaronder het zwangerschapshormoon progesteron en de neurosteroïde DHEA, ze sterk versterken. De gegevens ondersteunen een model waarbij cholesterol fungeert als een natuurlijke rem: activerende steroïden moeten eerst cholesterol uit die pocket verdringen, en wanneer ze dat doen in aanwezigheid van PIP2, kan het lagere domein van het kanaal roteren en kan het ionenpad wijder worden.
Sterkere moleculaire sleutels ontdekken
Om dit inzicht in praktische instrumenten om te zetten, screende het team een breed panel van natuurlijke en synthetische steroïden en hun spiegelbeeldvormen. Ze vonden meerdere nieuwe moleculen die Kir7.1 aanzetten, vaak bij lage micromolaire of zelfs submicromolaire concentraties. Een opvallende verbinding, een enantiomeer van het middel 17-hydroxyprogesteron capraat, bond sterk in dezelfde hydrofobe pocket die normaal cholesterol huisvest. In de structuur met deze activator vormde de polaire top van de steroïde een nauwe waterstofbrug met een sleutelthreonine-zijketen, terwijl het vettige lichaam tegen de helices van het kanaal aanschoof. Deze passende pasvorm helpt zijn potentie te verklaren en zijn vermogen het kanaal actief te houden zelfs in aanwezigheid van een standaard Kir7.1-blokker.
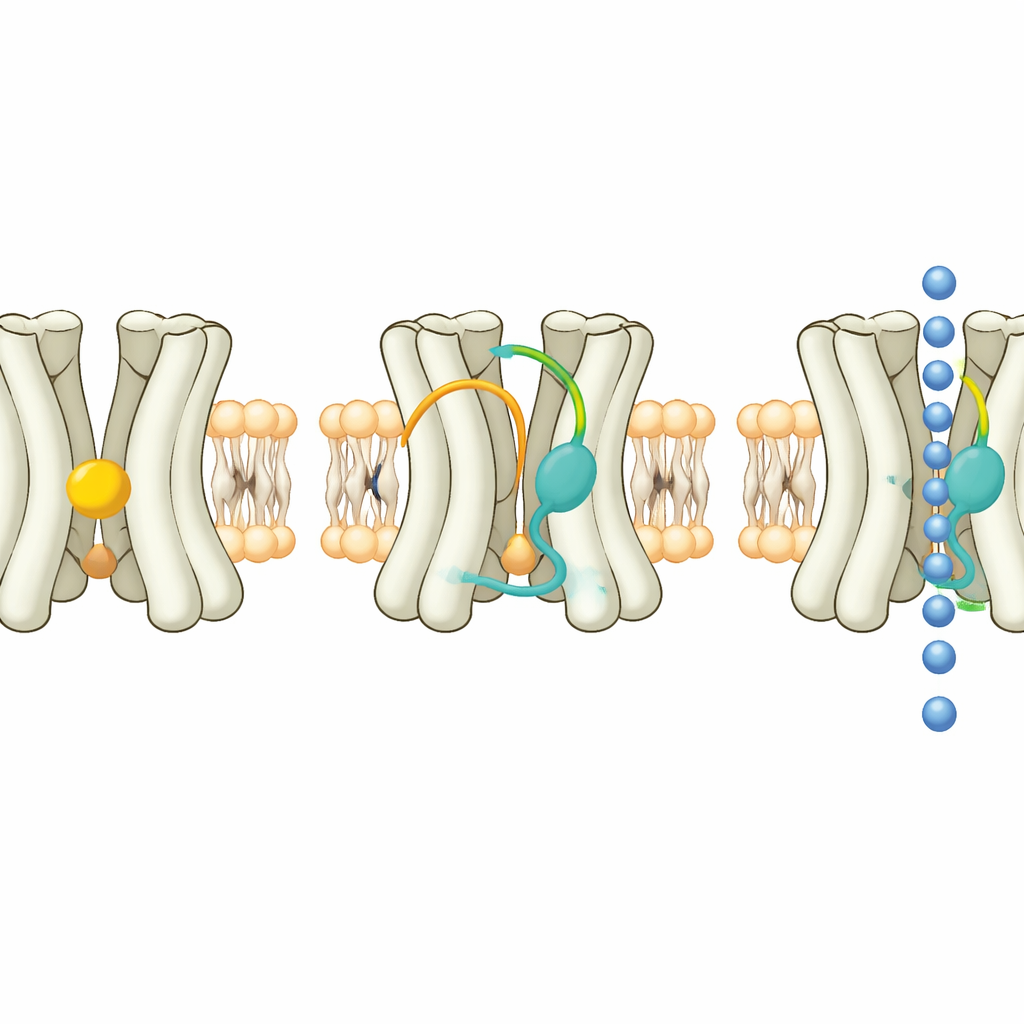
Van structurele kaart naar therapeutische belofte
Gezamenlijk tonen de resultaten aan dat Kir7.1 wordt beheerst door een samenwerkend partnerschap tussen PIP2, remmend cholesterol en selectieve activerende steroïden. PIP2 verankert en organiseert het kanaal gedeeltelijk; cholesterol houdt het in een uitgerekte, minder geleidende vorm; en steroïden die cholesterol verdringen, laten de helices ontspannen en stellen het lagere domein in staat te verschuiven naar een meer open, geleidende staat. Door deze interacties atoom voor atoom te resolven en te schetsen hoe kleine chemische aanpassingen de steroïde-potentie veranderen, biedt de studie een blauwdruk voor het ontwerpen van nieuwe geneesmiddelen die Kir7.1-activiteit herstellen of verfijnen bij ziekten van oog, hersenen en baarmoeder.
Bronvermelding: Niu, Q., Vu, S., Xu, Y. et al. Bioactive lipid-mediated structural and functional regulation of the essential human potassium channel Kir7.1. Nat Commun 17, 2764 (2026). https://doi.org/10.1038/s41467-026-68819-0
Trefwoorden: Kir7.1 kaliumkanaal, cholesterolregulatie, steroïde modulatoren, cryo-EM structuur, retinale pigmentepitheel