Clear Sky Science · sv
RUNX1 dämpar STAT1–GITRL‑signalering för att forma en immunsuppressiv CRC‑mikromiljö
Varför detta är viktigt för cancerbehandling
Kolorektalcancer är en av de vanligaste och mest dödliga cancerformerna i världen, och många patienter svarar inte väl på dagens immunoterapier. Denna studie avslöjar en dold molekylär ”broms” inne i tumörceller som påverkar hur immunsystemet beter sig i och runt kolorektala tumörer. Genom att förstå denna broms pekar forskarna på nya sätt att förutsäga vem som kan ha nytta av vissa immunstimulerande behandlingar och hur man kan få dessa terapier att fungera bättre.
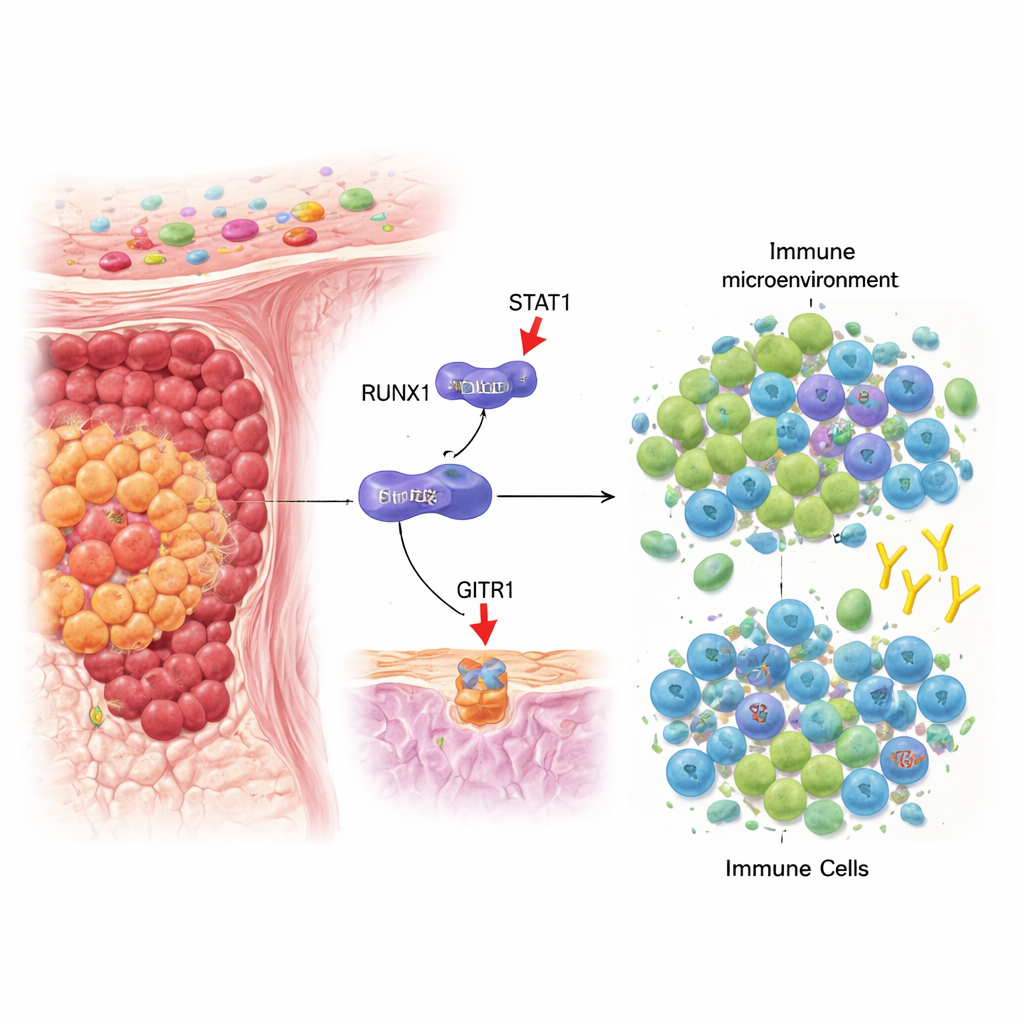
En dragkamp inne i kolontumörer
Vårt immunsystem patrullerar ständigt efter cancerceller, och två nyckelspelare i denna kamp är regulatoriska T‑celler (Tregs), som dämpar immunsvar, och CD8+ T‑celler, som kan döda tumörceller direkt. I kolorektalcancer utvecklar många tumörer en miljö som gynnar Tregs framför cytotoxiska T‑celler, vilket tillåter cancern att växa ostört. Författarna fokuserade på en gen kallad RUNX1, redan känd för att påverka hur blod‑ och solida tumörer beter sig, och undersökte om den också kan påverka denna immunskevhet i kolorektala tumörer.
En dold strömbrytare som kontrollerar immunsignaler
Genom att analysera patienttumörprover och stora cancer databaser fann teamet att kolorektala tumörer med höga nivåer av RUNX1 tenderade att ha låga nivåer av en ytmolekyl kallad GITRL och fler Tregs. GITRL sitter på tumörceller och andra celler och kan interagera med en partnersignal, GITR, på T‑celler. När GITRL binder GITR försvagas vanligtvis Treg‑aktiviteten och CD8+ T‑cellernas funktion stärks, vilket tippar balansen mot antitumoral immunitet. Experiment i cellinjer visade att minskad RUNX1 ökade GITRL, medan ökad RUNX1 minskade den, vilket tyder på att RUNX1 fungerar som en negativ regulator av denna immunstimulerande signal.
Hur ett protein blockerar ett annat
Forskarna frågade sedan hur RUNX1 sänker GITRL‑nivåerna. I stället för att binda direkt till GITRL‑genen interagerar RUNX1 fysiskt med ett annat protein kallat STAT1, en välkänd responder på immunsignalen interferon‑gamma. Normalt, när interferon‑gamma finns närvarande, bildar STAT1 par, rör sig in i nukleus och aktiverar gener som GITRL. Studien visar att RUNX1 binder STAT1 i cellens cytoplasma, förhindrar effektiv dimerisering av STAT1 och minskar dess överföring till kärnan. Som ett resultat får STAT1 svårare att aktivera GITRL‑genen, och tumörcellerna visar mindre GITRL på sin yta. Denna molekylära blockering gynnar i slutändan uppbyggnaden av Tregs och försvagar CD8+ T‑cellsaktivering i tumörmikromiljön.
Från musmodeller till terapeutisk potential
För att se hur detta spelar ut i levande organismer använde teamet muskolorektala tumörer konstruerade för att ändra RUNX1‑ eller GITRL‑nivåer. Tumörer rika på GITRL växte långsammare, hade färre Tregs och innehöll fler aktiverade CD8+ T‑celler. Däremot växte tumörer med extra RUNX1 snabbare, rymde fler Tregs och hade färre aktiva cytotoxiska T‑celler. Viktigt är att när dessa RUNX1‑rika tumörer behandlades med en experimentell antikropp som stimulerar GITR—efterliknande effekten av GITRL på T‑celler—blev tumörerna mycket mer känsliga för behandlingen och deras tillväxt minskade. Detta tyder på att när RUNX1 undertrycker tumörcells‑GITRL lämnar det fler GITR‑bärande Tregs kvar att riktas och utplånas av läkemedlet.
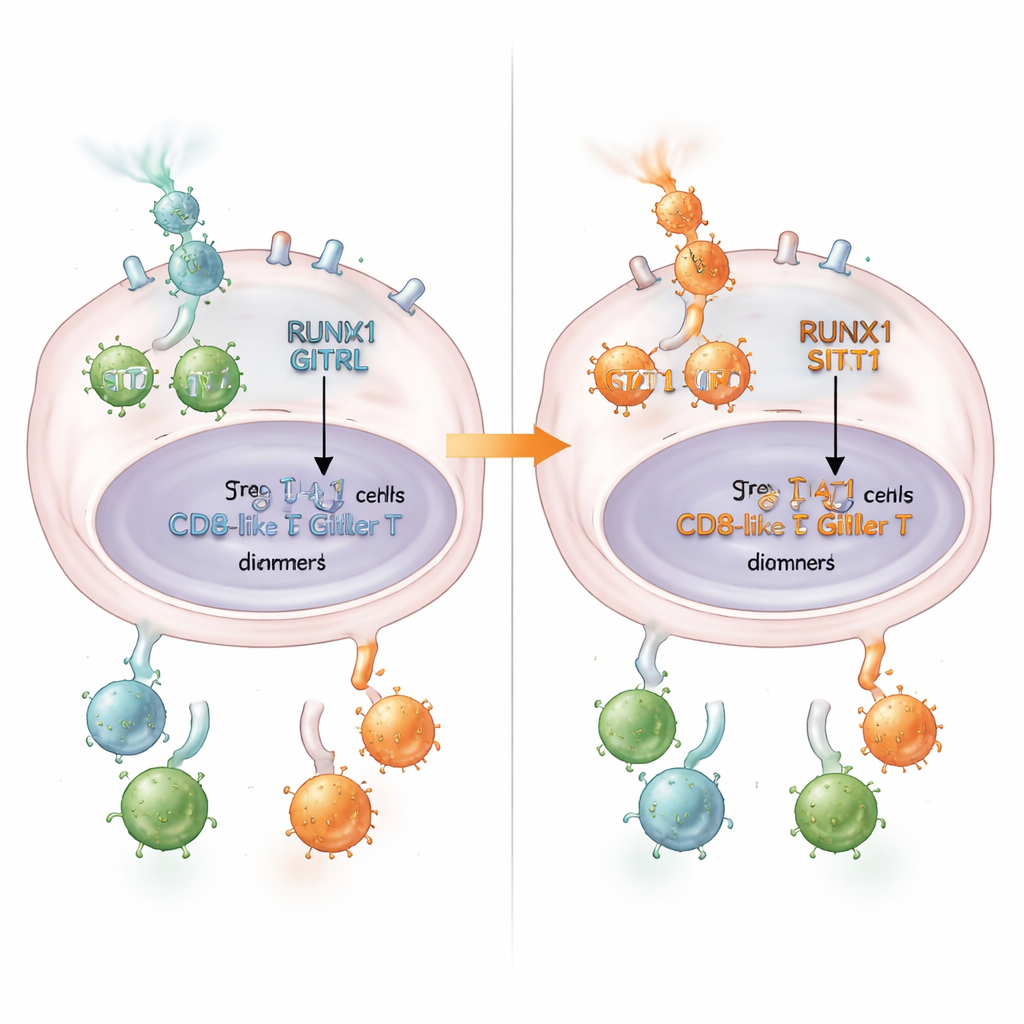
Vad detta betyder för patienter
Enkelt uttryckt visar detta arbete en händelsekedja där RUNX1 fungerar som en grindvakt: den håller tillbaka STAT1, sänker GITRL, uppmuntrar fredsbevarande Tregs och dämpar cancerbekämpande CD8+ T‑celler. Den kedjan hjälper till att förklara varför vissa kolorektala tumörer är mer immunsuppressiva än andra. Resultaten tyder på att mätning av RUNX1‑ och GITRL‑nivåer i tumörer kan hjälpa till att identifiera patienter som har större chans att gynnas av läkemedel som stimulerar GITR. På längre sikt kan terapier som lösgör RUNX1:s grepp om STAT1—eller på annat sätt återställer RUNX1/STAT1/GITRL‑axeln—återväcka immunsystemet inne i kolorektala tumörer och förbättra framgången för immunoterapi.
Citering: He, W., Zheng, L., Huang, W. et al. RUNX1 restrains STAT1-GITRL signaling to shape an immunosuppressive CRC microenvironment. Cell Death Discov. 12, 151 (2026). https://doi.org/10.1038/s41420-026-03053-7
Nyckelord: kolorektalcancer, tumörmikromiljö, regulatoriska T‑celler, GITR‑immunoterapi, RUNX1 STAT1‑signalering