Clear Sky Science · pl
RUNX1 ogranicza sygnalizację STAT1-GITRL, kształtując immunosupresyjne mikrośrodowisko raka jelita grubego
Dlaczego to ma znaczenie dla leczenia raka
Rak jelita grubego jest jednym z najczęściej występujących i najgroźniejszych nowotworów na świecie, a wielu pacjentów słabo reaguje na dostępne dziś leki immunoterapeutyczne. Badanie ujawnia ukrytą molekularną „hamulcową” w komórkach nowotworowych, która kształtuje zachowanie układu odpornościowego w obrębie i wokół guzów jelita grubego. Zrozumienie tego mechanizmu wskazuje nowe sposoby przewidywania, kto może skorzystać z określonych terapii wzmacniających odporność, oraz jak zwiększyć skuteczność tych terapii.
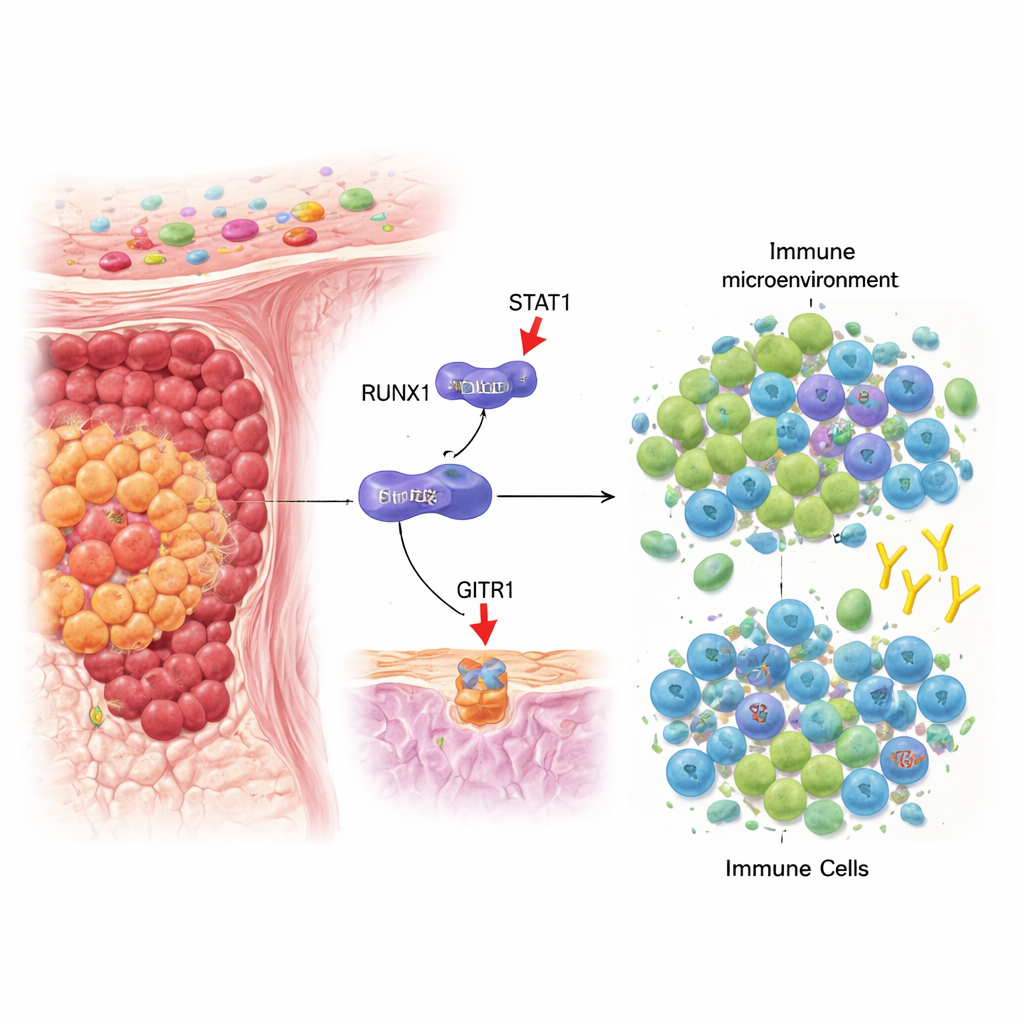
Tocząca się walka wewnątrz guzów jelita
Nasz układ odpornościowy nieustannie patroluje w poszukiwaniu komórek nowotworowych; dwoma kluczowymi uczestnikami tej walki są limfocyty T regulatorowe (Treg), które tłumią odpowiedzi odpornościowe, oraz limfocyty CD8+, zdolne bezpośrednio zabijać komórki nowotworowe. W raku jelita grubego wiele guzów tworzy środowisko sprzyjające Treg w stosunku do komórek zabójczych, co pozwala nowotworowi rosnąć bez kontroli. Autorzy skoncentrowali się na genie RUNX1, już znanym z wpływu na zachowanie nowotworów krwi i tkanek stałych, i sprawdzili, czy może on również wpływać na tę równowagę immunologiczną w obrębie guzów jelita grubego.
Ukryty przełącznik kontrolujący sygnały immunologiczne
Analizując próbki guzów od pacjentów i duże bazy danych nowotworowych, zespół odkrył, że guzy jelita grubego o wysokim poziomie RUNX1 mają zwykle niski poziom cząsteczki powierzchniowej zwanej GITRL oraz większą liczbę Treg. GITRL występuje na komórkach nowotworowych i innych komórkach i może wchodzić w interakcję z partnerem GITR na limfocytach T. Kiedy GITRL wiąże się z GITR, zwykle osłabia aktywność Treg i wzmacnia funkcję limfocytów CD8+, przechylając szalę na stronę odporności przeciwnowotworowej. Eksperymenty na liniach komórkowych wykazały, że zmniejszenie poziomu RUNX1 zwiększa GITRL, podczas gdy jego nadekspresja redukuje GITRL, co sugeruje, że RUNX1 działa jako negatywny regulator tego sygnału stymulującego odporność.
Jak jeden białko blokuje drugie
Naukowcy następnie zbadali, w jaki sposób RUNX1 obniża poziom GITRL. Zamiast wiązać się bezpośrednio z genem GITRL, RUNX1 fizycznie oddziałuje z innym białkiem, STAT1, dobrze znanym rezponderem na interferon‑gamma. Zwykle, gdy obecny jest interferon‑gamma, STAT1 tworzy dimery, przechodzi do jądra komórkowego i włącza geny, takie jak GITRL. Badanie pokazuje, że RUNX1 wiąże się ze STAT1 w cytoplazmie, utrudnia jego efektywne dimerowanie i zmniejsza przemieszczanie do jądra. W rezultacie STAT1 ma trudniej z aktywacją genu GITRL, a komórki nowotworowe wykazują mniej GITRL na swojej powierzchni. Ta molekularna blokada sprzyja nagromadzeniu Treg i osłabia aktywację limfocytów CD8+ w mikrośrodowisku guza.
Od modeli mysich do potencjału terapeutycznego
Aby sprawdzić, jak to wygląda in vivo, zespół wykorzystał mysie guzy jelita grubego zmodyfikowane w celu zmiany poziomów RUNX1 lub GITRL. Guzy bogate w GITRL rosły wolniej, miały mniej Treg i zawierały więcej aktywowanych limfocytów CD8+. Natomiast guzy z nadmiarem RUNX1 rosły szybciej, gromadziły więcej Treg i miały mniej aktywnych komórek zabójczych. Co ważne, gdy te guzy o wysokim poziomie RUNX1 leczono eksperymentalnym przeciwciałem stymulującym GITR — naśladującym efekt GITRL na limfocyty T — guzy stały się znacznie bardziej wrażliwe na terapię, a ich wzrost spowolnił. Sugeruje to, że gdy RUNX1 tłumi GITRL w komórkach guza, pozostawia więcej Treg z GITR, które lek może zaatakować i usunąć.
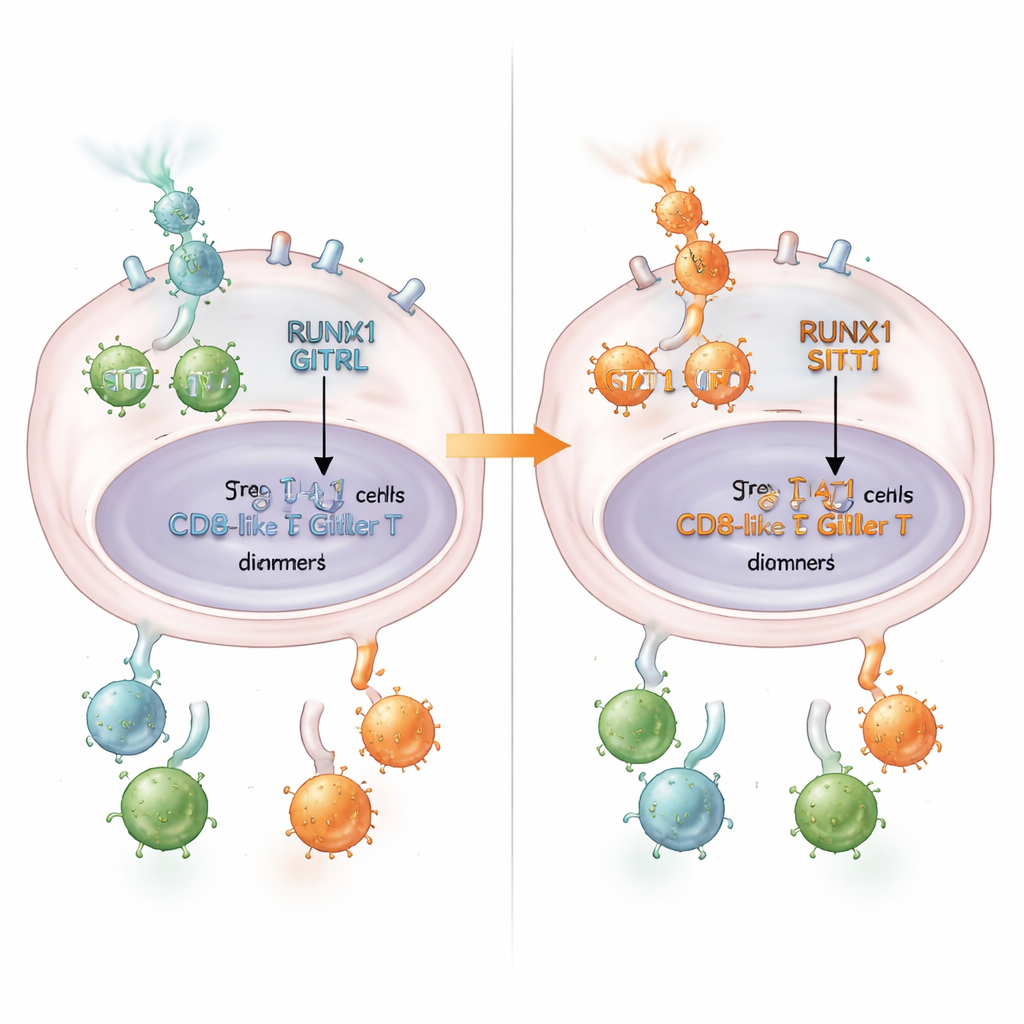
Co to oznacza dla pacjentów
Mówiąc prosto, praca ta odkrywa ciąg zdarzeń, w którym RUNX1 działa jak strażnik: powstrzymuje STAT1, obniża GITRL, sprzyja pokojowo nastawionym Treg i tłumi odporność komórkową CD8+. Ten łańcuch pomaga wyjaśnić, dlaczego niektóre guzy jelita grubego są bardziej immunosupresyjne niż inne. Wyniki sugerują, że pomiar poziomów RUNX1 i GITRL w guzach mógłby pomóc wytypować pacjentów bardziej skłonnych do skorzystania z leków stymulujących GITR. W dłuższej perspektywie terapie rozluźniające wpływ RUNX1 na STAT1 — lub w inny sposób przywracające oś RUNX1/STAT1/GITRL — mogłyby pobudzić układ odpornościowy w guzach jelita grubego i poprawić skuteczność immunoterapii.
Cytowanie: He, W., Zheng, L., Huang, W. et al. RUNX1 restrains STAT1-GITRL signaling to shape an immunosuppressive CRC microenvironment. Cell Death Discov. 12, 151 (2026). https://doi.org/10.1038/s41420-026-03053-7
Słowa kluczowe: rak jelita grubego, mikrośrodowisko guza, limfocyty T regulatorowe, immunoterapia GITR, szlak RUNX1 STAT1