Clear Sky Science · de
RUNX1 bremst STAT1‑GITRL‑Signalgebung und formt ein immunsuppressives CRC‑Mikromilieu
Warum das für die Krebsbehandlung wichtig ist
Kolorektales Karzinom gehört zu den häufigsten und tödlichsten Krebserkrankungen weltweit, und viele Patientinnen und Patienten sprechen nur schlecht auf die heute verfügbaren Immuntherapien an. Diese Studie deckt eine versteckte molekulare „Bremse“ in Tumorzellen auf, die beeinflusst, wie das Immunsystem in und um kolorektale Tumoren reagiert. Das Verständnis dieser Bremse weist auf neue Wege hin, vorherzusagen, wer von bestimmten immunstimulierenden Behandlungen profitieren könnte, und wie sich solche Therapien wirksamer machen lassen.
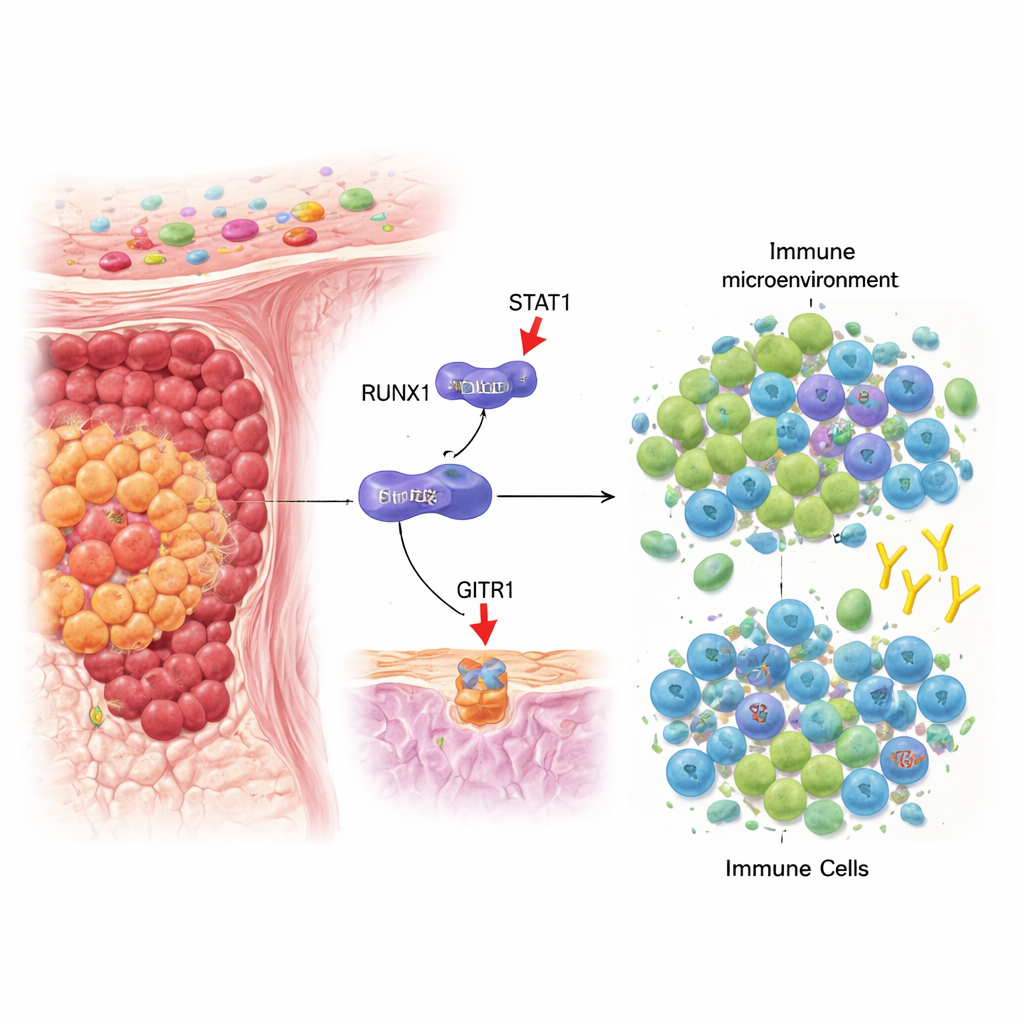
Ein Tauziehen in Darmtumoren
Unser Immunsystem patrouilliert ständig auf der Suche nach Krebszellen; zwei zentrale Akteure dieses Kampfes sind regulatorische T‑Zellen (Tregs), die Immunreaktionen abschwächen, und CD8+‑T‑Zellen, die Tumorzellen direkt abtöten können. Bei kolorektalen Karzinomen entwickeln viele Tumoren ein Milieu, das Tregs gegenüber Killer‑T‑Zellen bevorzugt, wodurch das Wachstum des Krebses ungehindert bleibt. Die Autorinnen und Autoren konzentrierten sich auf ein Gen namens RUNX1, das bereits als Einflussfaktor für Blut‑ und soliden Tumoren bekannt ist, und untersuchten, ob es auch dieses immunologische Gleichgewicht in kolorektalen Tumoren steuert.
Ein versteckter Schalter, der Immunsignale kontrolliert
Durch die Analyse von Patientenproben und großen Krebsdatenbanken fanden die Forschenden heraus, dass kolorektale Tumoren mit hohen RUNX1‑Werten tendenziell niedrige Werte des Oberflächenmoleküls GITRL und höhere Zahlen an Tregs aufwiesen. GITRL sitzt auf Tumorzellen und anderen Zellen und kann mit dem Partnermolekül GITR auf T‑Zellen interagieren. Wenn GITRL an GITR bindet, schwächt das in der Regel die Aktivität von Tregs und stärkt die Funktion von CD8+‑T‑Zellen, was die Waage zugunsten der anti‑tumoralen Immunität kippt. Zelllinienexperimente zeigten, dass eine Verminderung von RUNX1 GITRL erhöhte, während eine Erhöhung von RUNX1 GITRL reduzierte, was darauf hindeutet, dass RUNX1 als negativer Regulator dieses immunstimulierenden Signals wirkt.
Wie ein Protein ein anderes blockiert
Die Forschenden fragten dann, wie RUNX1 die GITRL‑Werte senkt. Anstatt direkt an das GITRL‑Gen zu binden, interagiert RUNX1 physisch mit einem anderen Protein namens STAT1, einem bekannten Antwortgeber auf den Immunboten Interferon‑gamma. Normalerweise bildet STAT1 bei Anwesenheit von Interferon‑gamma Paare, wandert in den Zellkern und schaltet Gene wie GITRL an. Die Studie zeigt, dass RUNX1 STAT1 im Zellplasma bindet, die effiziente Partnerbildung von STAT1 verhindert und seinen Transport in den Kern reduziert. Dadurch hat STAT1 es schwerer, das GITRL‑Gen zu aktivieren, und Tumorzellen zeigen weniger GITRL auf ihrer Oberfläche. Diese molekulare Blockade begünstigt letztlich die Ansammlung von Tregs und schwächt die Aktivierung von CD8+‑T‑Zellen im Tumormikromilieu.
Von Mausmodellen zu therapeutischem Potenzial
Um die Auswirkungen im Organismus zu prüfen, verwendete das Team Mausmodelle mit kolorektalen Tumoren, in denen RUNX1‑ oder GITRL‑Spiegel verändert wurden. Tumoren mit hohem GITRL wuchsen langsamer, wiesen weniger Tregs auf und enthielten mehr aktivierte CD8+‑T‑Zellen. Im Gegensatz dazu wuchsen Tumoren mit erhöhtem RUNX1 schneller, beherbergten mehr Tregs und hatten weniger aktive Killer‑T‑Zellen. Wichtig ist, dass diese RUNX1‑reichen Tumoren, wenn sie mit einem experimentellen Antikörper behandelt wurden, der GITR stimuliert — und damit die Wirkung von GITRL auf T‑Zellen nachahmt — deutlich therapieempfindlicher wurden und ihr Wachstum gebremst war. Das deutet darauf hin, dass RUNX1‑bedingte Unterdrückung von tumoralem GITRL mehr GITR‑tragende Tregs zurücklässt, die durch das Medikament gezielt angegriffen und reduziert werden können.
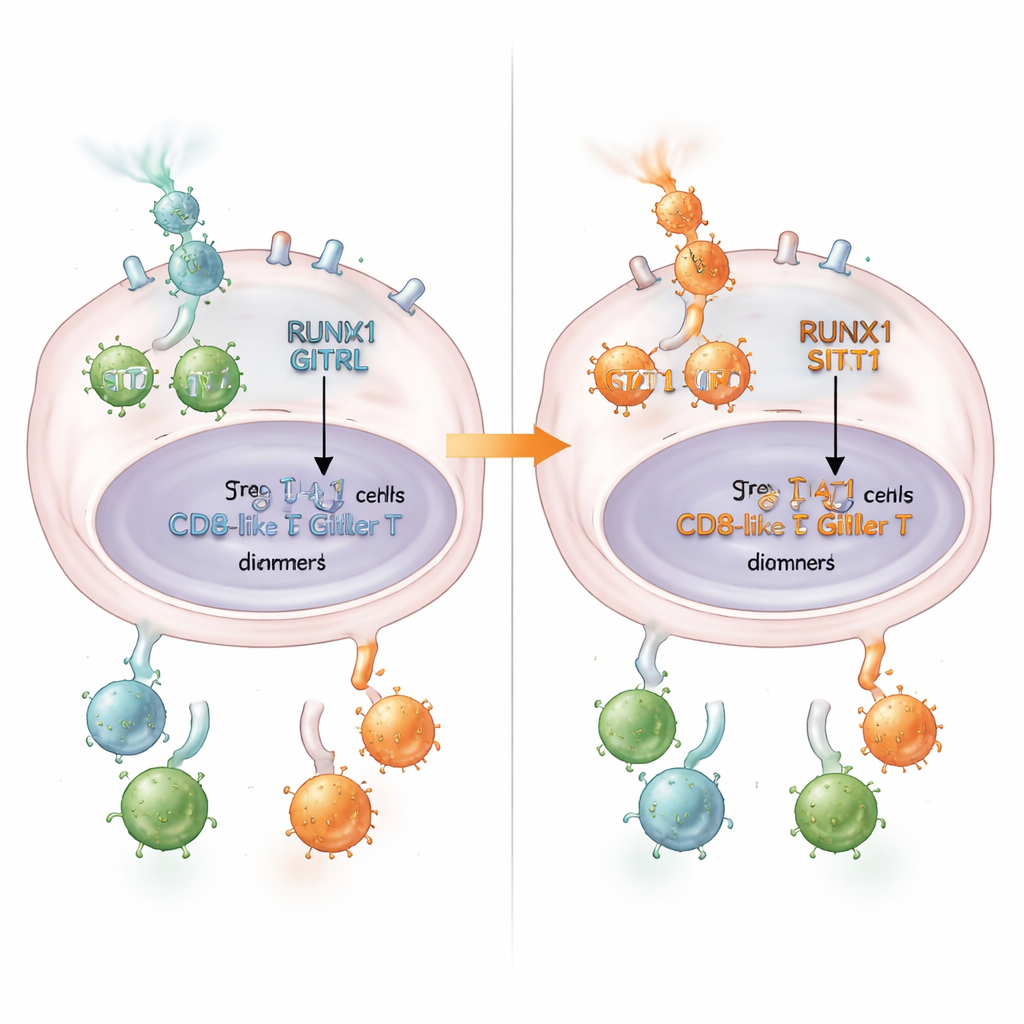
Was das für Patientinnen und Patienten bedeutet
Vereinfacht gesagt offenbart diese Arbeit eine Ereigniskette, in der RUNX1 als Torwächter fungiert: Es bremst STAT1, senkt GITRL, fördert friedensbewahrende Tregs und dämpft krebsbekämpfende CD8+‑T‑Zellen. Diese Kette hilft zu erklären, warum einige kolorektale Tumoren immunsuppressiver sind als andere. Die Ergebnisse legen nahe, dass die Messung von RUNX1‑ und GITRL‑Spiegeln in Tumoren helfen könnte, Patientinnen und Patienten zu identifizieren, die eher von GITR‑stimulierenden Medikamenten profitieren. Langfristig könnten Therapien, die RUNX1s Einfluss auf STAT1 lösen — oder die RUNX1/STAT1/GITRL‑Achse anderweitig wiederherstellen — das Immunsystem in kolorektalen Tumoren reaktivieren und so den Erfolg von Immuntherapien verbessern.
Zitation: He, W., Zheng, L., Huang, W. et al. RUNX1 restrains STAT1-GITRL signaling to shape an immunosuppressive CRC microenvironment. Cell Death Discov. 12, 151 (2026). https://doi.org/10.1038/s41420-026-03053-7
Schlüsselwörter: kolorektales Karzinom, Tumormikroumgebung, regulatorische T‑Zellen, GITR‑Immuntherapie, RUNX1‑STAT1‑Signalgebung