Clear Sky Science · es
RUNX1 controla la señalización STAT1‑GITRL para configurar un microambiente inmunosupresor en el CCR
Por qué esto importa para el tratamiento del cáncer
El cáncer colorrectal es uno de los tumores más frecuentes y mortales a nivel mundial, y muchos pacientes no responden bien a las inmunoterapias actuales. Este estudio descubre un “freno” molecular oculto dentro de las células tumorales que moldea el comportamiento del sistema inmune en y alrededor de los tumores colorrectales. Al entender este freno, los investigadores señalan nuevas formas de predecir quién podría beneficiarse de determinados tratamientos que estimulan la inmunidad y cómo mejorar la eficacia de esas terapias.
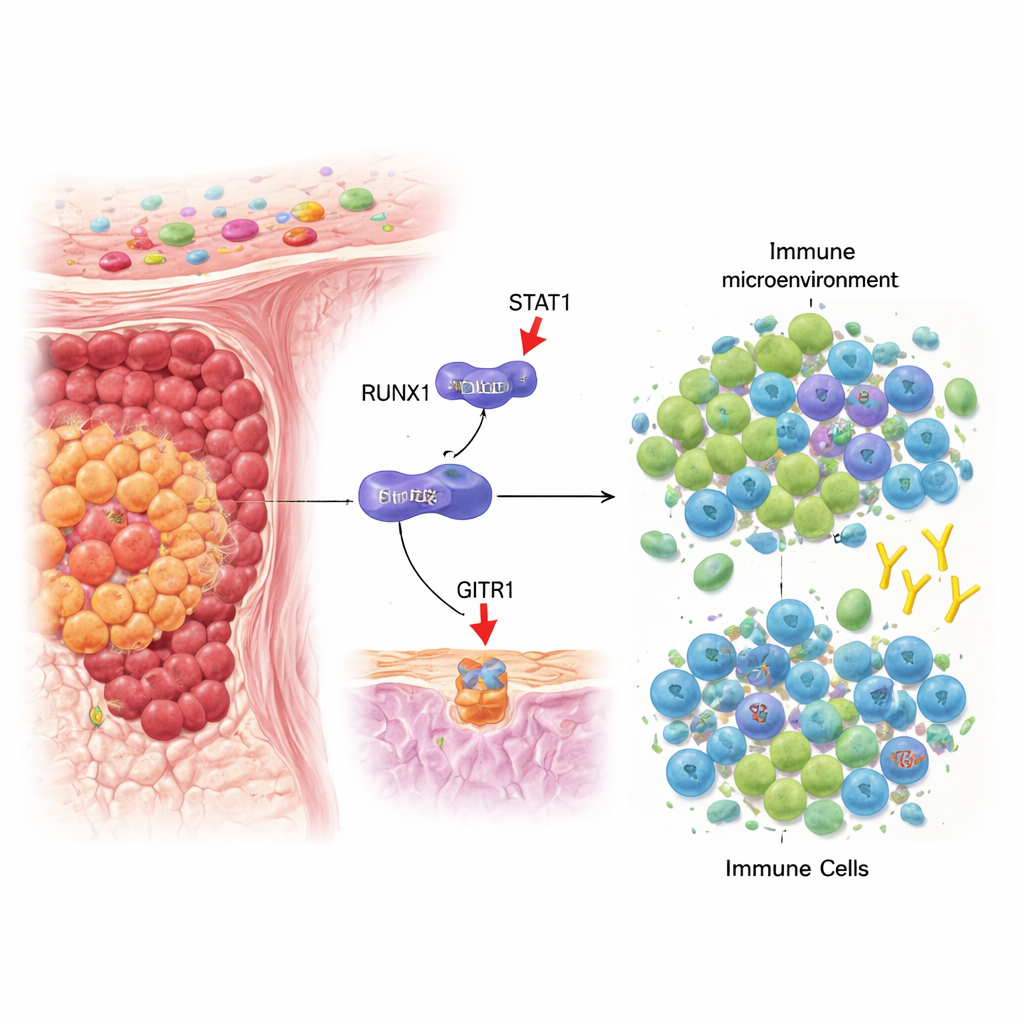
Una lucha interna dentro de los tumores de colon
Nuestro sistema inmune vigila constantemente la presencia de células cancerosas, y dos actores clave en esta batalla son las células T reguladoras (Tregs), que apagan las respuestas inmunitarias, y las células CD8+, que pueden matar directamente a las células tumorales. En el cáncer colorrectal, muchos tumores desarrollan un entorno que favorece a las Tregs frente a las células T citotóxicas, lo que permite que el cáncer crezca sin control. Los autores se centraron en un gen llamado RUNX1, ya conocido por influir en el comportamiento de tumores hematológicos y sólidos, y preguntaron si también podría afectar este equilibrio inmune dentro de los tumores colorrectales.
Un interruptor oculto que controla señales inmunes
Al analizar muestras tumorales de pacientes y grandes bases de datos de cáncer, el equipo encontró que los tumores colorrectales con niveles altos de RUNX1 tendían a presentar bajos niveles de una molécula de superficie llamada GITRL y un mayor número de Tregs. GITRL se encuentra en células tumorales y otras células y puede interactuar con una molécula compañera, GITR, en las células T. Cuando GITRL activa GITR, suele debilitar la actividad de las Tregs y potenciar la función de las células T CD8+, inclinando la balanza hacia la inmunidad antitumoral. Experimentos en líneas celulares mostraron que reducir RUNX1 aumentaba GITRL, mientras que aumentar RUNX1 lo reducía, lo que sugiere que RUNX1 actúa como un regulador negativo de esta señal que estimula el sistema inmune.
Cómo una proteína bloquea a otra
Los investigadores preguntaron entonces cómo RUNX1 reduce los niveles de GITRL. En lugar de unirse directamente al gen de GITRL, RUNX1 interactúa físicamente con otra proteína llamada STAT1, un conocido respondededor al mensajero inmune interferón‑gamma. Normalmente, cuando hay interferón‑gamma, STAT1 forma dímeros, se traslada al núcleo y activa genes como GITRL. El estudio muestra que RUNX1 se une a STAT1 en el compartimento citosólico, dificulta su dimerización y reduce su entrada en el núcleo. Como resultado, STAT1 tiene más dificultades para activar el gen GITRL, y las células tumorales muestran menos GITRL en su superficie. Este bloqueo molecular favorece finalmente la acumulación de Tregs y debilita la activación de las células T CD8+ en el microambiente tumoral.
De modelos en ratón al potencial terapéutico
Para ver cómo se manifiesta esto en organismos vivos, el equipo utilizó tumores colorrectales de ratón diseñados para alterar los niveles de RUNX1 o GITRL. Los tumores ricos en GITRL crecieron más despacio, presentaron menos Tregs y contenían más células CD8+ activadas. En cambio, los tumores con exceso de RUNX1 crecieron más rápido, alojaron más Tregs y tenían menos células T citotóxicas activas. De forma importante, cuando estos tumores con alto RUNX1 fueron tratados con un anticuerpo experimental que estimula GITR—imitando el efecto de GITRL sobre las células T—los tumores se volvieron mucho más sensibles a la terapia y su crecimiento se ralentizó. Esto sugiere que cuando RUNX1 suprime GITRL en las células tumorales, deja más Tregs con GITR disponibles para que el fármaco los apunte y deplete.
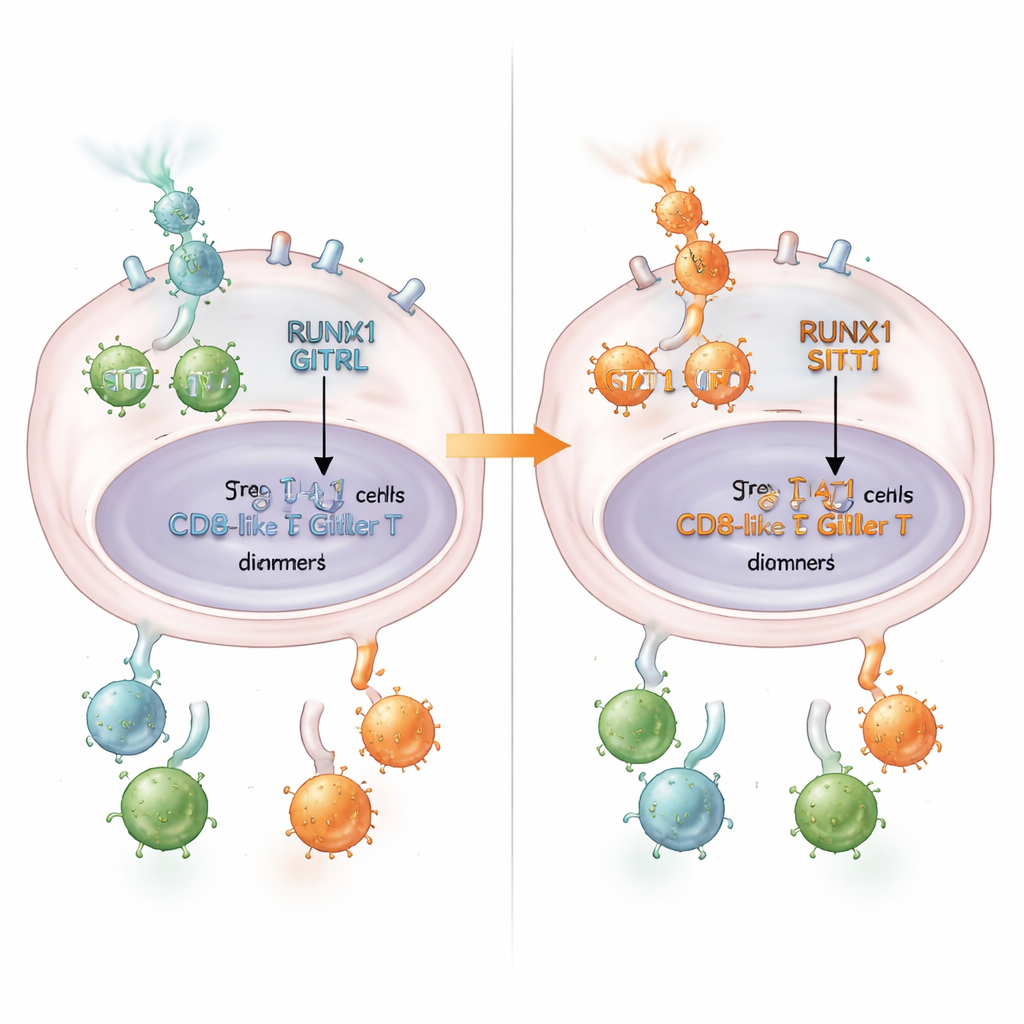
Qué significa esto para los pacientes
En términos accesibles, este trabajo revela una cadena de eventos en la que RUNX1 actúa como portero: frena a STAT1, reduce GITRL, favorece a las Tregs pacificadoras y atenúa a las células T CD8+ que combaten el cáncer. Esa cadena ayuda a explicar por qué algunos tumores colorrectales son más inmunosupresores que otros. Los hallazgos sugieren que medir los niveles de RUNX1 y GITRL en los tumores podría ayudar a identificar a los pacientes con más probabilidad de beneficiarse de fármacos que estimulen GITR. A más largo plazo, terapias que aflojen el control de RUNX1 sobre STAT1—o que, de otro modo, restauren el eje RUNX1/STAT1/GITRL—podrían reactivar el sistema inmune dentro de los tumores colorrectales y mejorar el éxito de la inmunoterapia.
Cita: He, W., Zheng, L., Huang, W. et al. RUNX1 restrains STAT1-GITRL signaling to shape an immunosuppressive CRC microenvironment. Cell Death Discov. 12, 151 (2026). https://doi.org/10.1038/s41420-026-03053-7
Palabras clave: cáncer colorrectal, microambiente tumoral, células T reguladoras, inmunoterapia GITR, señalización RUNX1 STAT1