Clear Sky Science · fr
RUNX1 freine la signalisation STAT1-GITRL pour façonner un micro‑environnement CRC immunosuppresseur
Pourquoi c’est important pour le traitement du cancer
Le cancer colorectal est l’un des cancers les plus fréquents et les plus meurtriers dans le monde, et de nombreux patients ne répondent pas bien aux traitements immunothérapeutiques actuels. Cette étude met au jour un « frein » moléculaire caché au sein des cellules tumorales qui façonne le comportement du système immunitaire dans et autour des tumeurs colorectales. En comprenant ce frein, les chercheurs ouvrent la voie à de nouvelles méthodes pour prédire qui pourrait bénéficier de certains traitements visant à stimuler l’immunité et pour améliorer l’efficacité de ces thérapies.
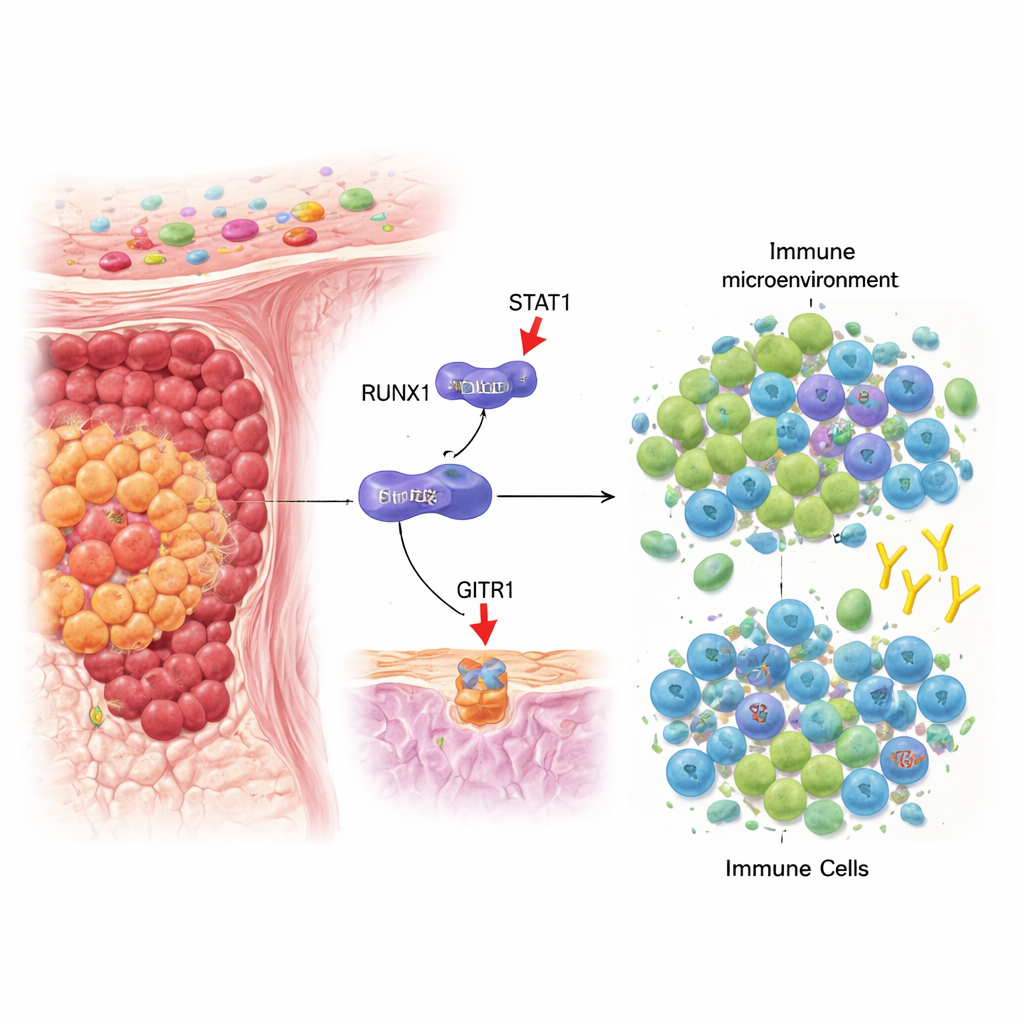
Une lutte de pouvoir au cœur des tumeurs du côlon
Notre système immunitaire patrouille en permanence à la recherche de cellules cancéreuses ; deux acteurs clés de cette bataille sont les cellules T régulatrices (Tregs), qui calment les réponses immunitaires, et les cellules T CD8+, capables de tuer directement les cellules tumorales. Dans le cancer colorectal, de nombreuses tumeurs développent un environnement qui favorise les Tregs au détriment des cellules T cytotoxiques, permettant ainsi au cancer de se développer sans contrôle. Les auteurs se sont intéressés à un gène nommé RUNX1, déjà connu pour influencer le comportement des tumeurs solides et hématologiques, et ont cherché s’il pouvait aussi modifier cet équilibre immunitaire au sein des tumeurs colorectales.
Un commutateur caché qui contrôle les signaux immunitaires
En analysant des échantillons tumoraux de patients et de larges bases de données sur le cancer, l’équipe a constaté que les tumeurs colorectales présentant des niveaux élevés de RUNX1 avaient tendance à afficher de faibles niveaux d’une molécule de surface appelée GITRL et un nombre accru de Tregs. GITRL est exprimée à la surface des cellules tumorales et d’autres cellules et peut interagir avec une molécule partenaire, GITR, sur les cellules T. Lorsque GITRL active GITR, cela affaiblit généralement l’activité des Tregs et renforce la fonction des cellules T CD8+, basculant l’équilibre en faveur de l’immunité anti‑tumorale. Des expériences sur des lignées cellulaires ont montré qu’abaisser RUNX1 augmentait GITRL, tandis qu’augmenter RUNX1 le réduisait, ce qui suggère que RUNX1 agit comme un régulateur négatif de ce signal stimulant l’immunité.
Comment une protéine bloque une autre
Les chercheurs se sont ensuite demandé comment RUNX1 diminue les niveaux de GITRL. Plutôt que de se lier directement au gène GITRL, RUNX1 interagit physiquement avec une autre protéine appelée STAT1, bien connue pour répondre au messager immunitaire interféron‑gamma. Normalement, en présence d’interféron‑gamma, STAT1 forme des dimères, migre vers le noyau et active l’expression de gènes tels que GITRL. L’étude montre que RUNX1 se lie à STAT1 dans le compartiment cytoplasmique, empêche un appariement efficace de STAT1 et réduit sa translocation nucléaire. En conséquence, STAT1 a plus de difficulté à activer le gène GITRL, et les cellules tumorales affichent moins de GITRL à leur surface. Ce blocage moléculaire favorise finalement l’accumulation de Tregs et affaiblit l’activation des cellules T CD8+ dans le microenvironnement tumoral.
Des modèles murins au potentiel thérapeutique
Pour évaluer ces mécanismes in vivo, l’équipe a utilisé des tumeurs colorectales murines conçues pour modifier les niveaux de RUNX1 ou de GITRL. Les tumeurs riches en GITRL croissaient plus lentement, comptaient moins de Tregs et contenaient davantage de cellules T CD8+ activées. En revanche, les tumeurs surexprimant RUNX1 croissaient plus rapidement, abritaient plus de Tregs et présentaient moins de cellules T tueuses actives. Fait important, lorsque ces tumeurs à fort RUNX1 étaient traitées par un anticorps expérimental stimulant GITR — imitant l’effet de GITRL sur les cellules T — les tumeurs devenaient beaucoup plus sensibles au traitement et leur croissance ralentissait. Cela suggère que lorsque RUNX1 supprime le GITRL des cellules tumorales, il laisse en place davantage de Tregs porteurs de GITR que le médicament peut cibler et éliminer.
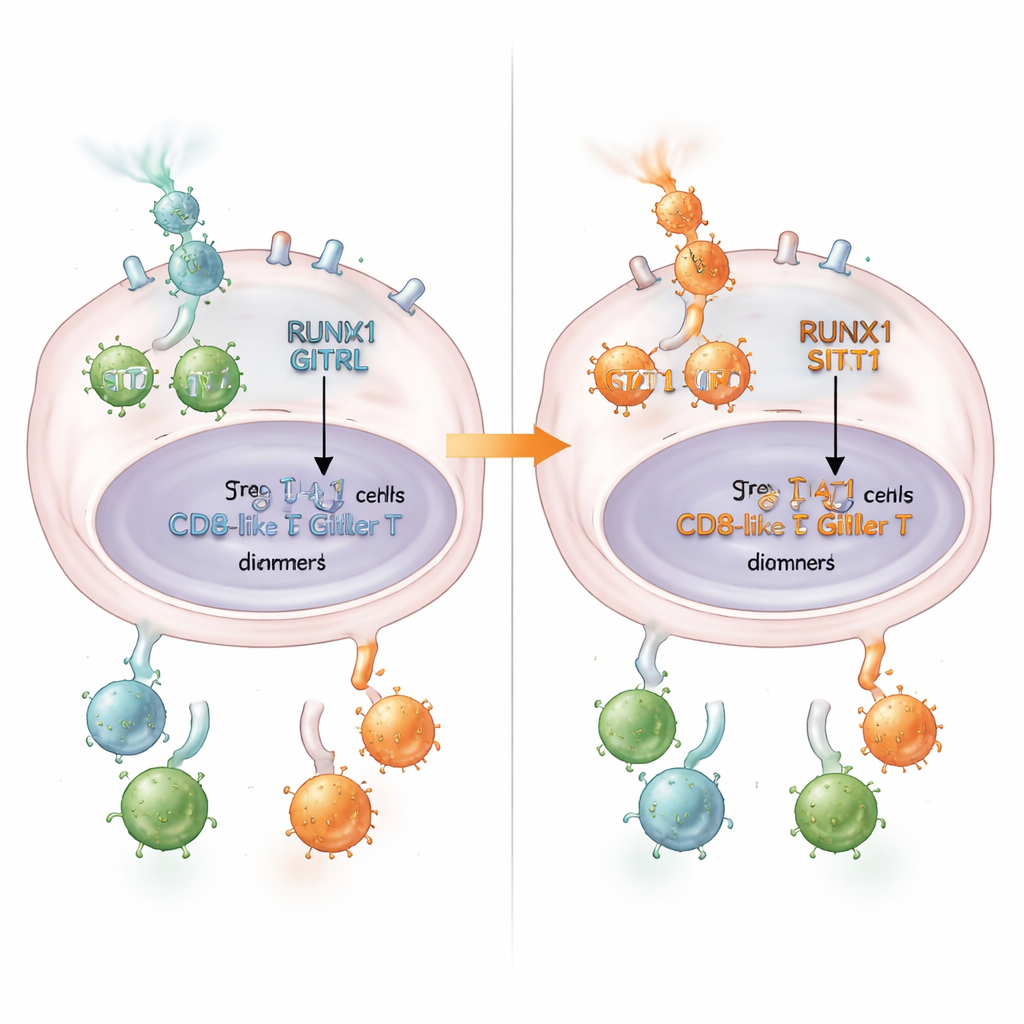
Ce que cela signifie pour les patients
En termes accessibles, ce travail révèle une chaîne d’événements où RUNX1 joue le rôle de gardien : il retient STAT1, abaisse GITRL, favorise les Tregs pacificateurs et atténue les cellules T CD8+ anti‑cancer. Cette chaîne aide à expliquer pourquoi certaines tumeurs colorectales sont plus immunosuppressives que d’autres. Les résultats suggèrent que mesurer les niveaux de RUNX1 et de GITRL dans les tumeurs pourrait aider à identifier les patients susceptibles de bénéficier de médicaments qui stimulent GITR. À plus long terme, des thérapies qui desserrent l’emprise de RUNX1 sur STAT1 — ou qui rétablissent autrement l’axe RUNX1/STAT1/GITRL — pourraient réveiller le système immunitaire au sein des tumeurs colorectales et améliorer le succès de l’immunothérapie.
Citation: He, W., Zheng, L., Huang, W. et al. RUNX1 restrains STAT1-GITRL signaling to shape an immunosuppressive CRC microenvironment. Cell Death Discov. 12, 151 (2026). https://doi.org/10.1038/s41420-026-03053-7
Mots-clés: cancer colorectal, microenvironnement tumoral, cellules T régulatrices, immunothérapie GITR, signalisation RUNX1 STAT1