Clear Sky Science · it
RUNX1 limita la segnalazione STAT1-GITRL per modellare un microambiente immunosoppressivo nel CRC
Perché questo è importante per il trattamento del cancro
Il cancro colorettale è tra i tumori più comuni e letali a livello mondiale, e molti pazienti non rispondono bene alle immunoterapie attuali. Questo studio scopre un “freno” molecolare nascosto nelle cellule tumorali che modella il comportamento del sistema immunitario dentro e intorno ai tumori colorettali. Capire questo freno suggerisce nuovi modi per prevedere chi potrebbe trarre beneficio da certi trattamenti che potenziano l’immunità e come rendere tali terapie più efficaci.
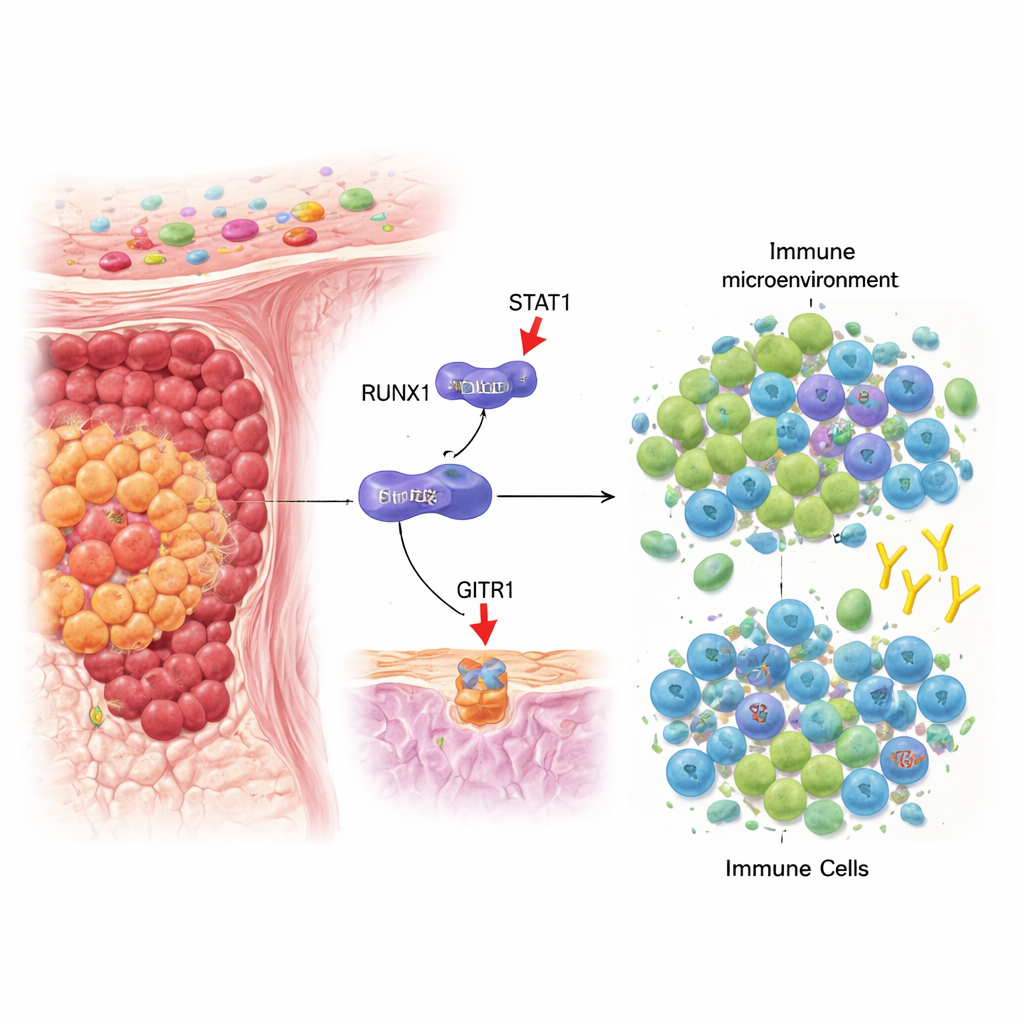
Una lotta interna nei tumori del colon
Il nostro sistema immunitario pattuglia continuamente alla ricerca di cellule tumorali; due attori chiave in questa battaglia sono le cellule T regolatorie (Treg), che attenuano le risposte immunitarie, e le cellule T CD8+, che possono uccidere direttamente le cellule tumorali. Nel cancro colorettale molti tumori sviluppano un ambiente che favorisce le Treg rispetto alle cellule T citotossiche, permettendo al tumore di crescere indisturbato. Gli autori si sono concentrati su un gene chiamato RUNX1, già noto per influenzare il comportamento di tumori ematologici e solidi, e si sono chiesti se possa anche alterare questo equilibrio immunitario nei tumori colorettali.
Un interruttore nascosto che controlla i segnali immunitari
Analizzando campioni tumorali di pazienti e ampi database sul cancro, il gruppo ha trovato che i tumori colorettali con alti livelli di RUNX1 tendevano ad avere bassi livelli di una molecola di superficie chiamata GITRL e un numero maggiore di Treg. GITRL è presente sulle cellule tumorali e su altre cellule e può interagire con il suo partner GITR sulle cellule T. Quando GITRL lega GITR, generalmente indebolisce l’attività delle Treg e potenzia la funzione delle cellule T CD8+, inclinando l’equilibrio verso l’immunità antitumorale. Esperimenti su linee cellulari hanno mostrato che ridurre RUNX1 aumenta GITRL, mentre aumentare RUNX1 lo riduce, suggerendo che RUNX1 funzioni come regolatore negativo di questo segnale immunostimolante.
Come una proteina blocca un’altra
I ricercatori hanno quindi indagato come RUNX1 riduca i livelli di GITRL. Invece di legarsi direttamente al gene GITRL, RUNX1 interagisce fisicamente con un’altra proteina chiamata STAT1, nota per rispondere all’interferone-gamma. Normalmente, in presenza di interferone-gamma, STAT1 forma dimeri, entra nel nucleo e attiva geni come GITRL. Lo studio mostra che RUNX1 lega STAT1 nel compartimento citosolico, impedendo un’efficiente dimerizzazione di STAT1 e riducendone il trasporto nel nucleo. Di conseguenza, STAT1 attiva meno il gene GITRL e le cellule tumorali espongono meno GITRL sulla loro superficie. Questo blocco molecolare favorisce l’accumulo di Treg e indebolisce l’attivazione delle cellule T CD8+ nel microambiente tumorale.
Dai modelli murini al potenziale terapeutico
Per osservare l’effetto negli organismi viventi, il gruppo ha usato tumori colorettali murini ingegnerizzati per modificare i livelli di RUNX1 o GITRL. I tumori ricchi di GITRL crescevano più lentamente, avevano meno Treg e contenevano più cellule T CD8+ attivate. Al contrario, tumori con RUNX1 aumentato crescevano più velocemente, ospitavano più Treg e avevano meno cellule T citotossiche attive. Importante, quando questi tumori ad alto RUNX1 sono stati trattati con un anticorpo sperimentale che stimola GITR—imitando l’effetto di GITRL sulle cellule T—i tumori sono diventati molto più sensibili alla terapia e la loro crescita è rallentata. Ciò suggerisce che, quando RUNX1 sopprime il GITRL delle cellule tumorali, lascia in situ più Treg che esprimono GITR, offrendo al farmaco bersagli da colpire e depletare.
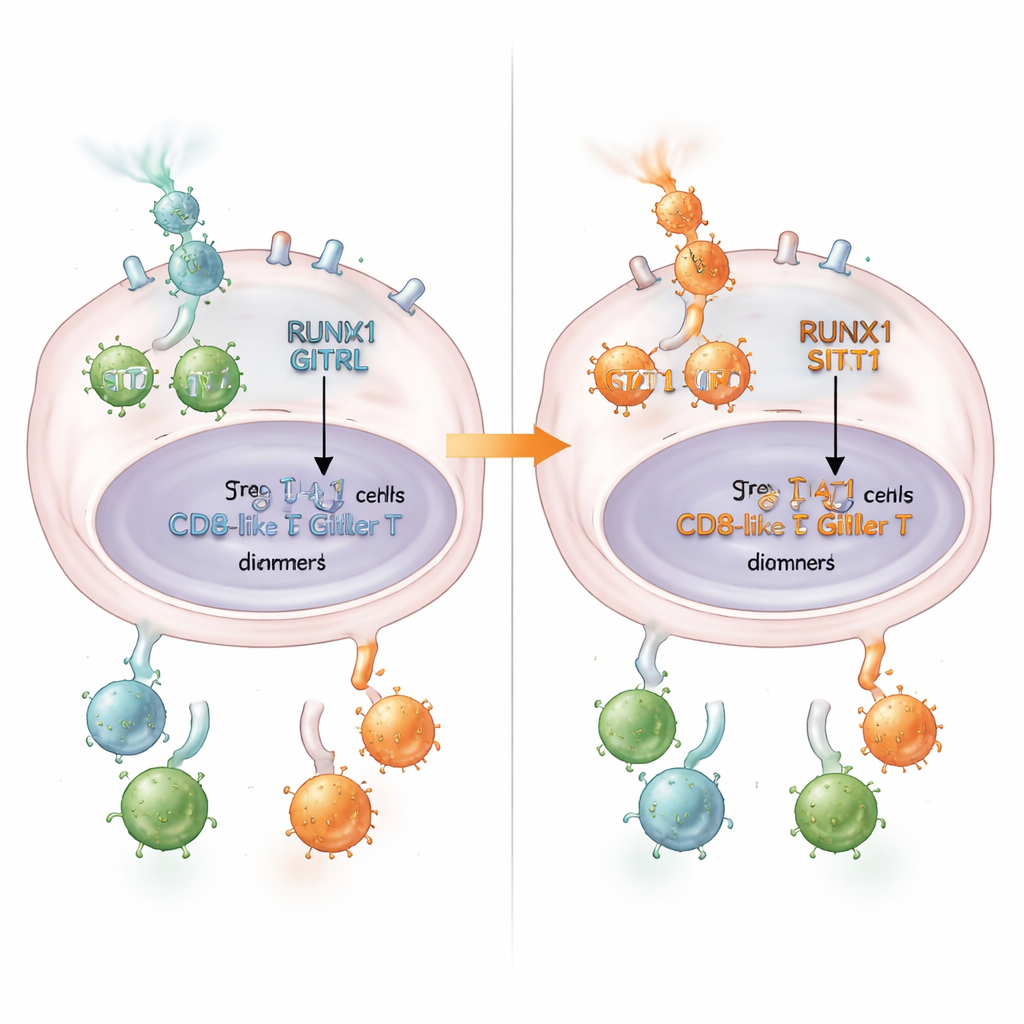
Cosa significa per i pazienti
In termini accessibili, questo lavoro rivela una catena di eventi in cui RUNX1 agisce come un guardiano: frena STAT1, abbassa GITRL, favorisce le Treg pacificatrici e attenua le cellule T CD8+ antitumorali. Questa catena aiuta a spiegare perché alcuni tumori colorettali sono più immunosoppressivi di altri. I risultati suggeriscono che misurare i livelli di RUNX1 e GITRL nei tumori potrebbe aiutare a identificare i pazienti più propensi a beneficiare di farmaci che stimolano GITR. A lungo termine, terapie che allentino il controllo di RUNX1 su STAT1—o che ripristinino l’asse RUNX1/STAT1/GITRL—potrebbero riattivare il sistema immunitario nei tumori colorettali e migliorare il successo dell’immunoterapia.
Citazione: He, W., Zheng, L., Huang, W. et al. RUNX1 restrains STAT1-GITRL signaling to shape an immunosuppressive CRC microenvironment. Cell Death Discov. 12, 151 (2026). https://doi.org/10.1038/s41420-026-03053-7
Parole chiave: cancro colorettale, microambiente tumorale, cellule T regolatorie, immunoterapia GITR, segnalazione RUNX1 STAT1