Clear Sky Science · nl
RUNX1 remt STAT1-GITRL-signaalering om een immunosuppressieve CRC-microomgeving te vormen
Waarom dit belangrijk is voor kankerbehandeling
Dikkedarmkanker is een van de meest voorkomende en dodelijke kankersoorten wereldwijd, en veel patiënten reageren niet goed op de huidige immunotherapieën. Deze studie onthult een verborgen moleculaire "rem" in tumorcellen die bepaalt hoe het immuunsysteem zich in en rondom colorectale tumoren gedraagt. Door dit remmechanisme te doorgronden, wijzen de onderzoekers op nieuwe manieren om te voorspellen wie baat kan hebben bij bepaalde immuunstimulerende behandelingen en hoe die therapieën effectiever kunnen worden gemaakt.
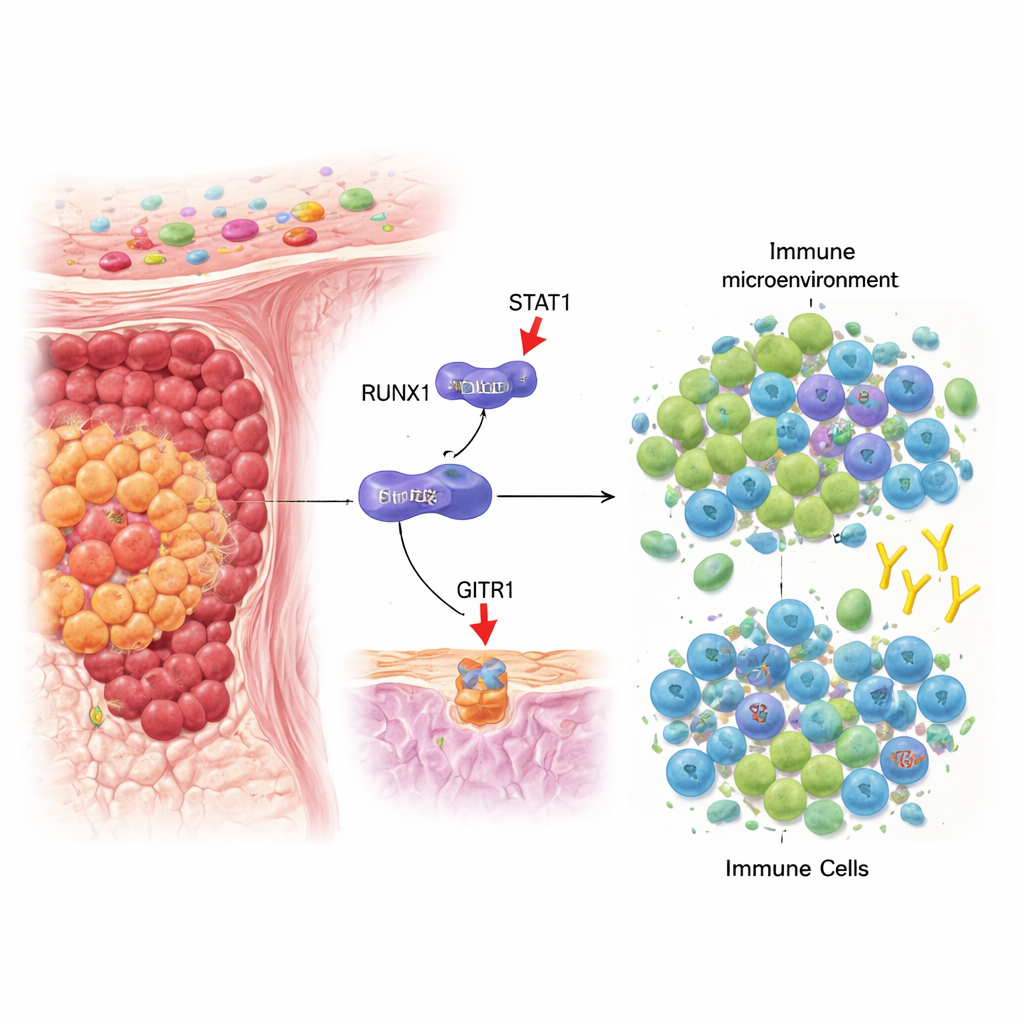
Een trekspel binnen colon‑tumoren
Ons immuunsysteem patrouilleert continu op zoek naar kankercellen, en twee belangrijke spelers in dit gevecht zijn regulatorische T‑cellen (Tregs), die immuunreacties dempen, en CD8+ T‑cellen, die tumorcellen rechtstreeks kunnen doden. Bij colorectale kanker ontwikkelen veel tumoren een omgeving die Tregs bevoordeelt boven cytotoxische T‑cellen, waardoor de kanker ongehinderd kan groeien. De auteurs richtten zich op een gen genaamd RUNX1, dat al bekendstaat om zijn invloed op bloed- en solide tumoren, en vroegen zich af of het ook deze immuunsbalans binnen colorectale tumoren kan beïnvloeden.
Een verborgen schakelaar die immuunsignalen regelt
Door patiënttumormonsters en grote kanker-databases te analyseren, vond het team dat colorectale tumoren met hoge RUNX1-niveaus vaak lage niveaus hadden van een oppervlaktemolecuul genaamd GITRL en juist hogere aantallen Tregs. GITRL zit op tumorcellen en andere cellen en kan binden aan een partnermolecuul, GITR, op T‑cellen. Wanneer GITRL GITR activeert, verzwakt dat doorgaans de Treg‑activiteit en versterkt het de functie van CD8+ T‑cellen, waardoor de balans naar anti‑tumor immuunsysteem kantelt. Experimenten in celkweken toonden dat het verlagen van RUNX1 GITRL verhoogde, terwijl het opvoeren van RUNX1 het verminderde, wat suggereert dat RUNX1 fungeert als een negatieve regulator van dit immuunstimulerende signaal.
Hoe het ene eiwit het andere blokkeert
De onderzoekers onderzochten vervolgens hoe RUNX1 GITRL‑niveaus verlaagt. In plaats van direct aan het GITRL-gen te binden, gaat RUNX1 fysiek een interactie aan met een ander eiwit genaamd STAT1, een bekende responder op de immuunboodschapper interferon‑gamma. Normaal gesproken, wanneer interferon‑gamma aanwezig is, vormt STAT1 paren, verplaatst het zich naar de kern en schakelt het genen zoals GITRL aan. De studie toont aan dat RUNX1 STAT1 bindt in het cytosol, de efficiënte dimerisatie van STAT1 verhindert en diens verplaatsing naar de kern vermindert. Hierdoor heeft STAT1 meer moeite om het GITRL‑gen aan te zetten, en tonen tumorcellen minder GITRL op hun oppervlak. Deze moleculaire blokkade bevordert uiteindelijk de ophoping van Tregs en verzwakt de activatie van CD8+ T‑cellen in de tumor‑microomgeving.
Van muismodellen naar therapeutisch potentieel
Om te zien hoe dit zich in levende organismen voordoet, gebruikte het team muizen met colorectale tumoren waarin RUNX1 of GITRL waren aangepast. Tumoren met veel GITRL groeiden langzamer, hadden minder Tregs en bevatten meer geactiveerde CD8+ T‑cellen. Daarentegen groeiden tumoren met extra RUNX1 sneller, huisvestten ze meer Tregs en waren er minder actieve cytotoxische T‑cellen. Belangrijk is dat wanneer deze RUNX1‑rijke tumoren werden behandeld met een experimenteel antilichaam dat GITR stimuleert—wat het effect van GITRL op T‑cellen nabootst—de tumoren veel gevoeliger werden voor de therapie en hun groei vertraagde. Dit suggereert dat wanneer RUNX1 de tumor‑cel GITRL onderdrukt, er juist meer GITR‑dragende Tregs aanwezig blijven die door het middel kunnen worden gericht en uitgeput.
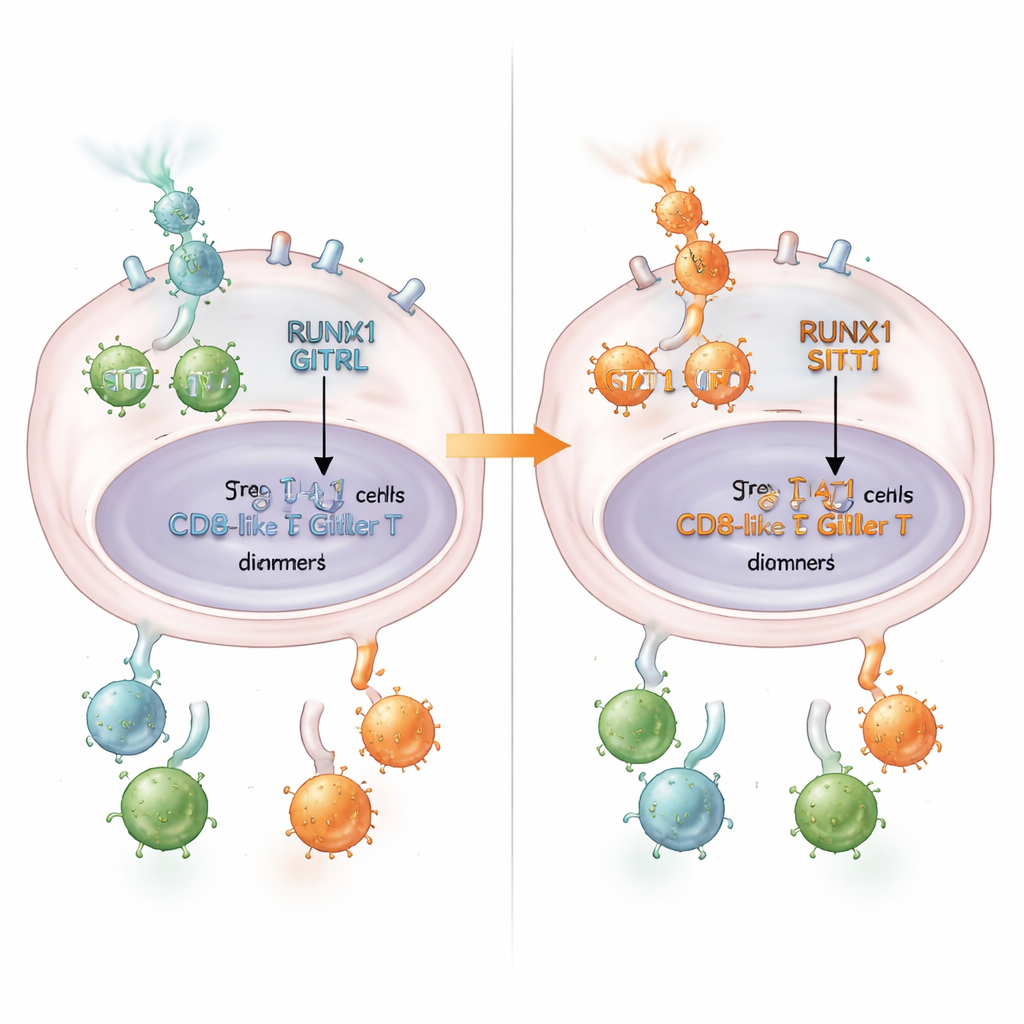
Wat dit betekent voor patiënten
In toegankelijke termen onthult dit werk een keten van gebeurtenissen waarin RUNX1 fungeert als poortwachter: het houdt STAT1 tegen, verlaagt GITRL, bevordert vredestichtende Tregs en dempt kankerbestrijdende CD8+ T‑cellen. Die keten helpt verklaren waarom sommige colorectale tumoren immuunsuppressiever zijn dan andere. De bevindingen suggereren dat het meten van RUNX1‑ en GITRL‑niveaus in tumoren kan helpen patiënten te identificeren die waarschijnlijk baat hebben bij middelen die GITR stimuleren. Op de lange termijn zouden therapieën die RUNX1’s greep op STAT1 verzwakken—or anderszins de RUNX1/STAT1/GITRL‑as herstellen—het immuunsysteem binnen colorectale tumoren kunnen heractiveren en het succes van immunotherapie kunnen verbeteren.
Bronvermelding: He, W., Zheng, L., Huang, W. et al. RUNX1 restrains STAT1-GITRL signaling to shape an immunosuppressive CRC microenvironment. Cell Death Discov. 12, 151 (2026). https://doi.org/10.1038/s41420-026-03053-7
Trefwoorden: dikkedarmkanker, tumormicro-omgeving, regulatorische T-cellen, GITR-immunotherapie, RUNX1 STAT1-signaalering