Clear Sky Science · sv
FUT8 omprogrammerar glykolytisk metabolism för att främja PKM2-laktylering och driva progression av klarcellig njurcancer
Varför njurcancerceller ändrar hur de förbränner socker
Klarcellig njurcancer är en av de vanligaste och mest dödliga formerna av njurcancer. Denna studie undersöker varför dessa tumörer är så beroende av socker och hur ett mindre känt enzym, FUT8, hjälper dem att växa, sprida sig och motstå behandling. Genom att följa hur socker bryts ner inne i cancerceller och hur restprodukterna kan omprogrammera proteiner avslöjar forskningen en ny sårbar punkt som framtida läkemedel kan rikta in sig på.
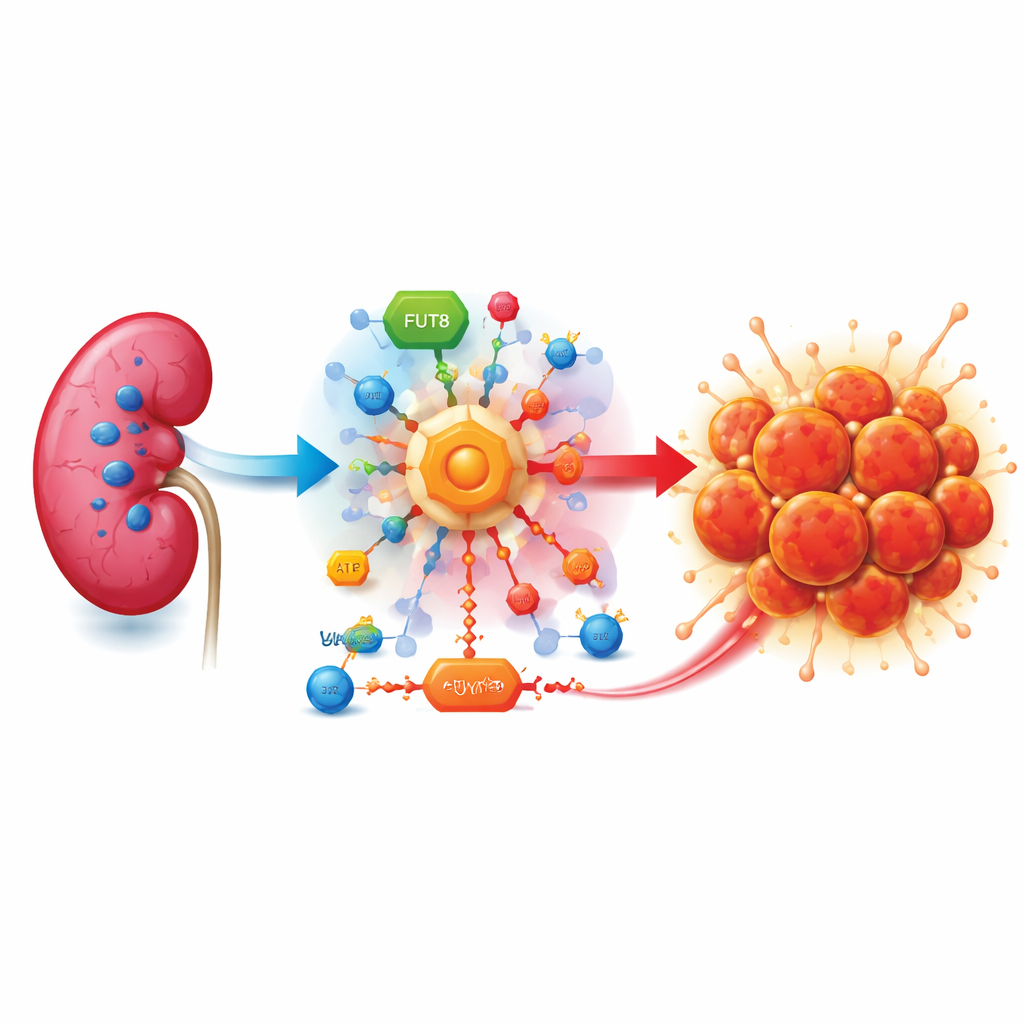
En sockerhungrig tumör
Klarcelligt njurcellscarcinom uppstår ofta när en skyddande gen kallad VHL förloras. Utan VHL beter sig cellerna som om de var syrebristiga, även när syre finns i överflöd. De slår på nödlägen som ökar sockernedbrytningen via en genväg känd som aerob glykolys. Istället för att utvinna energi fullt ut omvandlar cancerceller mycket av sockret till laktat, en sur biprodukt som byggs upp runt tumören och som hjälper den att växa, undkomma immunsystemet och sprida sig.
En förbisedd sockerdekoratör tar plats i rampljuset
Enzymet FUT8 tillsätter normalt en liten sockerrest, fukos, på många cellytproteiner och finjusterar hur celler svarar på tillväxtsignaler. Författarna visar att FUT8 i sig är starkt förhöjt i klarcelliga njurtumörer jämfört med normal njurvävnad. Patienter vars tumörer har högre FUT8 tenderar att ha kortare överlevnad, vilket gör FUT8 till en potentiell biomarkör. När FUT8 stängs av i njurcancerceller odlade i skålar eller i möss växer tumörerna långsammare, bildar färre kolonier, rör sig mindre och har en minskad förmåga att anlägga metastaser i lungorna. Markörer för ett mer invasivt, rörligt celltillstånd sjunker, vilket tyder på att FUT8 hjälper tumörer att anta ett formförändrande, spridande beteende.
Omkoppling av hur cancerceller använder bränsle
När forskarna gick djupare upptäckte de att FUT8 ökar aktiviteten hos HIF-1α, en huvudregulator av lågsyresvaret. Detta förstärker i sin tur glykolysen och försvagar cellens normala, syreberoende energiproduktion i mitokondrierna. När FUT8 tystas ned skiftar cellerna tillbaka mot effektivare mitokondriell respiration, deras försurning av omgivande medium minskar och laktatnivåerna inne i cellen sjunker. Att slå ner HIF-1α efterliknar dessa effekter, vilket indikerar att FUT8 driver ett ”Warburg-liknande” metabolt program till stor del genom denna hypoxiväg. Experiment där laktat tillsätts tillbaka till FUT8-defekta celler återställer delvis deras tillväxt och rörelse, vilket visar att laktat inte bara är avfall utan en aktiv drivkraft i maligniteten.
Från avfallsprodukt till proteinbrytpunkt
Studien frågar sedan vad laktat faktiskt gör inne i cellen. Utöver att försura omgivningen kan laktat fästa vid lysinrester på proteiner i en modifiering som kallas laktylering. Författarna upptäcker att FUT8:s inflytande på metabolismen höjer den globala laktyleringsnivån över många proteiner, och att hög FUT8 i patienttumörer går hand i hand med hög total laktylering. Genom en bred proteinkartläggning identifierar de ett nyckelmål: PKM2, ett centralt enzym i glykolysen. I klarcelliga njurcancerceller bär PKM2 en laktyleringsmarkör på en specifik position, K115, och denna märkning beror på FUT8 och laktatnivåer. När teamet konstruerar en version av PKM2 som inte kan laktyleras vid denna plats växer cancercellerna långsammare, migrerar mindre, producerar mindre syra och bildar mindre tumörer i möss. Denna icke-laktylerade PKM2 visar också ändrad aktivitet och lokalisation i cellen, vilket kopplar den kemiska märken direkt till enzymets funktion.
Parning av metabola och signaleringsmål
Slutligen testar forskarna om blockering av både laktatproduktion och FUT8 samtidigt kan dämpa tumörer mer effektivt. I musmodeller bromsar ett läkemedel som hämmar laktatbildande enzymer och en förening som blockerar FUT8 vardera tumörtillväxten på egen hand, men kombinationen fungerar bäst och minskar den övergripande nivån av laktylering i tumörproteiner. Dessa resultat tyder på att FUT8–HIF-1α–laktat–PKM2-kedjan bildar en kritisk ryggrad som kopplar förändrad metabolism till förändringar i proteinbeteende och cellidentitet i klarcellig njurcancer.
Vad detta betyder för patienter
För en lekman är budskapet att klarcelliga njurtumörer kapar både sockeranvändning och proteindekoration för att driva sin progression. FUT8 sitter i korsningen mellan dessa processer och hjälper cancerceller att överproducera laktat och sedan använda det laktatet för att slå om viktiga proteinswitchar som PKM2. Genom detta uppmuntras cellerna att växa snabbare och bli mer invasiva. Att rikta in sig på FUT8, laktatproduktionen eller den specifika laktyleringen av PKM2 kan erbjuda nya behandlingsstrategier och bidra till att förklara varför vissa patienter har sämre utfall än andra, även när deras tumörer delar samma initiala genetiska defekter.
Citering: Guo, Z., Jiang, H., Wang, X. et al. FUT8 reprograms glycolytic metabolism to promote PKM2 lactylation and drive clear cell renal cell carcinoma progression. Cell Death Discov. 12, 146 (2026). https://doi.org/10.1038/s41420-026-03013-1
Nyckelord: klarcellig njurcellscarcinom, tumörmetabolism, laktatsignalering, proteinalaktylering, FUT8