Clear Sky Science · fr
FUT8 reprogramme le métabolisme glycolytique pour promouvoir la lactylation de PKM2 et favoriser la progression du carcinome rénal à cellules claires
Pourquoi les cellules du rein cancéreuses modifient leur façon de brûler le sucre
Le carcinome rénal à cellules claires est l’une des formes de cancer du rein les plus fréquentes et les plus mortelles. Cette étude examine pourquoi ces tumeurs sont si dépendantes du sucre et comment une enzyme peu connue, FUT8, les aide à croître, à se propager et à résister aux traitements. En retraçant la façon dont le sucre est dégradé à l’intérieur des cellules tumorales et comment les déchets produits peuvent reprogrammer des protéines, les chercheurs mettent au jour une vulnérabilité nouvelle que de futurs médicaments pourraient cibler.
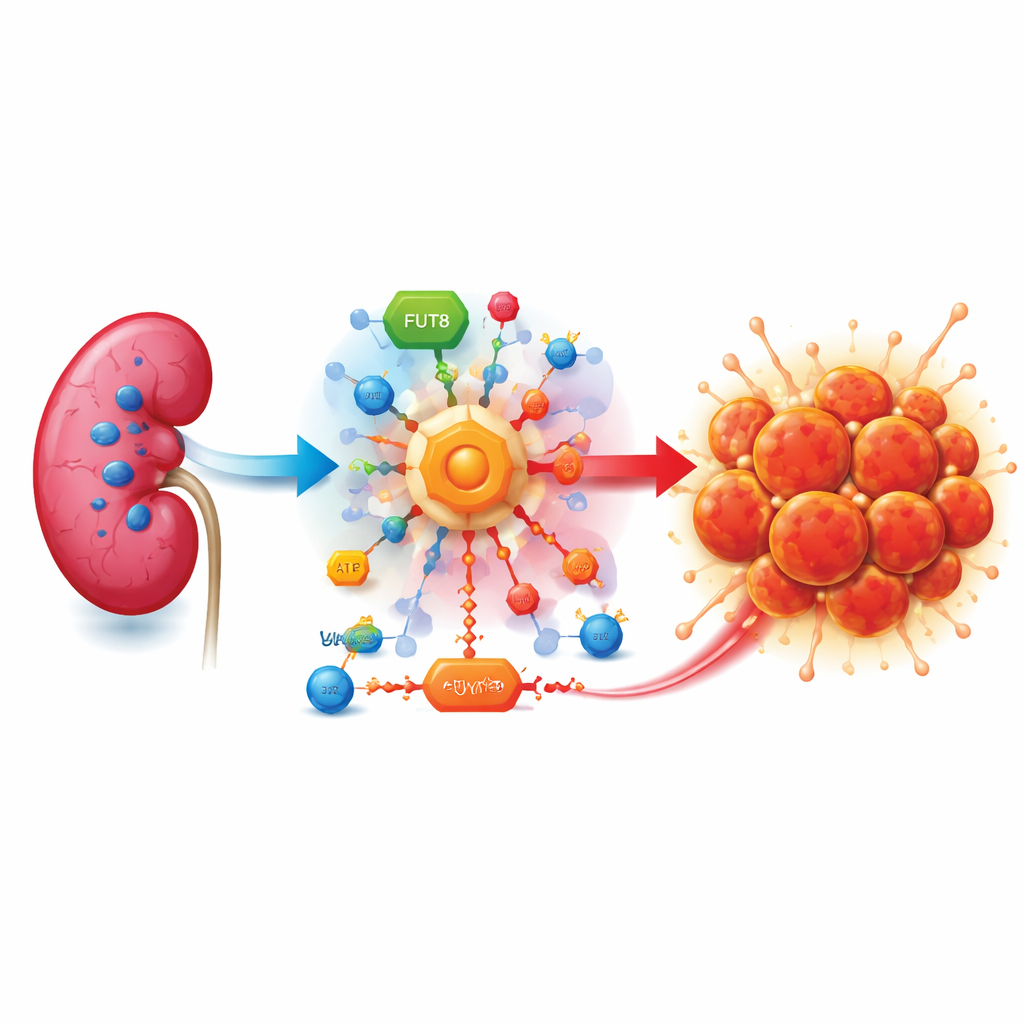
Une tumeur avide de sucre
Le carcinome rénal à cellules claires apparaît souvent quand un gène protecteur appelé VHL est perdu. Sans VHL, les cellules se comportent comme si elles manquaient d’oxygène, même lorsque l’oxygène est disponible. Elles activent des programmes d’urgence qui intensifient la combustion du sucre via une voie de contournement connue sous le nom de glycolyse aérobie. Plutôt que d’extraire pleinement l’énergie, les cellules cancéreuses convertissent une grande partie du sucre en lactate, un sous-produit acide qui s’accumule autour de la tumeur et favorise sa croissance, son évasion du système immunitaire et sa dissémination.
Un « décorateur » du sucre jusque-là négligé passe sous les projecteurs
L’enzyme FUT8 ajoute normalement une petite unité de sucre, la fucose, à de nombreuses protéines de surface cellulaire, modulant la façon dont les cellules répondent aux signaux de croissance. Les auteurs montrent que FUT8 est fortement surexprimé dans les tumeurs rénales à cellules claires par rapport au tissu rénal normal. Les patients dont les tumeurs présentent plus de FUT8 ont tendance à vivre moins longtemps, faisant de FUT8 un biomarqueur candidat. Lorsque FUT8 est désactivé dans des cellules de cancer du rein cultivées en laboratoire ou chez la souris, les tumeurs croissent plus lentement, forment moins de colonies, migrent moins et sont moins capables d’établir des métastases pulmonaires. Les marqueurs d’un état cellulaire plus invasif et mobile diminuent, ce qui suggère que FUT8 favorise l’adoption d’un comportement de type « transformation et diffusion » par les tumeurs.
Reconfigurer l’utilisation du carburant par les cellules cancéreuses
En creusant plus avant, les chercheurs découvrent que FUT8 augmente l’activité de HIF-1α, un régulateur majeur de la réponse à l’hypoxie. Cela renforce à son tour la glycolyse et affaiblit les centrales énergétiques habituelles de la cellule, les mitochondries, qui fonctionnent grâce à l’oxygène. Lorsque FUT8 est silencé, les cellules reviennent vers une respiration mitochondriale plus efficace, l’acidification du milieu environnant diminue et les niveaux de lactate intracellulaire chutent. L’inhibition de HIF-1α mime ces effets, indiquant que FUT8 pilote un programme métabolique de type « Warburg » en grande partie via cette voie hypoxique. Des expériences ajoutant du lactate à des cellules déficientes en FUT8 restaurent partiellement leur prolifération et leur mobilité, montrant que le lactate n’est pas qu’un déchet mais un moteur actif de la malignité.
Du déchet à l’interrupteur protéique
L’étude s’intéresse ensuite à ce que fait réellement le lactate à l’intérieur de la cellule. Au-delà de l’acidification du milieu, le lactate peut se lier aux résidus lysine des protéines via une modification appelée lactylation. Les auteurs constatent que l’influence de FUT8 sur le métabolisme augmente les niveaux globaux de lactylation sur de nombreuses protéines, et qu’un fort FUT8 dans les tumeurs de patients s’accompagne d’une forte lactylation globale. Grâce à une large analyse protéique, ils identifient une cible clé : PKM2, une enzyme centrale de la glycolyse. Dans les cellules de carcinome rénal à cellules claires, PKM2 porte une marque de lactylation à un site spécifique, K115, et cette marque dépend de FUT8 et des niveaux de lactate. Lorsque l’équipe conçoit une version de PKM2 qui ne peut pas être lactylée en ce point, les cellules cancéreuses proliferent plus lentement, migrent moins, produisent moins d’acide et forment des tumeurs plus petites chez la souris. Cette PKM2 non lactylée montre aussi une activité et une localisation intracellulaire altérées, reliant directement ce tag chimique au fonctionnement de l’enzyme.
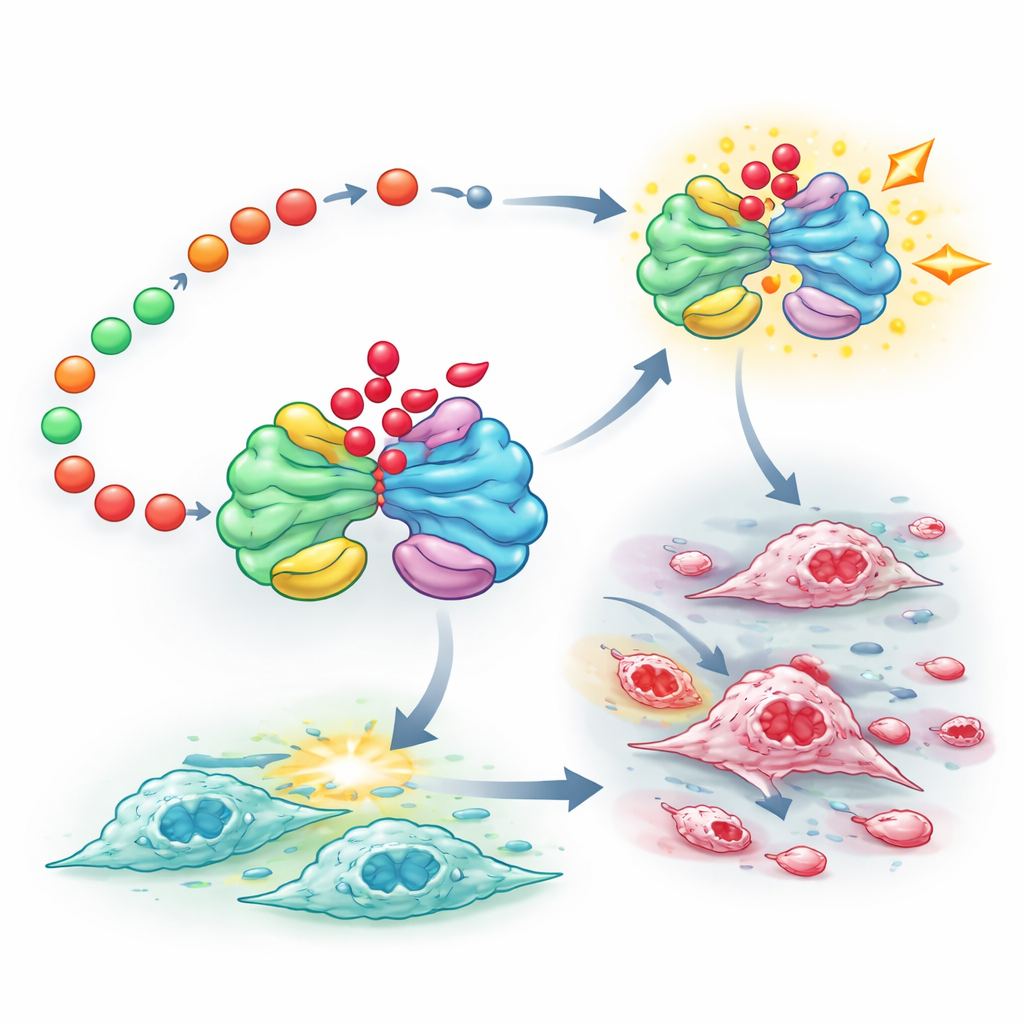
Associer cibles métaboliques et de signalisation
Enfin, les chercheurs testent si bloquer simultanément la production de lactate et FUT8 peut mieux contenir les tumeurs. Chez la souris, un médicament inhibant les enzymes formant le lactate et un composé bloquant FUT8 ralentissent chacun la croissance tumorale individuellement, mais la combinaison est la plus efficace et réduit le niveau global de lactylation des protéines tumorales. Ces résultats suggèrent que la chaîne FUT8–HIF-1α–lactate–PKM2 forme un axe critique reliant le métabolisme altéré aux changements du comportement protéique et de l’identité cellulaire dans le carcinome rénal à cellules claires.
Ce que cela signifie pour les patients
Pour un lecteur non spécialiste, le message est que les tumeurs rénales à cellules claires détournent à la fois l’utilisation du sucre et la « décoration » des protéines pour alimenter leur progression. FUT8 se trouve au carrefour de ces processus, aidant les cellules cancéreuses à surproduire du lactate puis à utiliser ce lactate pour activer des interrupteurs protéiques importants comme PKM2. Ce mécanisme encourage les cellules à croître plus vite et à devenir plus invasives. Cibler FUT8, la production de lactate ou la lactylation spécifique de PKM2 pourrait offrir de nouvelles stratégies thérapeutiques et aider à expliquer pourquoi certains patients ont un pronostic plus défavorable, même lorsque leurs tumeurs partagent les mêmes défauts génétiques initiaux.
Citation: Guo, Z., Jiang, H., Wang, X. et al. FUT8 reprograms glycolytic metabolism to promote PKM2 lactylation and drive clear cell renal cell carcinoma progression. Cell Death Discov. 12, 146 (2026). https://doi.org/10.1038/s41420-026-03013-1
Mots-clés: carcinome rénal à cellules claires, métabolisme tumoral, signalisation par le lactate, lactylation des protéines, FUT8