Clear Sky Science · pl
FUT8 przeprogramowuje metabolizm glikolityczny, promuje laktylację PKM2 i napędza postęp raka jasnokomórkowego nerki
Dlaczego komórki raka nerki zmieniają sposób, w jaki spalają cukier
Rak jasnokomórkowy nerki jest jedną z najczęstszych i najbardziej śmiertelnych postaci raka nerek. W tym badaniu zbadano, dlaczego te guzy są tak uzależnione od cukru oraz jak mniej znany enzym FUT8 pomaga im rosnąć, szerzyć się i opierać leczeniu. Śledząc, jak cukier jest rozkładany wewnątrz komórek nowotworowych i jak powstające produkty odpadowe mogą przeprogramowywać białka, badania ujawniają nowy słaby punkt, który przyszłe leki mogłyby zaatakować.
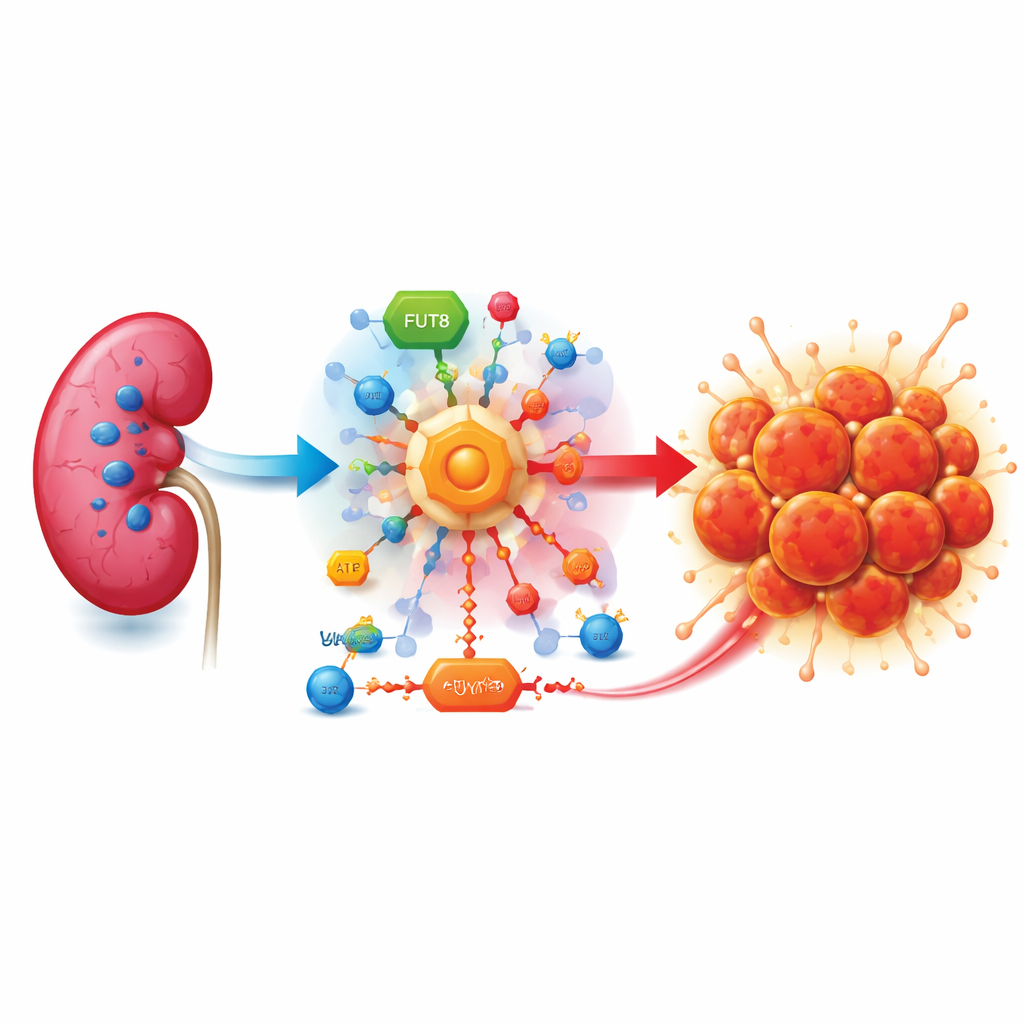
Guz głodny cukru
Rak jasnokomórkowy nerki często pojawia się w wyniku utraty genetycznego „strażnika” zwanego VHL. Bez VHL komórki zachowują się tak, jakby cierpiały na niedobór tlenu, nawet gdy tlenu jest pod dostatkiem. Włączają awaryjne programy, które zwiększają spalanie cukru poprzez skróconą ścieżkę znaną jako glikoliza tlenowa. Zamiast w pełni pozyskiwać energię, komórki nowotworowe przekształcają znaczną część cukru w mleczan, kwaśny produkt uboczny, który gromadzi się wokół guza i pomaga mu rosnąć, unikać układu odpornościowego oraz szerzyć się.
Niedoceniany dekorator cukrowy wchodzi na scenę
Enzym FUT8 zwykle dodaje małą cząsteczkę cukru, fukozę, do wielu białek na powierzchni komórek, modulując ich reakcje na sygnały wzrostu. Autorzy wykazują, że FUT8 jest wyraźnie podwyższony w guzach nerki jasnokomórkowej w porównaniu z prawidłową tkanką nerkową. Pacjenci, których guzy mają wyższe poziomy FUT8, mają tendencję do krótszego przeżycia, co wskazuje na FUT8 jako potencjalny biomarker. Gdy FUT8 jest wyłączany w komórkach raka nerki hodowanych na szalkach lub u myszy, guzy rosną wolniej, tworzą mniej kolonii, przemieszczają się mniej i mają mniejszą zdolność do zawiązywania przerzutów w płucach. Markery bardziej inwazyjnego, mobilnego stanu komórek spadają, sugerując, że FUT8 pomaga popychać guzy w kierunku zachowań sprzyjających rozprzestrzenianiu się.
Przełączenie sposobu wykorzystania paliwa przez komórki nowotworowe
Głębiej drążąc, badacze odkryli, że FUT8 wzmacnia aktywność HIF-1α, głównego regulatora odpowiedzi na niskie stężenie tlenu. To z kolei wzmacnia glikolizę i osłabia normalne, tlenowe „elektrownie” komórki — mitochondria. Gdy FUT8 jest wyciszony, komórki przełączają się z powrotem na bardziej wydajne oddychanie mitochondrialne, ich zakwaszanie otaczającego środowiska maleje, a poziomy mleczanu wewnątrz komórki spadają. Wyciszenie HIF-1α naśladuje te efekty, co wskazuje, że FUT8 napędza program metaboliczny podobny do efektu Warburga w dużej mierze przez tę ścieżkę hipoksji. Eksperymenty, w których do komórek pozbawionych FUT8 dodano mleczan, częściowo przywróciły ich wzrost i ruchliwość, pokazując, że mleczan nie jest jedynie odpadem, lecz aktywnym czynnikiem napędzającym złośliwość.
Od produktu odpadowego do przełącznika białkowego
Badanie następnie zadaje pytanie, co mleczan właściwie robi wewnątrz komórki. Poza zakwaszaniem środowiska, mleczan może przyłączać się do reszt lizyny w białkach w modyfikacji zwanej laktylacją. Autorzy stwierdzają, że wpływ FUT8 na metabolizm podnosi globalne poziomy laktylacji wielu białek, a wysoki FUT8 w guzach pacjentów idzie w parze z wysoką ogólną laktylacją. Przy użyciu szerokiego przeglądu białek identyfikują jeden kluczowy cel: PKM2, centralny enzym glikolizy. W komórkach raka jasnokomórkowego nerki PKM2 nosi znak laktylacji na konkretnym miejscu, K115, a ten znak zależy od FUT8 i poziomów mleczanu. Kiedy zespół zaprojektował wersję PKM2, która nie może być laktylowana w tym miejscu, komórki rakowe rosły wolniej, migrowały mniej, produkowały mniej kwasu i tworzyły mniejsze guzy u myszy. Ta nie-laktylowana PKM2 wykazywała także zmienioną aktywność i rozmieszczenie w komórce, łącząc chemiczny znacznik bezpośrednio z funkcją enzymu.
Łączenie celów metabolicznych i sygnałowych
Na koniec badacze sprawdzili, czy jednoczesne zablokowanie produkcji mleczanu i FUT8 może skuteczniej pohamować guzy. W modelach mysich lek hamujący enzymy tworzące mleczan oraz związek blokujący FUT8 każdy z osobna spowalniały wzrost guza, ale kombinacja działała najlepiej i zmniejszała ogólny poziom laktylacji białek guza. Wyniki te sugerują, że łańcuch FUT8–HIF-1α–mleczan–PKM2 tworzy krytyczne rusztowanie łączące zmieniony metabolizm z zmianami zachowania białek i tożsamości komórkowej w raku jasnokomórkowym nerki.
Co to oznacza dla pacjentów
Dla laika przekaz jest taki, że guzy jasnokomórkowe nerki zawłaszczają zarówno wykorzystanie cukru, jak i dekorowanie białek, aby napędzać swój postęp. FUT8 stoi na skrzyżowaniu tych procesów, pomagając komórkom nowotworowym nadprodukcję mleczanu, a następnie wykorzystywać ten mleczan do przełączania ważnych białek, takich jak PKM2. W ten sposób sprzyja szybszemu wzrostowi i zwiększonej inwazyjności komórek. Celowanie w FUT8, produkcję mleczanu lub specyficzną laktylację PKM2 może zaoferować nowe strategie leczenia i pomóc wyjaśnić, dlaczego niektórzy pacjenci mają gorsze rokowania niż inni, nawet gdy ich guzy mają te same początkowe defekty genetyczne.
Cytowanie: Guo, Z., Jiang, H., Wang, X. et al. FUT8 reprograms glycolytic metabolism to promote PKM2 lactylation and drive clear cell renal cell carcinoma progression. Cell Death Discov. 12, 146 (2026). https://doi.org/10.1038/s41420-026-03013-1
Słowa kluczowe: rak jasnokomórkowy nerki, metabolizm nowotworu, sygnalizacja przez mleczany, laktylacja białek, FUT8