Clear Sky Science · ar
FUT8 يعيد برمجة التمثيل الغذائي الجليكولي لترويج لاكتلة PKM2 ودفع تقدم سرطان الكلى ذو الخلايا الصافية
لماذا تغيّر خلايا سرطان الكلى طريقة تحرقها للسكر
سرطان الكلى ذو الخلايا الصافية هو أحد أكثر أنواع سرطان الكلى شيوعًا وخطورة. يستكشف هذا البحث سبب اعتماد هذه الأورام الشديد على السكر وكيف يساعد إنزيم أقل شهرة، FUT8، في نموها وانتشارها ومقاومتها للعلاج. من خلال تتبع كيفية تكسير السكر داخل الخلايا السرطانية وكيف يمكن للنواتج الثانوية أن تعيد برمجة البروتينات، تكشف الدراسة عن نقطة ضعف جديدة قد تستهدفها أدوية مستقبلية.
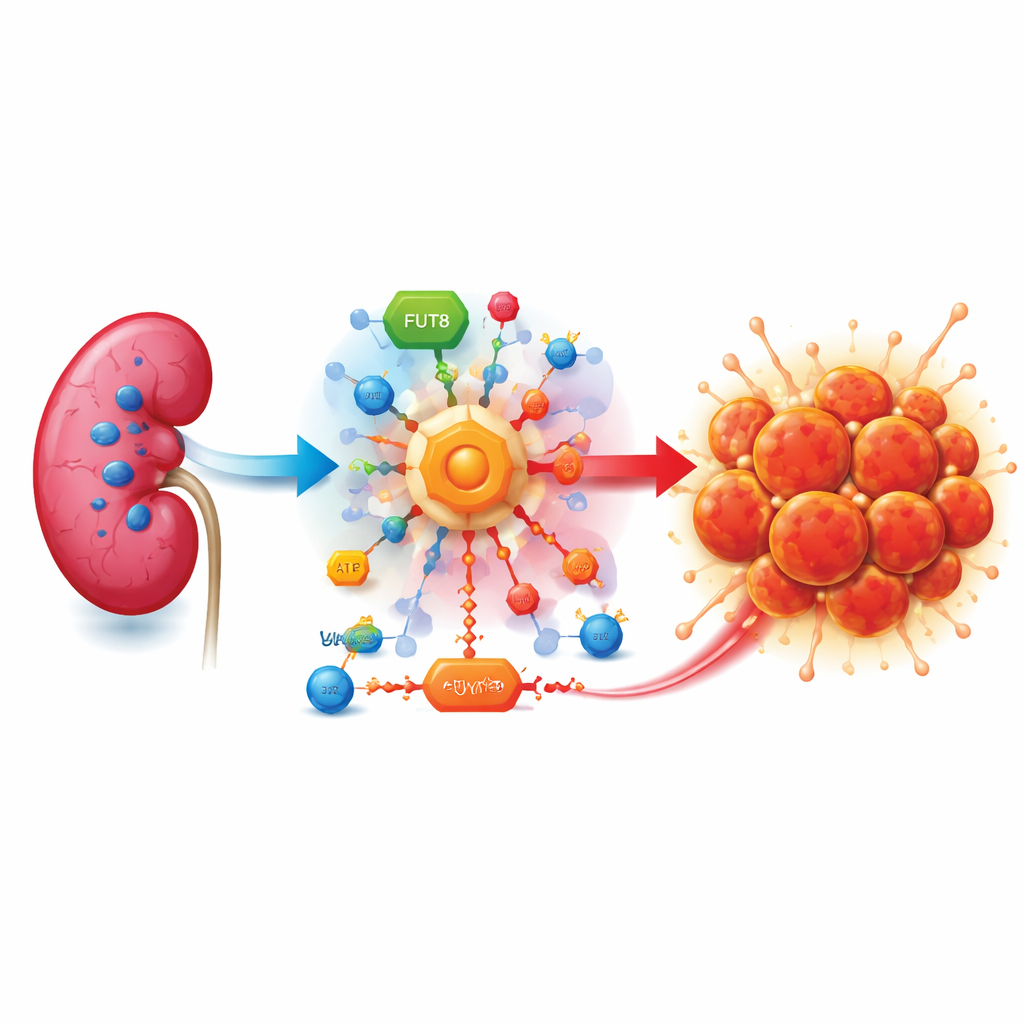
ورم جائع للسكر
غالبًا ما ينشأ سرطان الكلى ذو الخلايا الصافية حين يفقد جين حارس يُدعى VHL. من دون VHL، تتصرف الخلايا كما لو أنها محرومة من الأكسجين حتى عندما يتوفر الأكسجين بكثرة. تُشغّل برامج طوارئ تزيد من حرق السكر عبر مسار مختصر يُعرف بالجليكوليز الهوائي. بدلاً من استخلاص الطاقة بالكامل، تحوّل الخلايا السرطانية جزءًا كبيرًا من السكر إلى لاكتات، منتج ثانوي حمضي يتراكم حول الورم ويساعده على النمو وتفادي الجهاز المناعي والانتشار.
مُزيّن سُكري مُهمَل يلفت الأنظار
عادةً يضيف الإنزيم FUT8 سكرًا صغيرًا (فوكوز) إلى العديد من بروتينات سطح الخلية، ما يضبط كيفية استجابة الخلايا لإشارات النمو. يبين المؤلفون أن FUT8 مرتفع بقوة في أورام الكلى ذات الخلايا الصافية مقارنة بنسيج الكلى الطبيعي. المرضى الذين تحتوي أورامهم على مستويات أعلى من FUT8 يميلون إلى العيش لفترة أقصر، مما يضع FUT8 كعلامة حيوية محتملة. عند إيقاف FUT8 في خلايا سرطان الكلى المزروعة في الأطباق أو في الفئران، تنمو الأورام ببطء أكبر، تتكوّن مستعمرات أقل، تتحرك أقل، وتصبح أقل قدرة على زرع نقائل في الرئتين. تنخفض علامات الحالة الخلوية الأكثر غزوًا وحركية، مما يشير إلى أن FUT8 يساعد على دفع الأورام نحو سلوك متحوّل وشديد الانتشار.
إعادة توصيل كيفية استخدام الخلايا السرطانية للوقود
عند التعمق، اكتشف الباحثون أن FUT8 يزيد نشاط HIF-1α، المنظم الرئيسي لاستجابة نقص الأكسجين. وهذا بدوره يعزز الجليكوليز ويضعف مصانع الطاقة العادية المعتمدة على الأكسجين في الميتوكوندريا. عندما يُسكت FUT8، تعود الخلايا إلى التنفس الميتوكوندري الأكثر كفاءة، ينخفض تحمّض الوسط المحيط، وتنخفض مستويات اللاكتات داخل الخلية. تقلّد خفض HIF-1α هذه التأثيرات، مما يشير إلى أن FUT8 يقود برنامجًا أيضيًا شبيهًا بواربورغ إلى حد كبير عبر مسار نقص الأكسجين هذا. تجارب إضافة اللاكتات مرة أخرى إلى خلايا ناقصة FUT8 تستعيد جزئيًا نموها وحركتها، مبينة أن اللاكتات ليست مجرد نفاية بل هي محرّك نشط للخبيثة.
من منتج نفاية إلى مفتاح بروتيني
تسأل الدراسة بعد ذلك ما الذي تفعله اللاكتات داخل الخلية بالضبط. بخلاف تحميض البيئة، يمكن للاكتات أن تلتصق ببقايا الليسين على البروتينات في تعديل يُسمى اللاكتلة. يجد المؤلفون أن تأثير FUT8 على التمثيل الغذائي يرفع مستويات اللاكتلة العامة عبر العديد من البروتينات، وأن ارتفاع FUT8 في أورام المرضى يسير جنبًا إلى جنب مع ارتفاع اللاكتلة الكلي. باستخدام مسح واسع للبروتينات، يحددون هدفًا رئيسيًا: PKM2، إنزيم محوري في الجليكوليز. في خلايا سرطان الكلى ذات الخلايا الصافية، يحمل PKM2 علامة لاكتلة عند موقع محدد، K115، وتعتمد هذه العلامة على مستويات FUT8 واللاكتات. عندما يصمم الفريق نسخة من PKM2 لا يمكن لاكتلتها عند هذا الموقع، تنمو الخلايا السرطانية أبطأ، تهاجر أقل، تنتج حمضًا أقل، وتشكل أورامًا أصغر في الفئران. تُظهر هذه النسخة غير اللاكتلتة من PKM2 أيضًا نشاطًا وموقعًا داخل الخلية مختلفين، مما يربط الوسم الكيميائي مباشرة بكيفية عمل الإنزيم.
مزاوجة الأهداف الأيضية والإشارية
أخيرًا، يختبر الباحثون ما إذا كان حجب إنتاج اللاكتات وFUT8 في الوقت نفسه يمكن أن يكبح الأورام بشكل أكثر فعالية. في نماذج الفئران، يبطئ دواء يثبط إنزيمات تكوين اللاكتات ومركب يعيق FUT8 نمو الورم كلٌ منهما على حدة، لكن الجمع بينهما يعمل أفضل ويقلل المستوى العام للاكتلة في بروتينات الورم. تشير هذه النتائج إلى أن سلسلة FUT8–HIF-1α–اللاكتات–PKM2 تشكّل عمودًا فقريًا حاسمًا يربط التغيرات الأيضية بتعديلات سلوك البروتين وهوية الخلية في سرطان الكلى ذو الخلايا الصافية.
ما الذي يعنيه هذا للمرضى
للقارئ العادي، الرسالة هي أن أورام الكلى ذات الخلايا الصافية تستولي على كلٍ من استخدام السكر وتزيين البروتينات لتغذية تقدمها. يقع FUT8 عند مفترق هذين المسارين، حيث يساعد الخلايا السرطانية على إنتاج اللاكتات بكثرة ثم استخدام تلك اللاكتات لقلب مفاتيح بروتينية مهمة مثل PKM2. بفعل ذلك، يشجع الخلايا على النمو بسرعة أكبر وأن تصبح أكثر غزوًا. قد يوفر استهداف FUT8 أو إنتاج اللاكتات أو اللاكتلة المحددة لـPKM2 استراتيجيات علاجية جديدة ويساعد على تفسير سبب سوء حظ بعض المرضى مقارنة بآخرين، حتى عندما تشترك أورامهم في نفس العيوب الجينية الأولية.
الاستشهاد: Guo, Z., Jiang, H., Wang, X. et al. FUT8 reprograms glycolytic metabolism to promote PKM2 lactylation and drive clear cell renal cell carcinoma progression. Cell Death Discov. 12, 146 (2026). https://doi.org/10.1038/s41420-026-03013-1
الكلمات المفتاحية: سرطان الكلى ذو الخلايا الصافية, تمثيل الورم الغذائي, إشارات اللاكتات, لاكتلة البروتين, FUT8