Clear Sky Science · de
FUT8 programmiert den glykolytischen Stoffwechsel um, fördert PKM2-Lactylierung und treibt das Fortschreiten des klarzelligen Nierenzellkarzinoms voran
Warum Nierenkrebszellen ihre Zuckerverbrennung ändern
Das klarzellige Nierenzellkarzinom ist eine der häufigsten und tödlichsten Formen von Nierenkrebs. Diese Studie untersucht, warum diese Tumoren so stark auf Zucker angewiesen sind und wie ein wenig bekanntes Enzym, FUT8, ihr Wachstum, ihre Ausbreitung und ihre Therapie-Resistenz unterstützt. Indem sie nachverfolgt, wie Zucker in Krebszellen abgebaut wird und wie die entstehenden Abbauprodukte Proteine umprogrammieren können, zeigt die Forschung eine neue Schwachstelle, die künftige Medikamente angreifen könnten.
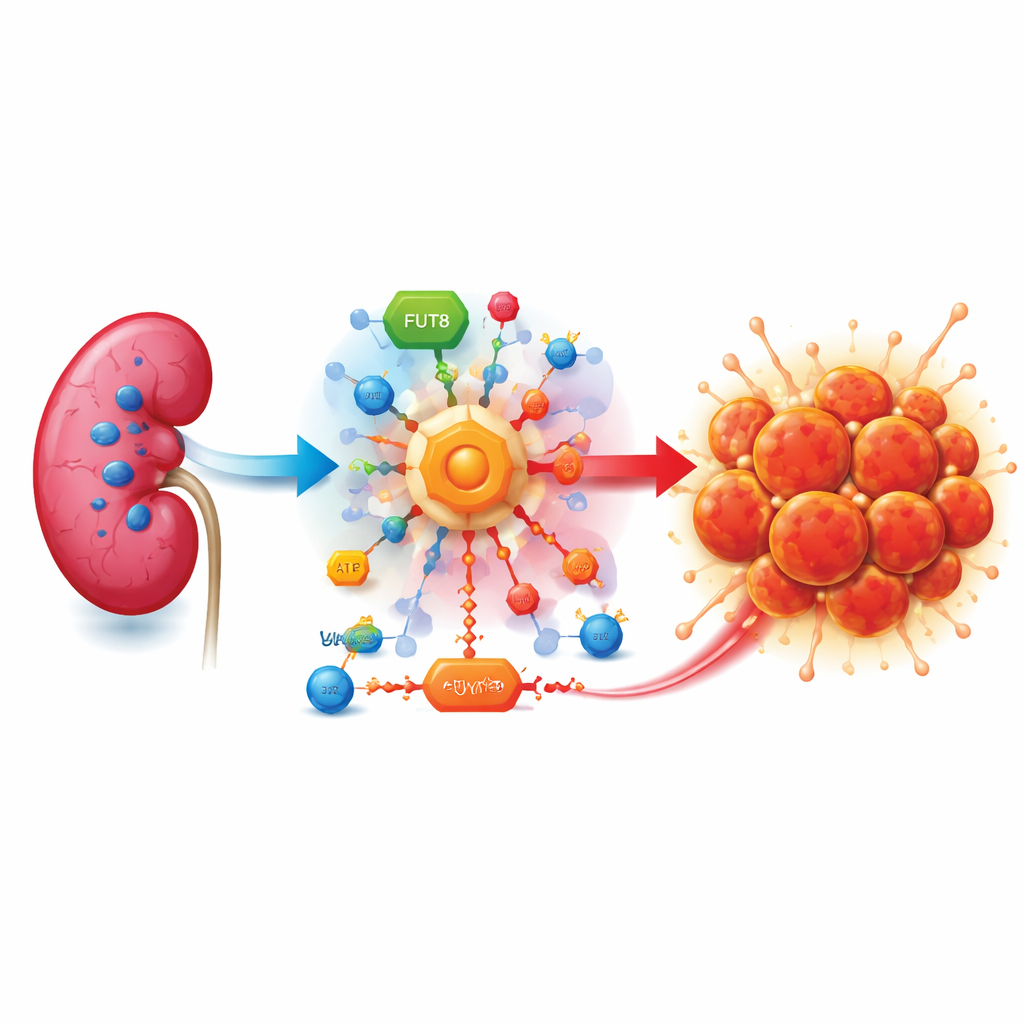
Ein zuckerhungriger Tumor
Das klarzellige Nierenzellkarzinom entsteht häufig, wenn ein Wächtergen namens VHL verloren geht. Ohne VHL verhalten sich Zellen so, als litten sie unter Sauerstoffmangel, selbst wenn ausreichend Sauerstoff vorhanden ist. Sie schalten Notprogramme ein, die die Zuckerverbrennung über einen Kurzschlussweg namens aerobe Glykolyse hochfahren. Anstatt Energie vollständig zu gewinnen, wandeln Krebszellen einen Großteil des Zuckers in Laktat um, ein saures Nebenprodukt, das sich um den Tumor anreichert und dessen Wachstum, Immunflucht und Ausbreitung fördert.
Ein übersehener Zucker-Decorator tritt ins Rampenlicht
Das Enzym FUT8 fügt gewöhnlich vielen Oberflächenproteinen eine kleine Zuckerstruktur, Fucose, hinzu und beeinflusst so, wie Zellen auf Wachstumssignale reagieren. Die Autoren zeigen, dass FUT8 in klarzelligen Nierentumoren deutlich erhöht ist im Vergleich zu normalem Nierengewebe. Patienten, deren Tumoren mehr FUT8 aufweisen, haben tendenziell eine kürzere Überlebenszeit, was FUT8 als möglichen Biomarker kennzeichnet. Wenn FUT8 in Nierenkrebszellen, die in der Kultur oder in Mäusen wachsen, ausgeschaltet wird, wachsen Tumoren langsamer, bilden weniger Kolonien, bewegen sich weniger und können seltener Metastasen in der Lunge bilden. Marker eines invasiveren, mobilen Zellzustands sinken, was darauf hindeutet, dass FUT8 Tumoren in Richtung eines formwandelnden, ausbreitungsfreudigen Verhaltens treibt.
Umschaltung, wie Krebszellen Treibstoff nutzen
Bei genauerer Untersuchung entdeckten die Forscher, dass FUT8 die Aktivität von HIF-1α steigert, einem zentralen Regulator der Reaktion auf niedrigen Sauerstoff. Dies verstärkt wiederum die Glykolyse und schwächt die normalen, sauerstoffabhängigen Energiefabriken der Zelle in den Mitochondrien. Wenn FUT8 stillgelegt wird, verlagern sich die Zellen zurück zu effizienterer mitochondrialer Atmung, die Versauerung des umgebenden Mediums nimmt ab und der Laktatspiegel in den Zellen sinkt. Die Herunterregulierung von HIF-1α ahmt diese Effekte nach, was darauf hinweist, dass FUT8 ein „Warburg-ähnliches“ Stoffwechselprogramm hauptsächlich über diesen Hypoxie-Weg antreibt. Experimente, die Laktat zu FUT8-defizienten Zellen hinzufügten, stellen teilweise deren Wachstum und Migration wieder her und zeigen, dass Laktat nicht nur Abfall, sondern ein aktiver Treiber der Malignität ist.
Vom Abfallprodukt zum Protein-Schalter
Die Studie fragt dann, was Laktat tatsächlich innerhalb der Zelle bewirkt. Über die Versauerung der Umgebung hinaus kann Laktat an Lysinreste von Proteinen angehängt werden, eine Modifikation, die Lactylierung genannt wird. Die Autoren finden, dass FUT8s Einfluss auf den Stoffwechsel die globalen Lactylierungsniveaus vieler Proteine erhöht und dass hohe FUT8-Werte in Patiententumoren mit hoher Gesamt-Lactylierung einhergehen. In einer breit angelegten Proteinanalyse identifizieren sie ein zentrales Ziel: PKM2, ein Schlüsselenzym der Glykolyse. In klarzelligen Nierenkrebszellen trägt PKM2 eine Lactylierung an einer spezifischen Position, K115, und diese Markierung hängt von FUT8 und den Laktatspiegeln ab. Wenn das Team eine Version von PKM2 erzeugt, die an dieser Stelle nicht lactyliert werden kann, wachsen Krebszellen langsamer, wandern weniger, produzieren weniger Säure und bilden in Mäusen kleinere Tumoren. Dieses nicht-lactylierte PKM2 zeigt auch veränderte Aktivität und zelluläre Lokalisation, was den chemischen Marker direkt mit der Funktion des Enzyms verbindet.
Metabolische und Signalziele koppeln
Schließlich prüfen die Forscher, ob das gleichzeitige Blockieren von Laktatproduktion und FUT8 Tumoren wirksamer eindämmen kann. In Mausmodellen verlangsamen sowohl ein Wirkstoff, der Laktat-bildende Enzyme hemmt, als auch eine Verbindung, die FUT8 blockiert, jeweils das Tumorwachstum, doch die Kombination wirkt am besten und reduziert das allgemeine Niveau der Lactylierung in Tumorproteinen. Diese Ergebnisse deuten darauf hin, dass die FUT8–HIF-1α–Laktat–PKM2-Kette ein kritisches Rückgrat bildet, das veränderten Stoffwechsel mit Änderungen im Proteingehalt und der Zellidentität im klarzelligen Nierenkrebs verbindet.
Was das für Patienten bedeutet
Für Laien lautet die Botschaft, dass klarzellige Nierentumoren sowohl den Zuckerstoffwechsel als auch die Proteinmodifikation kapern, um ihr Fortschreiten zu befeuern. FUT8 steht im Schnittpunkt dieser Prozesse, indem es Krebszellen hilft, zu viel Laktat zu produzieren und dieses Laktat dann zu nutzen, um wichtige Proteinschalter wie PKM2 umzulegen. Dadurch werden Zellen zu schnellerem Wachstum und stärkerer Invasivität angeregt. Das Anvisieren von FUT8, der Laktatproduktion oder der spezifischen Lactylierung von PKM2 könnte neue Behandlungsstrategien eröffnen und erklären, warum manche Patienten schlechtere Verläufe haben als andere, selbst wenn ihre Tumoren dieselben anfänglichen genetischen Defekte teilen.
Zitation: Guo, Z., Jiang, H., Wang, X. et al. FUT8 reprograms glycolytic metabolism to promote PKM2 lactylation and drive clear cell renal cell carcinoma progression. Cell Death Discov. 12, 146 (2026). https://doi.org/10.1038/s41420-026-03013-1
Schlüsselwörter: klarzelliges Nierenzellkarzinom, Tumorstoffwechsel, Laktat-Signalgebung, Protein-Lactylierung, FUT8