Clear Sky Science · ru
FUT8 перепрограммирует гликолитический метаболизм, усиливает лактиляцию PKM2 и способствует прогрессированию почечно-клеточного рака прозрачноклеточного типа
Почему клетки рака почки меняют способ утилизации сахара
Прозрачноклеточный рак почки — один из самых распространённых и смертоносных типов рака почки. В этом исследовании изучают, почему эти опухоли так зависят от сахара и как малоизвестный фермент FUT8 помогает им расти, распространяться и сопротивляться лечению. Отслеживая, как в раковых клетках расщепляется сахар и как образующиеся побочные продукты перепрограммируют белки, исследование выявляет новую уязвимость, на которую потенциально можно нацелить будущие препараты.
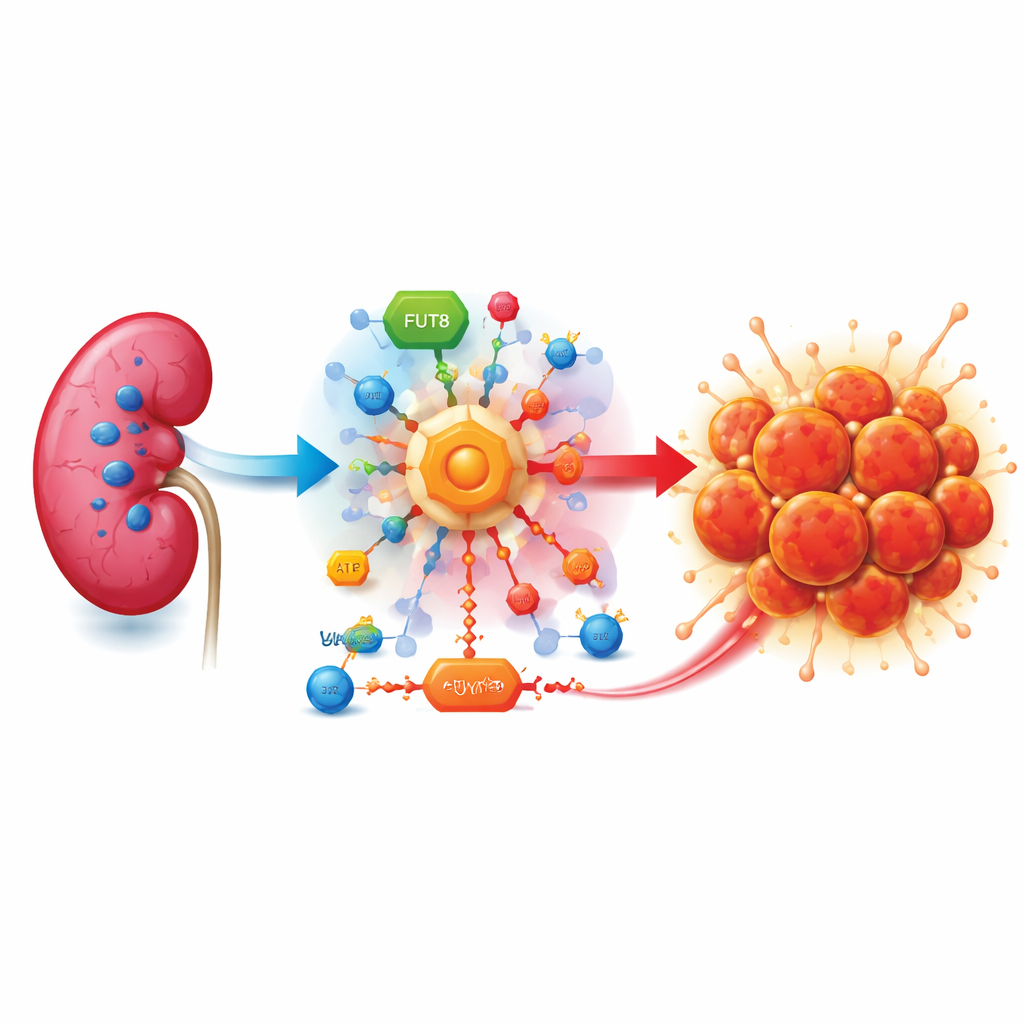
Опухоль, жаждущая сахара
Прозрачноклеточный почечно-клеточный рак часто развивается при утрате гена-хранителя VHL. Без VHL клетки ведут себя так, будто испытывают недостаток кислорода, даже при его избытке. Они включают аварийные программы, которые усиливают расщепление сахара через упрощённый путь, известный как аэробный гликолиз. Вместо полного извлечения энергии раковые клетки превращают большую часть сахара в лактат — кислый побочный продукт, который накапливается вокруг опухоли и помогает ей расти, ускользать от иммунной системы и метастазировать.
Незаметный «декоратор» сахара выходит на свет
Фермент FUT8 обычно добавляет к многим белкам на поверхности клетки небольшую сахарную единицу — фукозу, — регулируя реакцию клеток на сигналы роста. Авторы показывают, что уровень FUT8 значительно повышен в прозрачноклеточных опухолях почки по сравнению с нормальной почечной тканью. У пациентов с более высоким уровнем FUT8 выживаемость, как правило, ниже, что делает FUT8 кандидатом в биомаркеры. При выключении FUT8 в клетках рака почки в культуре или у мышей опухоли растут медленнее, образуют меньше колоний, меньше мигрируют и хуже поселяются в лёгких при метастазировании. Маркёры более инвазивного и подвижного состояния клетки снижаются, что указывает на роль FUT8 в продвижении опухолей к пластичной, расселяющейся форме.
Перепрограммирование использования топлива в раковых клетках
При дальнейшем изучении исследователи обнаружили, что FUT8 усиливает активность HIF-1α — ключевого регулятора ответа на низкий уровень кислорода. Это, в свою очередь, усиливает гликолиз и ослабляет нормальные кислород-зависимые энергетические процессы в митохондриях. При подавлении FUT8 клетки возвращаются к более эффективному митохондриальному дыханию, снижается закисление окружающей среды, и внутриклеточный уровень лактата падает. Подавление HIF-1α воспроизводит эти эффекты, что указывает на то, что FUT8 индуцирует «варбургоподобную» метаболическую программу во многом через этот гипоксический путь. Эксперименты с добавлением лактата в клетки, лишённые FUT8, частично восстанавливают их рост и подвижность, показывая, что лактат — не просто отход, а активный драйвер злокачественности.
От отхода к переключателю белков
Далее исследование задаётся вопросом, что именно делает лактат внутри клетки. Помимо подкисления среды, лактат может присоединяться к остаткам лизина в белках в модификации, называемой лактиляцией. Авторы обнаруживают, что влияние FUT8 на метаболизм повышает глобальные уровни лактиляции во многих белках, и что высокий FUT8 в опухолях пациентов кореллирует с высокой общей лактиляцией. С помощью широкого протеинного анализа они выделяют ключевую мишень: PKM2, центральный фермент гликолиза. В клетках прозрачноклеточного рака почки PKM2 несёт метку лактиляции в специфической позиции K115, и наличие этой метки зависит от FUT8 и уровней лактата. Когда команда создаёт версию PKM2, не способную к лактиляции в этом месте, раковые клетки растут медленнее, реже мигрируют, меньше подкисляют среду и образуют меньшие опухоли у мышей. Такая нелактелированная PKM2 также демонстрирует изменённую активность и распределение в пределах клетки, что напрямую связывает химическую метку с функцией фермента.
Сочетание метаболических и сигнальных мишеней
Наконец, исследователи проверяют, не эффективнее ли одновременно блокировать образование лактата и FUT8. В моделях на мышах препарат, ингибирующий ферменты, формирующие лактат, и соединение, блокирующее FUT8, каждый по отдельности замедляли рост опухолей, но сочетание давало наилучший эффект и снижало общий уровень лактиляции в белках опухолей. Эти результаты предполагают, что цепочка FUT8–HIF-1α–лактат–PKM2 образует критический каркас, связывающий изменённый метаболизм с изменениями в поведении белков и идентичности клеток при прозрачноклеточном раке почки.
Что это значит для пациентов
Проще говоря, прозрачноклеточные опухоли почки присваивают себе и способы использования сахара, и механизмы «украшения» белков, чтобы подпитывать своё прогрессирование. FUT8 стоит на перекрёстке этих процессов, помогая клеткам перепроизводить лактат и затем использовать этот лактат для переключения важных белков, таких как PKM2. За счёт этого он стимулирует более быстрый рост и повышенную инвазивность клеток. Нацеливание на FUT8, образование лактата или на специфическую лактиляцию PKM2 может предложить новые стратегии лечения и помочь объяснить, почему некоторые пациенты переносят болезнь хуже других, даже при одинаковых исходных генетических дефектах опухоли.
Цитирование: Guo, Z., Jiang, H., Wang, X. et al. FUT8 reprograms glycolytic metabolism to promote PKM2 lactylation and drive clear cell renal cell carcinoma progression. Cell Death Discov. 12, 146 (2026). https://doi.org/10.1038/s41420-026-03013-1
Ключевые слова: прозрачноклеточный почечно-клеточный рак, метаболизм опухоли, лактатная сигнализация, лактиляция белков, FUT8