Clear Sky Science · nl
FUT8 herprogrammeert glycolytisch metabolisme om PKM2-lactylatie te bevorderen en de progressie van clear cell niercelcarcinoom aan te jagen
Waarom nierkankercellen veranderen hoe ze suiker verbranden
Clear cell nierkanker is een van de meest voorkomende en dodelijke vormen van nierkanker. Deze studie onderzoekt waarom deze tumoren zo verslaafd zijn aan suiker en hoe een minder bekende enzym, FUT8, hen helpt te groeien, uit te zaaien en behandelingen te weerstaan. Door na te gaan hoe suiker in kankercellen wordt afgebroken en hoe de resulterende afvalproducten eiwitten kunnen herprogrammeren, onthult het onderzoek een nieuw zwak punt dat toekomstige medicijnen mogelijk kunnen aanboren.
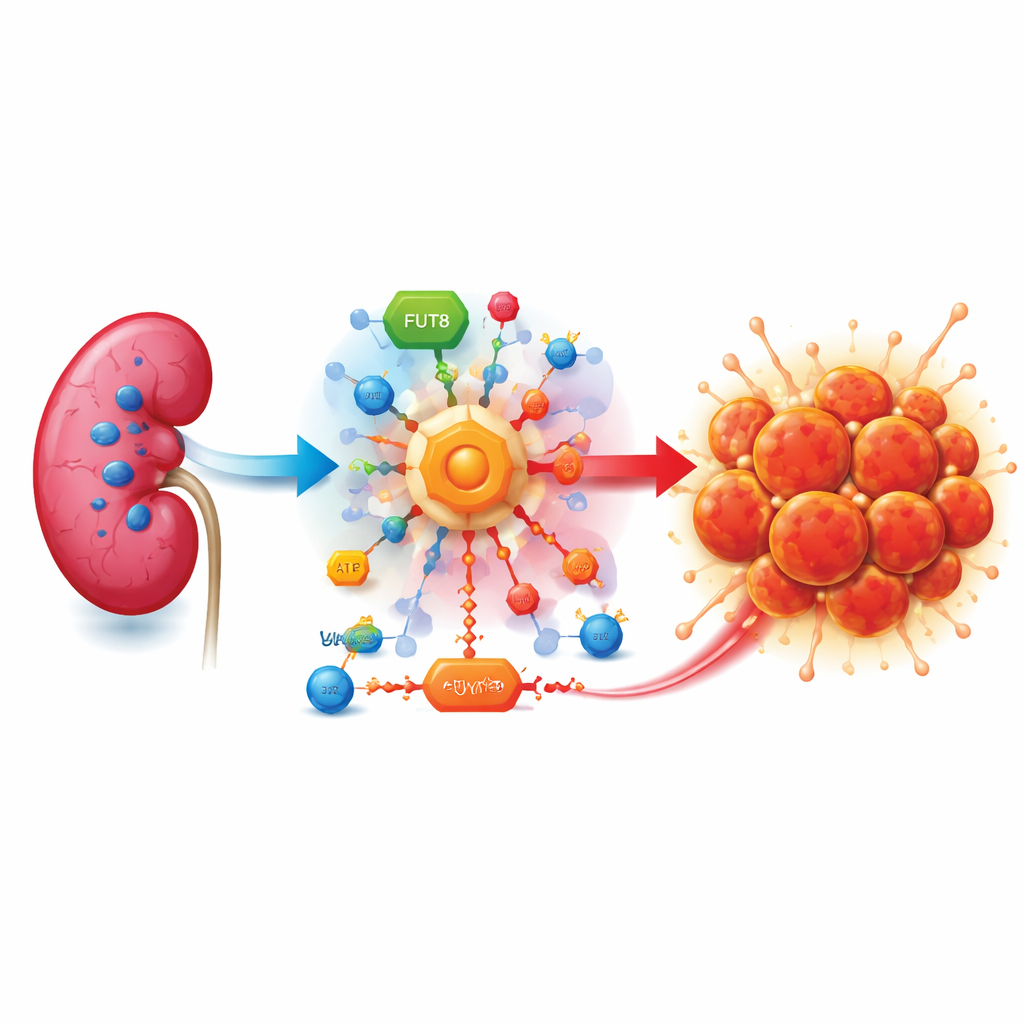
Een suikerhongerende tumor
Clear cell niercelcarcinoom ontstaat vaak wanneer een bewakersgen genaamd VHL verloren gaat. Zonder VHL gedragen cellen zich alsof ze zuurstoftekort hebben, zelfs wanneer er voldoende zuurstof aanwezig is. Ze schakelen noodprogramma's in die de suikerverbranding opvoeren via een versnelde route die bekendstaat als aerobe glycolyse. In plaats van energie volledig te winnen, zetten kankercellen veel van de suiker om in lactaat, een zuur bijproduct dat zich rond de tumor ophoopt en de groei, het ontwijken van het immuunsysteem en de verspreiding bevordert.
Een over het hoofd gezien suikerdecorator treedt op de voorgrond
Het enzym FUT8 voegt normaal gesproken een klein suikerderivaat, fucose, toe aan veel celoppervlakte-eiwitten, waarmee het de manier waarop cellen reageren op groeisignalen finetunet. De auteurs tonen aan dat FUT8 zelf sterk verhoogd is in clear cell-nier tumoren vergeleken met normaal nierweefsel. Patiënten waarvan de tumoren meer FUT8 bevatten, hebben doorgaans een kortere overleving, waardoor FUT8 een kandidaat-biomarker wordt. Wanneer FUT8 wordt uitgeschakeld in nierkankercellen gekweekt in schaaltjes of in muizen, groeien tumoren langzamer, vormen ze minder kolonies, bewegen ze minder en zijn ze minder goed in staat om metastasen in de longen te zaaien. Merkers van een meer invasieve, mobiele cellulaire staat nemen af, wat suggereert dat FUT8 tumoren helpt naar een vormveranderend, verspreidend gedrag te duwen.
Het herbedraden van hoe kankercellen brandstof gebruiken
Dieper gravend ontdekten de onderzoekers dat FUT8 de activiteit van HIF-1α versterkt, een hoofdregelaar van de reactie op laag zuurstofgehalte. Dit versterkt op zijn beurt de glycolyse en verzwakt de normale, zuurstofafhankelijke energiecentrales van de cel in de mitochondriën. Wanneer FUT8 wordt uitgeschakeld, schakelen cellen terug naar efficiëntere mitochondriale respiratie, daalt de verzuring van het omliggende medium en nemen de lactaatniveaus binnenin de cel af. Het onderdrukken van HIF-1α imiteert deze effecten, wat aangeeft dat FUT8 een “Warburg-achtig” metabool programma grotendeels via deze hypoxie-route aandrijft. Experimenten waarbij lactaat wordt toegevoegd aan FUT8-deficiënte cellen herstellen gedeeltelijk hun groei en beweging, wat aantoont dat lactaat niet alleen afval is maar een actieve aanjager van maligniteit.
Van afvalproduct naar eiwitschakelaar
De studie onderzoekt vervolgens wat lactaat eigenlijk binnen de cel doet. Naast het zuurder maken van de omgeving, kan lactaat zich aan lysineresiduen op eiwitten hechten in een modificatie die lactylatie wordt genoemd. De auteurs vinden dat de invloed van FUT8 op het metabolisme de globale lactylatieniveaus over veel eiwitten verhoogt, en dat hoge FUT8 in patiënstumoren gepaard gaat met hoge algemene lactylatie. Met behulp van een brede eiwitsurveillantie identificeren ze één sleuteltarget: PKM2, een centraal enzym in de glycolyse. In clear cell nierkankercellen draagt PKM2 een lactylatiekenmerk op een specifieke positie, K115, en dit kenmerk is afhankelijk van FUT8 en lactaatniveaus. Wanneer het team een versie van PKM2 maakt die op deze plek niet gelactyleerd kan worden, groeien kankercellen langzamer, migreren minder, produceren minder zuur en vormen ze kleinere tumoren in muizen. Deze niet-gelactyleerde PKM2 vertoont ook gewijzigde activiteit en locatie binnen de cel, waarmee het chemische label direct gekoppeld wordt aan hoe het enzym functioneert.
Combineren van metabole en signaaltargets
Ten slotte testen de onderzoekers of het gelijktijdig blokkeren van zowel lactaatproductie als FUT8 tumoren effectiever kan beteugelen. In muismodellen remt een geneesmiddel dat lactaatvormende enzymen blokkeert en een verbinding die FUT8 remt elk op zichzelf de tumor groei, maar de combinatie werkt het beste en vermindert het algemene niveau van lactylatie in tumoreiwitten. Deze resultaten suggereren dat de FUT8–HIF-1α–lactaat–PKM2-keten een cruciale ruggengraat vormt die veranderde metabolisme koppelt aan veranderingen in eiwitgedrag en celidentiteit in clear cell niercelcarcinoom.
Wat dit betekent voor patiënten
Voor een niet-specialist is de boodschap dat clear cell-nier tumoren zowel het suikergebruik als de eiwitdecoratie kapen om hun progressie te voeden. FUT8 ligt op het kruispunt van deze processen en helpt kankercellen om te veel lactaat te produceren en dat lactaat vervolgens te gebruiken om belangrijke eiwitschakelaars zoals PKM2 om te zetten. Daarmee stimuleert het cellen om sneller te groeien en invasiever te worden. Het richten op FUT8, de lactaatproductie of de specifieke lactylatie van PKM2 zou nieuwe behandelingsstrategieën kunnen bieden en helpen verklaren waarom sommige patiënten slechter af zijn dan anderen, zelfs wanneer hun tumoren dezelfde initiële genetische defecten delen.
Bronvermelding: Guo, Z., Jiang, H., Wang, X. et al. FUT8 reprograms glycolytic metabolism to promote PKM2 lactylation and drive clear cell renal cell carcinoma progression. Cell Death Discov. 12, 146 (2026). https://doi.org/10.1038/s41420-026-03013-1
Trefwoorden: clear cell niercelcarcinoom, tumormetabolisme, lactaatsignaalgeving, proteïnelactylatie, FUT8