Clear Sky Science · sv
Förklarbar prediktion av läkemedelsbiverkningar i centrala nervsystemet via biologiskt informerat grafneuralt nätverk
Varför dolda läkemedelsrisker spelar roll
Många läkemedel som hjälper vår hjärna kan också i tysthet skada den. Yrsel, förvirring, kramper eller depression kan dyka upp först efter att ett läkemedel använts brett. Traditionella laboratorie- och kliniska tester är för långsamma och kostsamma för att fånga alla möjliga problem före godkännande, särskilt för centrala nervsystemet där biverkningar kan vara subtila men livsavgörande. Denna studie presenterar en ny datormodell som läser över stora biologiska dataset för att tidigt flagga sannolika hjärnrelaterade biverkningar och för att visa den kedja av molekylära händelser som kan orsaka dem.
Att koppla ihop läkemedel och symtom
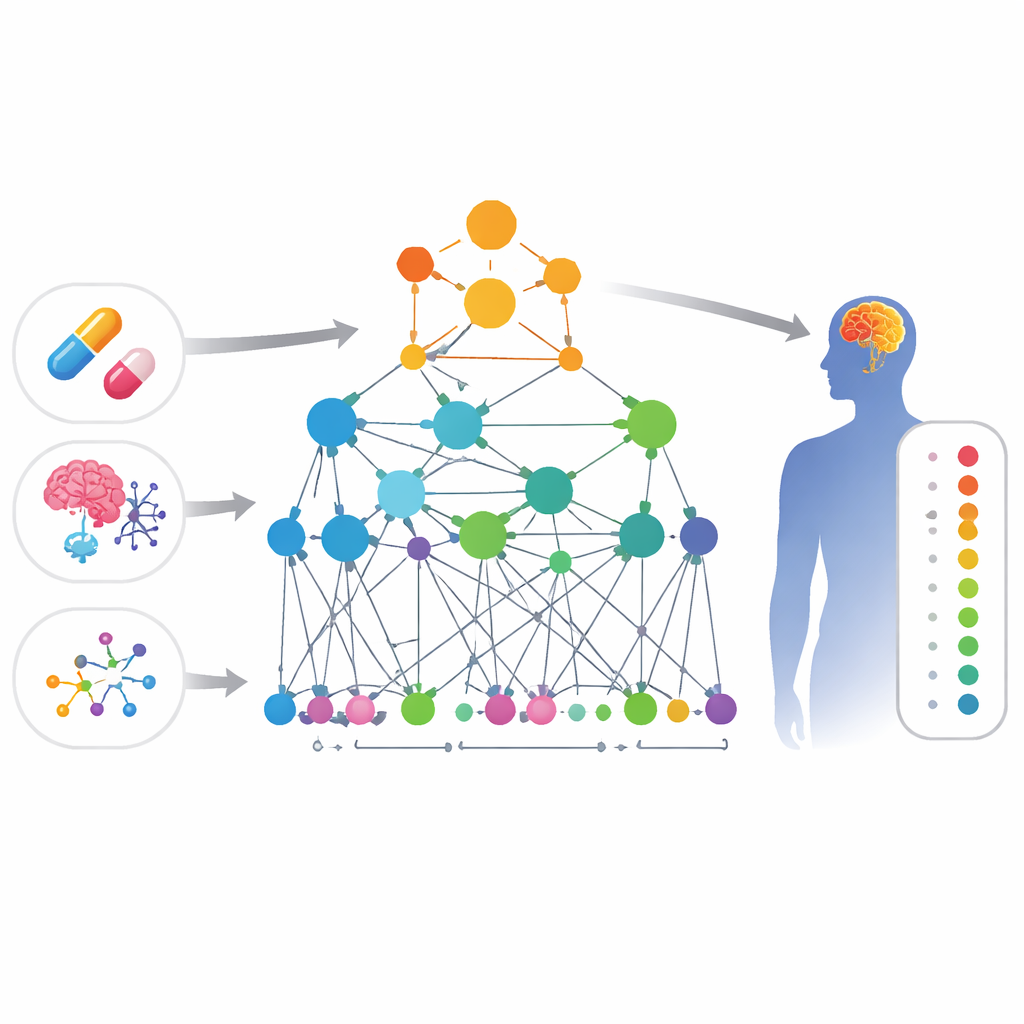
Forskarna byggde en stor "karta" av biologisk kunskap som länkar fyra typer av entiteter: läkemedel, biverkningar, gener och genfunktioner. I denna karta är varje objekt en punkt, och linjer mellan punkter representerar bevis för att de är relaterade — till exempel två gener som fysiskt interagerar, två läkemedel med liknande kemisk struktur eller ett läkemedel som är känt för att orsaka en viss biverkning. Eftersom klagomål relaterade till centrala nervsystemet både är vanliga och ofta förbises, fokuserade teamet kartan på hjärnrelaterade problem som stämningsförändringar, rörelsestörningar och andra neurologiska symtom.
Ett smart nätverk som lär biologi
På denna karta designade författarna en specialiserad form av artificiell intelligens kallad ett grafneuralt nätverk. Till skillnad från en standardmodell som ser varje läkemedel isolerat, betraktar detta tillvägagångssätt nätet av samband runt varje läkemedel och biverkning. Modellen, kallad HHAN-DSI, är "biologiskt informerad": den får endast föra vidare information längs vägar som biologiskt sett är meningsfulla — till exempel från en gen till en annan den direkt interagerar med, från en gen till ett läkemedel som riktar sig mot den, och sedan från det läkemedlet till biverkningar som setts med liknande läkemedel. Genom att ge större vikt åt de mest informativa vägarna lär sig systemet kompakta matematiska fingeravtryck för varje läkemedel och varje biverkning, och poängsätter sedan hur sannolikt varje par är att vara kopplade.
Att sätta modellen på prov
För att se om dessa prediktioner stämmer med verkligheten tränade teamet modellen på en kurerad databas över biverkningar rapporterade i officiell produktinformation och testade den sedan mot både denna källa och en separat uppsättning post-marknadsföringsrapporter om säkerhet. Dessa externa rapporter fångar problem som framkom först efter att läkemedel var i bred användning. Modellen skiljde inte bara verkliga läkemedels–biverkningspar från falska, utan rankade, viktigast av allt, de mest oroande effekterna högt på sina listor. Den överträffade flera befintliga maskininlärningsmetoder i denna rankningsuppgift, särskilt när data var glesa, som typiskt är fallet för nya läkemedel. I många fall där modellen verkade "fel" eftersom en förutsagd biverkning saknades i den kurerade databasen, återfanns samma läkemedels–symtomlänk i de verkliga säkerhetsrapporterna, vilket tyder på att modellen upptäckt förbisedda risker.
Att kika in i svart lådan
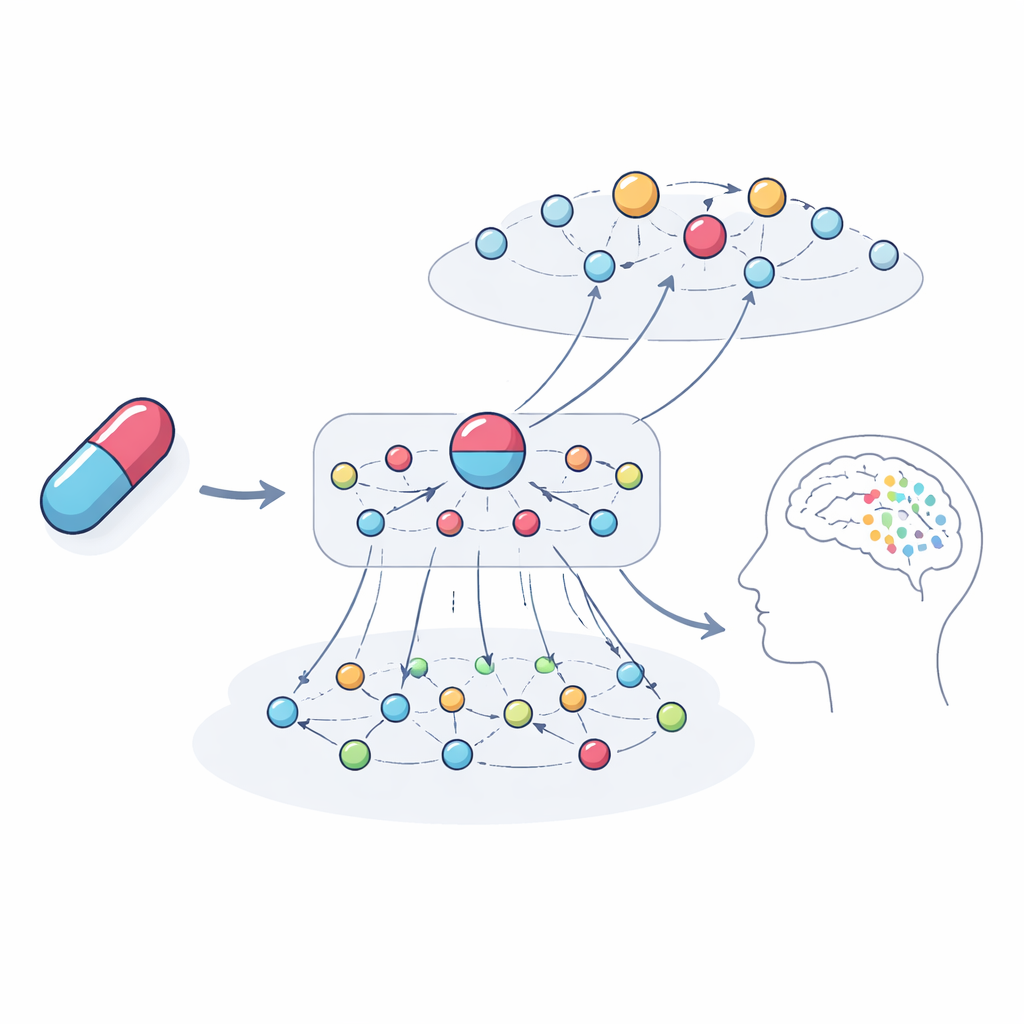
Ett centralt mål var inte bara att förutsäga problem utan att förklara dem. Författarna spårade de mest inflytelserika kedjorna av samband som modellen använde för specifika exempel. För narkos- och antidepressiva ketamin lyfte systemet fram nätverk av gener och relaterade läkemedel som pekar mot hallucinationer och depression som potentiella utfall. Dessa vägar involverade genfamiljer kopplade till dopamin- och serotonin‑signalering, immunsystem- och hormonvägar, samt läkemedel med liknande mål som har fallrapporter om liknande problem. När teamet analyserade de gener modellen betonat fann de att dessa var starkt överrepresenterade för processer som redan är kända för att forma hjärnfunktion och psykiatriska symtom, vilket stärker att förklaringarna är biologiskt meningsfulla snarare än godtyckliga.
Vad detta betyder för patienter och framtida läkemedel
Enkelt uttryckt visar detta arbete att det är möjligt att använda befintliga biologiska och säkerhetsdata för att bygga ett tidigt varningssystem för hjärnrelaterade biverkningar — och att se varför dessa varningar uppstår. HHAN-DSI är inte avsedd att ersätta läkare eller kliniska prövningar, utan att hjälpa forskare och säkerhetsexperter prioritera vilka potentiella biverkningar som ska undersökas och övervakas, särskilt för nya läkemedel med liten direkt erfarenhet. Genom att belysa de molekylära vägar som länkar läkemedel till oönskade symtom kan tillvägagångssättet vägleda säkrare läkemedelsdesign, mer riktad övervakning och i slutändan bättre skydd för patienter som är beroende av behandlingar som verkar i hjärnan.
Citering: Huang, T., Lin, KH., Machado-Vieira, R. et al. Explainable drug side effect prediction in central neural system via biologically informed graph neural network. Transl Psychiatry 16, 205 (2026). https://doi.org/10.1038/s41398-026-03971-1
Nyckelord: läkemedelsbiverkningar, centrala nervsystemet, grafneurala nätverk, läkemedelssäkerhet, förklarbar AI