Clear Sky Science · ru
Объяснимая предсказательная модель побочных эффектов лекарств в центральной нервной системе на основе биологически обоснованной графовой нейронной сети
Почему скрытые риски лекарств важны
Многие препараты, которые помогают нашему мозгу, одновременно могут тихо ему вредить. Головокружение, спутанность сознания, судороги или депрессия могут проявиться лишь после широкого применения лекарства. Традиционные лабораторные и клинические испытания слишком дорогие и медленные, чтобы обнаружить каждую возможную проблему до одобрения, особенно в отношении центральной нервной системы, где побочные эффекты могут быть тонкими, но изменяющими жизнь. В этом исследовании предложена новая компьютерная модель, которая анализирует огромные биологические наборы данных, чтобы ранжировать вероятные побочные эффекты, связанные с мозгом, и показать цепочки молекулярных событий, которые могут их вызывать.
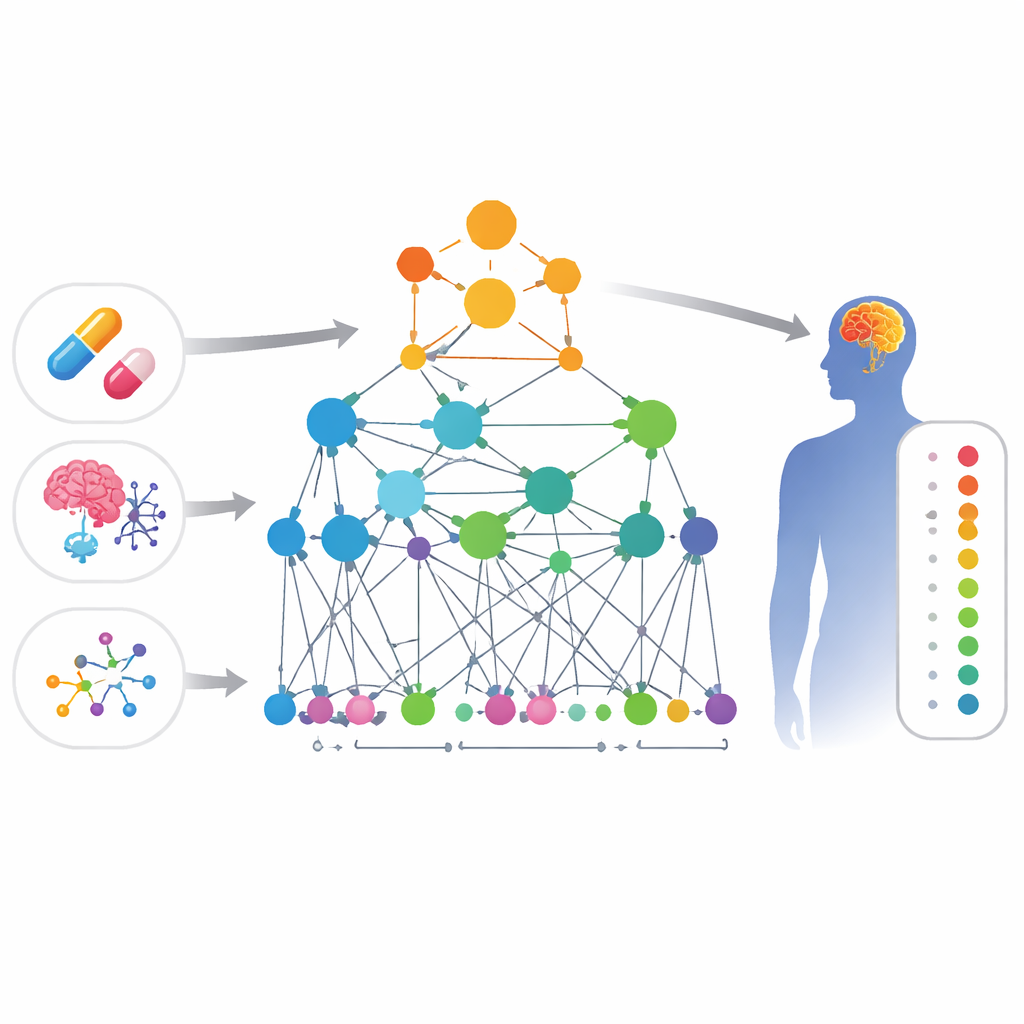
Соединяя точки между препаратами и симптомами
Исследователи построили большую «карту» биологических знаний, связывающую четыре типа сущностей: препараты, побочные эффекты, гены и функции генов. В этой карте каждая единица представлена узлом, а линии между узлами отражают доказательства их связи — например, два гена, физически взаимодействующие друг с другом, два препарата с похожими химическими структурами или препарат, известный тем, что вызывает определённый побочный эффект. Поскольку жалобы, связанные с центральной нервной системой, одновременно часты и часто остаются незамеченными, команда сосредоточила эту карту на проблемах, связанных с мозгом, таких как изменения настроения, нарушения движений и другие неврологические симптомы.
Умная сеть, которая изучает биологию
Поверх этой карты авторы разработали специализированную форму искусственного интеллекта — графовую нейронную сеть. В отличие от стандартной модели, рассматривающей каждый препарат в изоляции, этот подход изучает сеть связей вокруг каждого препарата и побочного эффекта. Модель, названная HHAN‑DSI, «биологически информирована»: ей разрешено передавать информацию только по путям, имеющим биологический смысл — например, от одного гена к другому, с которым он напрямую взаимодействует, от гена к препарату, нацеленному на него, а затем от этого препарата к побочным эффектам, наблюдавшимся у схожих препаратов. Придавая больший вес наиболее информативным путям, система обучается компактным математическим отпечаткам для каждого препарата и каждого побочного эффекта, а затем оценивaет, насколько вероятна связь для любой пары.
Проверка модели
Чтобы проверить, совпадают ли эти предсказания с реальностью, команда обучила модель на кураторской базе данных побочных эффектов, указанных в официальной информации о препаратах, а затем протестировала её как по этому источнику, так и по отдельному набору послерыночных сообщений о безопасности. Эти внешние отчёты фиксируют проблемы, выявившиеся только после широкого применения препаратов. Модель не только отличала истинные пары «препарат–побочный эффект» от ложных, но, что важнее, ранжировала наиболее тревожные эффекты в верхней части списков. Она превзошла несколько существующих методов машинного обучения в задаче ранжирования, особенно при недостатке данных, что типично для новых лекарств. Во многих случаях, где модель казалась «неправой» из‑за отсутствия предсказанного побочного эффекта в кураторской базе, та же связь «препарат–симптом» была обнаружена в реальных отчётах о безопасности, что указывает на то, что модель выявила упущенные риски.
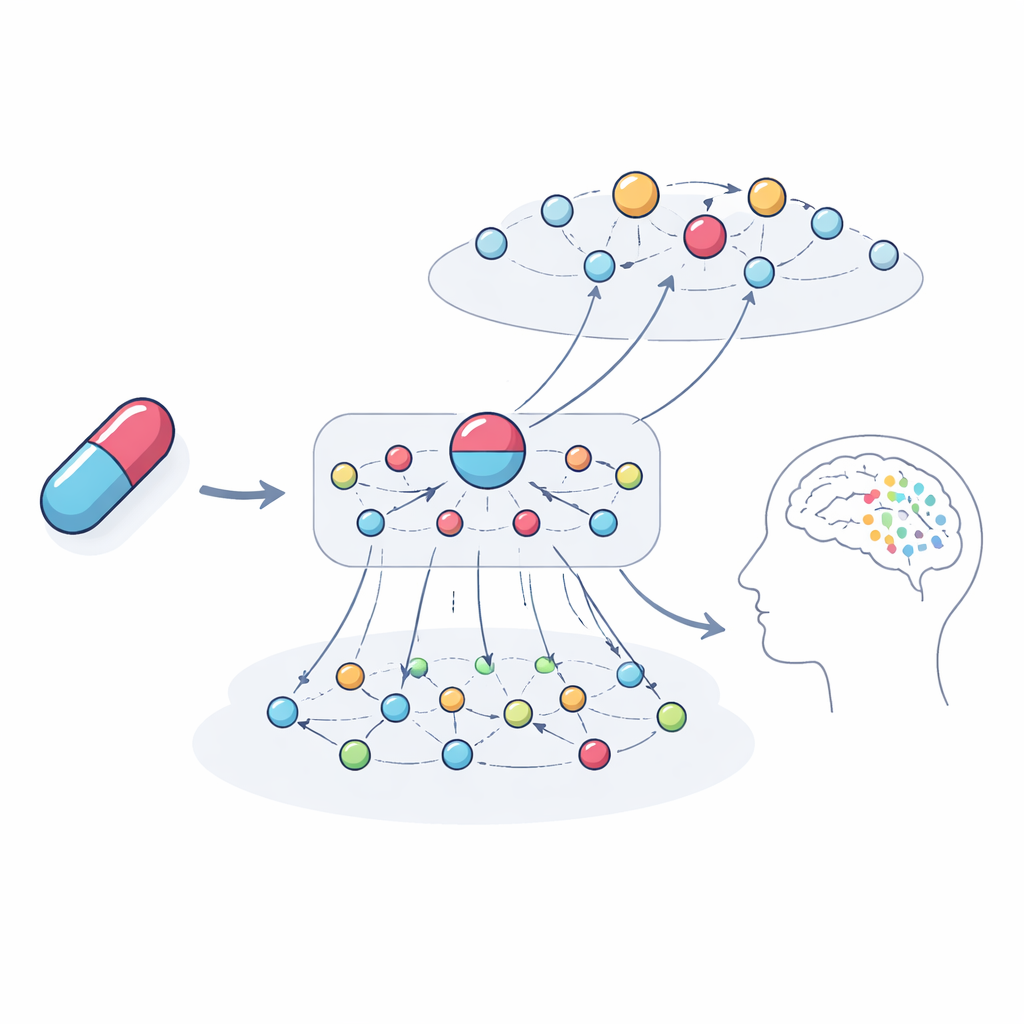
Заглядывая внутрь «чёрного ящика»
Ключевая цель заключалась не только в предсказании проблемы, но и в её объяснении. Авторы проследили наиболее влиятельные цепочки связей, которые модель использовала в конкретных примерах. Для анестетика и антидепрессанта кетамина система выделила сети генов и связанных препаратов, указывающие на галлюцинации и депрессию как возможные последствия. Эти пути включали семейства генов, связанные с дофаминовой и серотониновой сигнализацией, иммунные и гормональные пути, а также препараты с похожими мишенями, по которым имеются отдельные сообщения о схожих проблемах. Когда команда проанализировала гены, на которые модель делала упор, они обнаружили сильное обогащение процессами, уже известными как формирующие функцию мозга и психиатрические симптомы, что подтверждает биологическую обоснованность объяснений, а не их произвольный характер.
Что это значит для пациентов и будущих лекарств
Проще говоря, эта работа демонстрирует, что можно использовать существующие биологические и данные по безопасности для создания системы раннего предупреждения о побочных эффектах, связанных с мозгом — и при этом видеть, почему такие предупреждения возникают. HHAN‑DSI не предназначена для замены врачей или клинических испытаний, а для помощи исследователям и специалистам по безопасности в приоритизации потенциальных побочных эффектов для дальнейшего изучения и мониторинга, особенно для новых препаратов с малым опытом применения. Освещая молекулярные пути, связывающие лекарства с нежелательными симптомами, подход может направлять более безопасную разработку лекарств, более целевое надзорное наблюдение и, в конечном счёте, лучшую защиту пациентов, которые зависят от лечения, воздействующего на мозг.
Цитирование: Huang, T., Lin, KH., Machado-Vieira, R. et al. Explainable drug side effect prediction in central neural system via biologically informed graph neural network. Transl Psychiatry 16, 205 (2026). https://doi.org/10.1038/s41398-026-03971-1
Ключевые слова: побочные эффекты лекарств, центральная нервная система, графовые нейронные сети, фармаконадзор, объяснимая ИИ