Clear Sky Science · pl
Wyjaśnialne przewidywanie działań niepożądanych leków w ośrodkowym układzie nerwowym za pomocą biologicznie informowanej sieci grafowej
Dlaczego ukryte ryzyko leków ma znaczenie
Wiele leków, które pomagają naszemu mózgowi, może jednocześnie go po cichu szkodzić. Zawroty głowy, dezorientacja, drgawki czy depresja mogą ujawnić się dopiero po szerokim zastosowaniu leku. Tradycyjne badania laboratoryjne i kliniczne są zbyt powolne i kosztowne, by wychwycić każde możliwe zagrożenie przed dopuszczeniem do obrotu, zwłaszcza w przypadku ośrodkowego układu nerwowego, gdzie działania niepożądane bywają subtelne, lecz zmieniające życie. W tym badaniu przedstawiono nowy model komputerowy, który analizuje obszerne zbiory danych biologicznych, by wcześnie wskazywać prawdopodobne działania niepożądane związane z mózgiem oraz pokazywać łańcuch zdarzeń molekularnych, które mogą je powodować.
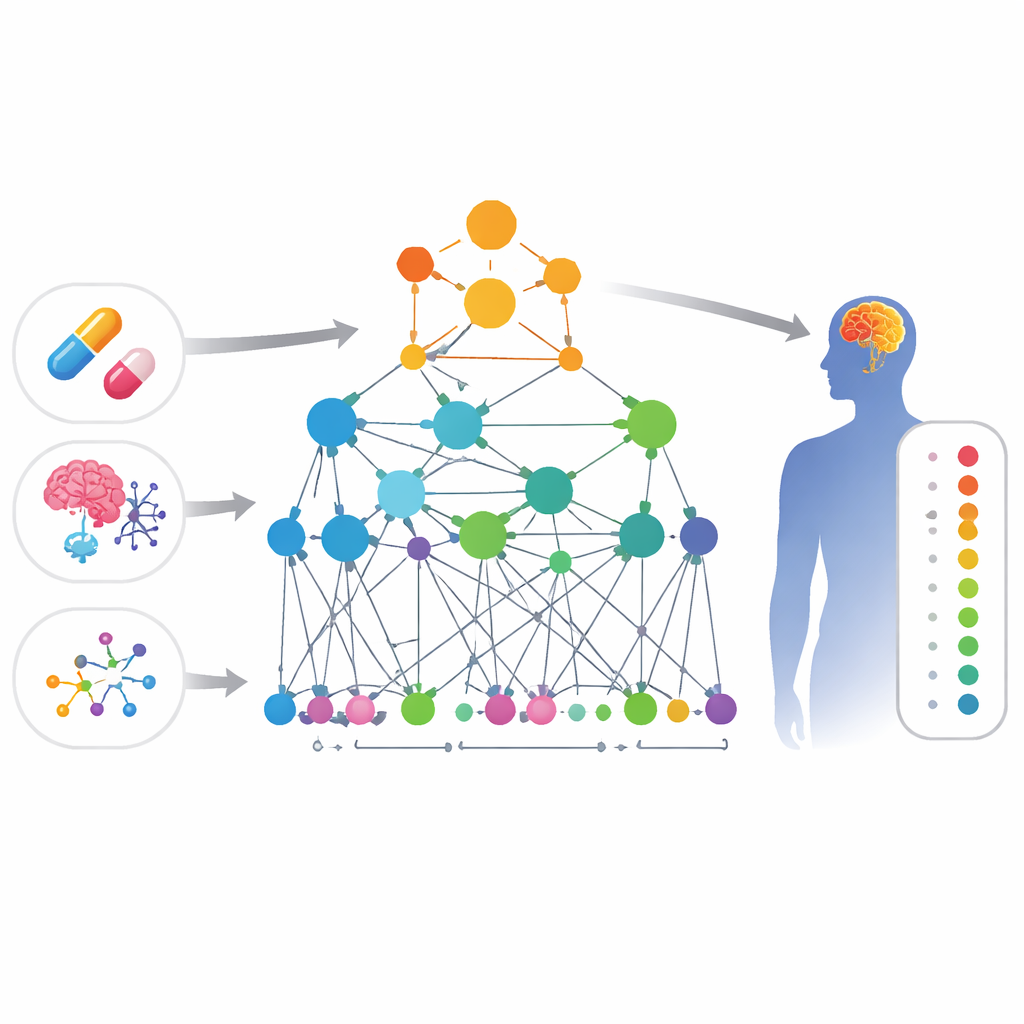
Łączenie kropek między lekami a objawami
Naukowcy zbudowali rozległą „mapę” wiedzy biologicznej łączącą cztery rodzaje elementów: leki, działania niepożądane, geny i funkcje genów. W tej mapie każdy element jest węzłem, a krawędzie między węzłami reprezentują dowody na ich powiązanie — na przykład dwa geny, które fizycznie wchodzą w interakcję, dwa leki o podobnej strukturze chemicznej lub lek, któremu przypisuje się wywoływanie określonego działania niepożądanego. Ponieważ dolegliwości związane z ośrodkowym układem nerwowym są powszechne i często przeoczane, zespół skupił tę mapę na problemach mózgowych, takich jak zmiany nastroju, zaburzenia ruchowe i inne objawy neurologiczne.
Inteligentna sieć, która uczy się biologii
Na bazie tej mapy autorzy zaprojektowali wyspecjalizowaną formę sztucznej inteligencji zwaną grafową siecią neuronową. W przeciwieństwie do standardowego modelu, który traktuje każdy lek izolacyjnie, to podejście analizuje sieć powiązań wokół danego leku i działania niepożądanego. Model, nazwany HHAN-DSI, jest „biologicznie informowany”: pozwala na przekazywanie informacji tylko wzdłuż ścieżek mających sens biologiczny — na przykład od jednego genu do genu, z którym bezpośrednio wchodzi w interakcję, od genu do leku, który go celuje, a następnie od tego leku do działań niepożądanych obserwowanych przy podobnych lekach. Nadając większą wagę najbardziej informatywnym ścieżkom, system uczy się zwartej matematycznej reprezentacji (odcisków) dla każdego leku i każdego działania niepożądanego, a następnie ocenia, jak prawdopodobne jest powiązanie danej pary.
Testowanie modelu
Aby sprawdzić, czy przewidywania odpowiadają rzeczywistości, zespół trenował model na skuratorowanej bazie danych działań niepożądanych zgłaszanych w oficjalnych informacjach o produktach, a następnie testował go wobec tej bazy i oddzielnego zestawu raportów po wprowadzeniu na rynek. Te zewnętrzne raporty obejmują problemy, które pojawiły się dopiero po szerokim stosowaniu leków. Model nie tylko odróżniał prawdziwe pary lek–działanie niepożądane od fałszywych, ale co ważniejsze — umieszczał najbardziej niepokojące efekty wysoko na swoich listach. W zadaniu rangowania przewyższał kilka istniejących metod uczenia maszynowego, zwłaszcza gdy dane były skąpe, co jest typowe dla nowych leków. W wielu przypadkach, gdy model wydawał się „błędny”, bo przewidywane działanie niepożądane nie występowało w skuratorowanej bazie, ten sam związek lek–objaw pojawiał się w raportach z praktyki klinicznej — co sugeruje, że model wykrył przeoczone ryzyka.
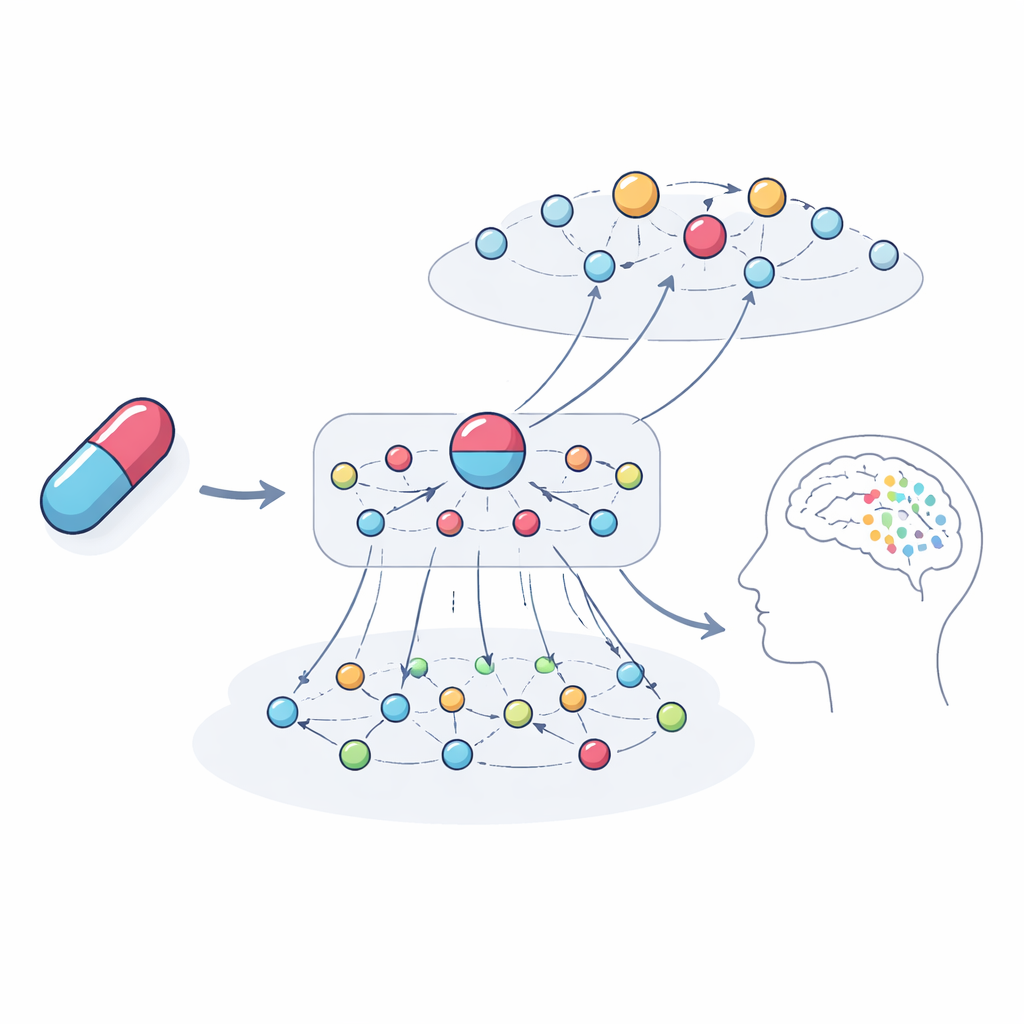
Zajrzeć do wnętrza czarnej skrzynki
Jednym z głównych celów nie było jedynie przewidywanie problemów, lecz ich wyjaśnianie. Autorzy śledzili najbardziej wpływowe łańcuchy powiązań, których model używał w konkretnych przykładach. Dla anestetyku i antydepresantu ketaminy system wyróżnił sieci genów i powiązanych leków wskazujące na halucynacje i depresję jako potencjalne skutki. Ścieżki te obejmowały rodziny genów związane z sygnalizacją dopaminy i serotoniny, szlaki immunologiczne i hormonalne oraz leki o podobnych celach, które mają raportowane przypadki podobnych problemów. Po przeanalizowaniu genów podkreślonych przez model zespół stwierdził, że są one silnie wzbogacone w procesy już znane jako kształtujące funkcje mózgu i objawy psychiatryczne, co wzmacnia przekonanie, że wyjaśnienia mają uzasadnienie biologiczne, a nie są przypadkowe.
Co to oznacza dla pacjentów i przyszłych leków
Mówiąc prościej, ta praca pokazuje, że można wykorzystać istniejące dane biologiczne i bezpieczeństwa do zbudowania systemu wczesnego ostrzegania przed działaniami niepożądanymi związanymi z mózgiem — oraz zobaczyć, dlaczego te ostrzeżenia się pojawiają. HHAN-DSI nie ma zastępować lekarzy ani badań klinicznych, lecz pomagać badaczom i ekspertom ds. bezpieczeństwa priorytetyzować, które potencjalne działania niepożądane należy badać i monitorować, szczególnie w przypadku nowych leków z ograniczonym doświadczeniem klinicznym. Rzucając światło na molekularne szlaki łączące leki z niepożądanymi objawami, podejście to może prowadzić do bezpieczniejszego projektowania leków, bardziej ukierunkowanego nadzoru i w efekcie lepszej ochrony pacjentów polegających na terapiach działających na mózg.
Cytowanie: Huang, T., Lin, KH., Machado-Vieira, R. et al. Explainable drug side effect prediction in central neural system via biologically informed graph neural network. Transl Psychiatry 16, 205 (2026). https://doi.org/10.1038/s41398-026-03971-1
Słowa kluczowe: działania niepożądane leków, ośrodkowy układ nerwowy, sieć neuronowa grafowa, farmakowigilanacja, wyjaśnialna sztuczna inteligencja