Clear Sky Science · sv
Matstrupscancer: från patogenes till precisa terapier
Varför denna cancer är viktig för dig
Matstrupscancer drabbar röret som för maten från munnen till magen och tillhör de dödligaste mag-tarm-cancerformerna globalt. Eftersom tidig sjukdom ofta ger få eller inga symtom blir många först diagnostiserade när sväljningssvårigheter redan föreligger och behandlingsmöjligheterna är begränsade. Denna översikt sammanför vad forskare nu vet om hur matstrupscancer uppstår, hur den växer och hur läkare lär sig att upptäcka den tidigare och behandla den på mer individualiserade sätt som så småningom kan förbättra överlevnaden.
Två huvudtyper av cancer, många olika risker
Matstrupscancer förekommer i praktiken i två huvudformer. Den ena, kallad skivepitelcancer, uppstår ofta i den mellersta och övre delen av matstrupen och är särskilt vanlig i delar av Asien och Afrika. Den har stark koppling till rökning, kraftig alkoholkonsumtion, mycket heta drycker, vissa konserveringsmedel i mat och dålig näring. Den andra, adenocarcinom, framträder vanligtvis där matstrupen möter magen och är vanligare i västländer. Den är förknippad med kronisk reflux, ett tillstånd som kallas Barretts esofagus där slemhinnan förändrar karaktär, samt med fetma och rökning. Tillsammans orsakade dessa cancerformer nästan en halv miljon dödsfall globalt 2022, och män drabbas mycket oftare än kvinnor.
Från frisk slemhinna till tumör
Båda cancerformer utvecklas i steg snarare än att uppträda över en natt. Vid skivepitelcancer kan år av irritation från tobak, alkohol eller andra exponeringar pressa de platta ytcellerna i matstrupen genom stadier av förtjockning, onormal tillväxt och slutligen invasiv cancer. Vid adenocarcinom kan upprepad syra- och gallsyrereflux omvandla den normala slemhinnan till Barrett-vävnad, som sedan kan utvecklas genom lågrads- och högradsförändringar innan den blir malign. Längs denna väg samlar cellerna på sig DNA-skador, förlorar viktiga skyddsfunktioner såsom TP53–"vaktgenet" och får extra kopior av tillväxtfrämjande gener. Författarna beskriver hur moderna "multi-omics"-verktyg, som läser DNA, RNA, proteiner och kemiska markörer på genomet, avslöjar detaljerade kartor över dessa förändringar och hjälper till att skilja lesioner som sannolikt förblir stabila från dem som är redo att bli cancerösa. 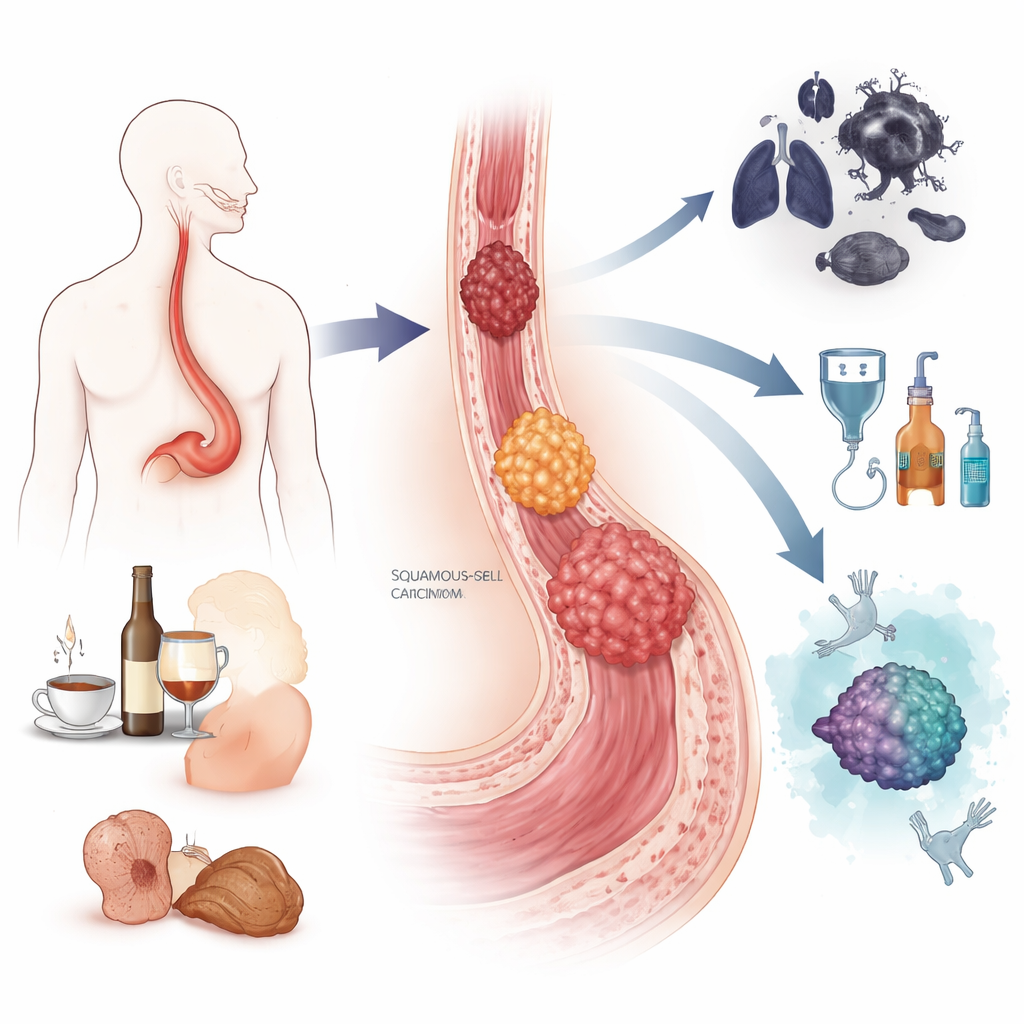
Omgivningen runt tumören
Cancerceller utvecklas inte ensamma: de kommunicerar ständigt med sin omgivning. I matstrupen interagerar premaligna och maligna celler med stödjande celler som fibroblaster, immunceller som antingen kan attackera eller skydda tumörer, blodkärl och till och med bofasta bakterier. Med tiden "utbildas" normala fibroblaster till cancerassocierade fibroblaster som hjälper till att omforma vävnaden, bygga ett skyddande skelett runt tumören och skydda den från cytostatika och immunangrepp. I början kan immunceller känna igen och förstöra onormala celler, men när tumören avancerar skapar den ofta en mer hämmande miljö fylld av utmattade T‑celler och specialiserade makrofager som dämpar antitumörsvar. Förskjutningar i den lokala mikrobiomen, såsom överväxt av vissa munbakterier, kan ytterligare elda på kronisk inflammation eller till och med försvaga behandlingssvar.
Prevention, tidig upptäckt och mindre invasiv behandling
Eftersom så många riskfaktorer hänger ihop med livsstil och miljö har prevention stort genomslag. Att sluta röka och begränsa alkoholintag kan kraftigt minska risken för skivepitelcancer över tid, medan viktkontroll, hantering av reflux och hälsosamma dieter rika på frukt och grönsaker kan sänka risken för adenocarcinom. I regioner med mycket hög förekomst har storskaliga endoskopiprogram visat att direkt inspektion av matstrupens slemhinna och avlägsnande av premaligna lesioner kan minska dödligheten. Nya verktyg syftar till att göra screening mer bekväm och prisvärd: svalbara svampar som samlar celler, blodtester som upptäcker cancerspecifika DNA-metyleringsmönster, saliv‑microRNA‑profiler och artificiell intelligens som hjälper endoskopister att upptäcka små lesioner. När sjukdomen fångas tidigt kan många matstrupscancer nu tas bort med endoskopiska tekniker eller behandlas med riktad ablatering, vilket sparar patienterna stora operationer och ger botfrekvenser över 90 procent. 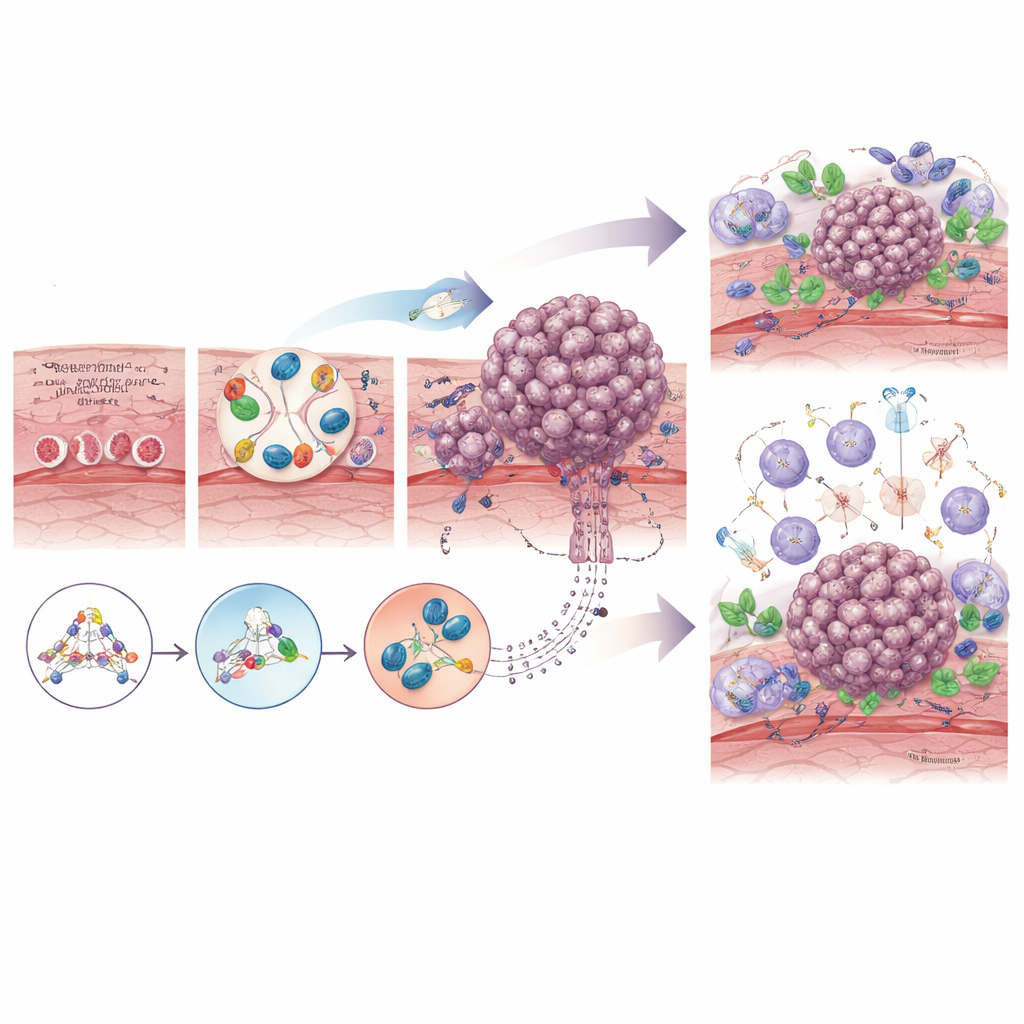
Mot precisa terapier för avancerad sjukdom
För mer avancerade tumörer är den standardmässiga grunden fortfarande operation, cytostatika och strålbehandling, men behandlingen blir allt mer individualiserad. Vissa adenocarcinom överproducerar specifika receptorer som HER2 eller VEGFR2, vilka kan blockeras av riktade läkemedel som läggs till kemoterapi. I båda huvudsubtyperna har immuncheckpoint-hämmare—läkemedel som släpper bromsarna på T‑celler—förbättrat överlevnaden när de kombineras med kemoterapi eller ges efter kemoradiation och operation. Forskare testar också kombinationer av immunterapi med strålning eller riktade medel och utforskar nästa generations tillvägagångssätt såsom CAR‑T och TCR‑modifierade T‑celler. Samtidigt använder de genetiska och immunologiska signaturer för att förutse vilka som sannolikt får nytta och för att förstå varför andra återinsjuknar, med målet att övervinna resistens.
Vad detta betyder för patienter och framtiden
Översikten avslutar att matstrupscancer, som tidigare betraktades som en genomgående dyster diagnos, går in i en era av mer precis prevention och vård. Genom att klargöra hur vardagliga exponeringar, ärftliga benägenheter och mikromiljöförändringar samverkar för att driva tumörer, börjar forskare identifiera de som har högst risk långt innan symtom uppträder och utforma screeningsverktyg anpassade till olika miljöer. För dem som utvecklar cancer styr detaljerad molekylär profilering val mellan endoskopisk behandling, operation, cytostatika, riktade läkemedel och immunterapi. Mycket återstår för att göra tidig upptäckt allmänt tillgänglig och för att hantera behandlingsresistens, men den framväxande bilden är en av stadiga framsteg—från en universell, enstorleks‑passar‑alla‑strategi mot interventioner som är bättre tajmade, mindre invasiva och mer skräddarsydda efter varje persons tumörbiologi.
Citering: Zhang, S., Shen, Y., Zhu, L. et al. Esophageal cancer: from pathogenesis to precision therapies. Sig Transduct Target Ther 11, 134 (2026). https://doi.org/10.1038/s41392-026-02614-7
Nyckelord: matstrupscancer, Barretts esofagus, cancerscreening, tumörmikromiljö, immunterapi