Clear Sky Science · nl
Slokdarmkanker: van pathogenese tot precisietherapieën
Waarom deze kanker voor u van belang is
Slokdarmkanker treft de buis die voedsel van de mond naar de maag voert en behoort tot de dodelijkste maag‑darminfecties wereldwijd. Omdat de ziekte in een vroeg stadium vaak weinig of geen klachten geeft, wordt bij veel mensen pas een diagnose gesteld wanneer slikken al moeilijk is en behandelopties beperkt zijn. Dit overzicht bundelt wat wetenschappers nu weten over hoe slokdarmkanker ontstaat, hoe ze groeit, en hoe artsen leren om de ziekte eerder te detecteren en meer gepersonaliseerd te behandelen — wat uiteindelijk de overleving zou kunnen verbeteren.
Twee hoofdtypen, veel verschillende risicofactoren
Slokdarmkanker komt in feite in twee belangrijke vormen voor. Eén vorm, squameuze‑celcarcinoom genoemd, ontstaat vaak in het midden en bovenste deel van de slokdarm en komt vooral voor in delen van Azië en Afrika. Deze vorm is sterk gerelateerd aan roken, zwaar alcoholgebruik, zeer hete dranken, bepaalde voedselconserveermiddelen en slechte voeding. De andere, adenocarcinoom, verschijnt meestal waar de slokdarm de maag ontmoet en komt vaker voor in westerse landen. Dit type wordt in verband gebracht met chronische zure reflux, een aandoening die Barretts slokdarm wordt genoemd waarbij het slijmvlies van karakter verandert, en met obesitas en roken. Samen veroorzaakten deze kankers in 2022 bijna een half miljoen sterfgevallen wereldwijd, en mannen worden veel vaker getroffen dan vrouwen.
Van gezond slijmvlies naar tumor
Beide kankertypen ontwikkelen zich via een stapsgewijs proces en verschijnen niet van de ene op de andere dag. Bij het squameuze‑celcarcinoom kunnen jarenlange irritatie door tabak, alcohol of andere blootstellingen de platte cellen van het slijmvlies door fasen van verdikking en abnormale groei duwen, totdat er invasieve kanker ontstaat. Bij adenocarcinoom kan herhaaldelijke zure en galreflux het normale slijmvlies omzetten in Barrett‑weefsel, dat vervolgens via laag‑ en hooggradige voorstadia tot maligniteit kan doorgroeien. Gedurende dit traject raken cellen beschadigd in hun DNA, verliezen ze belangrijke bewakers zoals het TP53‑gen en krijgen ze extra kopieën van genen die de groei stimuleren. De auteurs beschrijven hoe moderne "multi‑omics"‑instrumenten, die DNA, RNA, eiwitten en chemische tags op het genoom lezen, gedetailleerde kaarten van deze veranderingen blootleggen en helpen onderscheid te maken tussen laesies die waarschijnlijk stabiel blijven en die klaarstaan om kanker te worden. 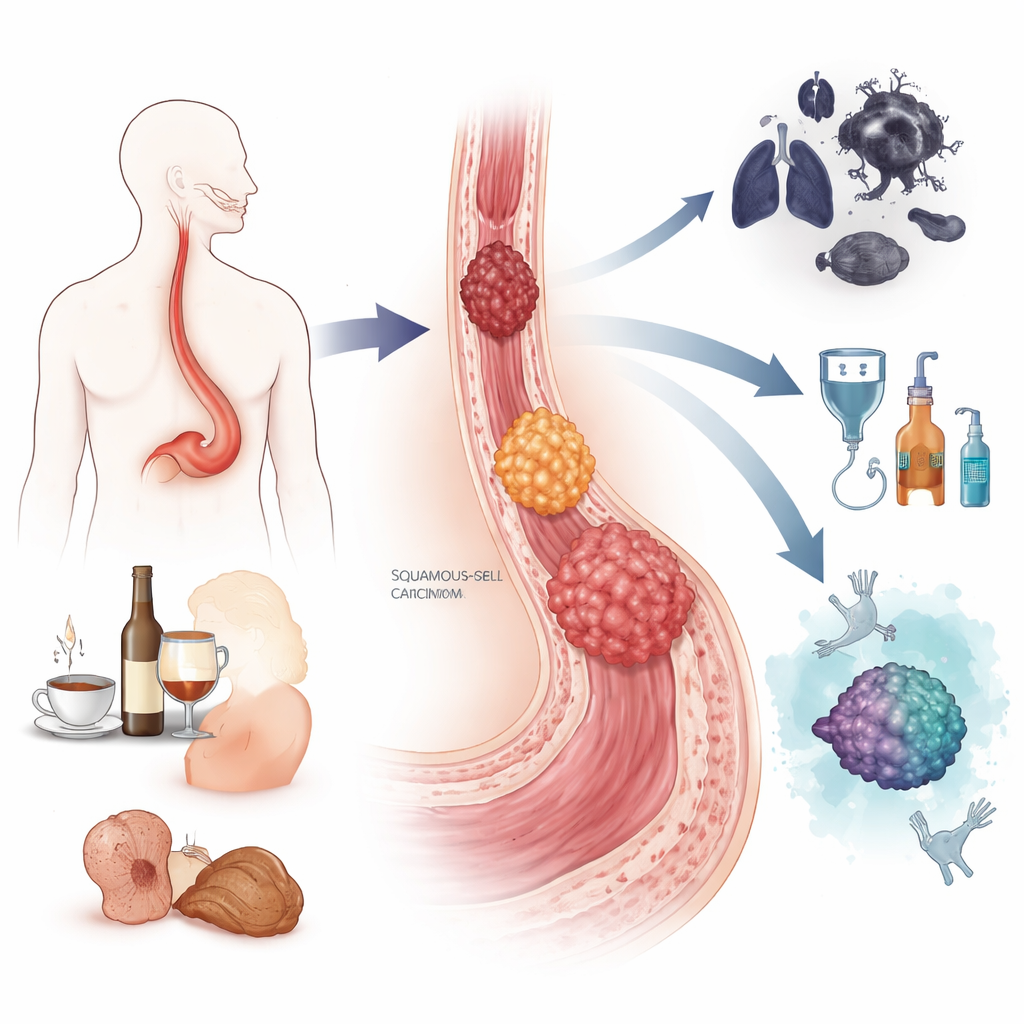
De omgeving rond de tumor
Kankercellen evolueren niet alleen: ze communiceren voortdurend met hun omgeving. In de slokdarm interageren voor‑tumorale en tumorale cellen met ondersteunende cellen die fibroblasten worden genoemd, met immuuncellen die tumoren kunnen aanvallen of beschermen, met bloedvaten en zelfs met residentiële bacteriën. In de loop van de tijd worden normale fibroblasten "opgeleid" tot kanker‑gerelateerde fibroblasten die helpen het weefsel te herschikken, een beschermend geraamte rond de tumor opbouwen en de tumor afschermen tegen chemotherapie en immuunaanvallen. In het begin kunnen immuuncellen abnormale cellen herkennen en vernietigen, maar naarmate de tumor vordert, creëert zij vaak een meer onderdrukkende omgeving vol uitgeputte T‑cellen en gespecialiseerde macrofagen die antitumorale responsen dempen. Verschuivingen in het lokale microbioom, zoals overgroei van bepaalde mondbacteriën, kunnen chronische ontsteking verder aanwakkeren of zelfs de respons op behandeling verminderen.
Preventie, vroegdetectie en minder invasieve behandeling
Aangezien veel risicofactoren samenhangen met leefstijl en omgeving, heeft preventie groot potentieel. Stoppen met roken en het beperken van alcoholgebruik kunnen het risico op squameuze‑celkanker in de loop van de tijd sterk verlagen, terwijl gewichtsbeheersing, het onder controle houden van zure reflux en een gezond dieet rijk aan fruit en groenten het risico op adenocarcinoom kunnen verminderen. In regio’s met zeer hoge incidentie hebben grootschalige endoscopieprogramma’s aangetoond dat directe inspectie van het slokdarmslijmvlies en het verwijderen van voorstadia sterfte kan verminderen. Nieuwe instrumenten proberen screening comfortabeler en betaalbaarder te maken: inslikbare sponzen die cellen verzamelen, bloedtesten die kankerspecifieke DNA‑methylatiepatronen detecteren, speekselmicroRNA‑profielen en kunstmatige‑intelligentiesystemen die endoscopisten helpen kleine laesies te herkennen. Wanneer ze vroeg worden ontdekt, kunnen veel slokdarmkankers nu worden verwijderd met endoscopische technieken of behandeld met gerichte ablatie, waardoor patiënten grote operaties kunnen vermijden en genezingspercentages van boven de 90 procent mogelijk zijn. 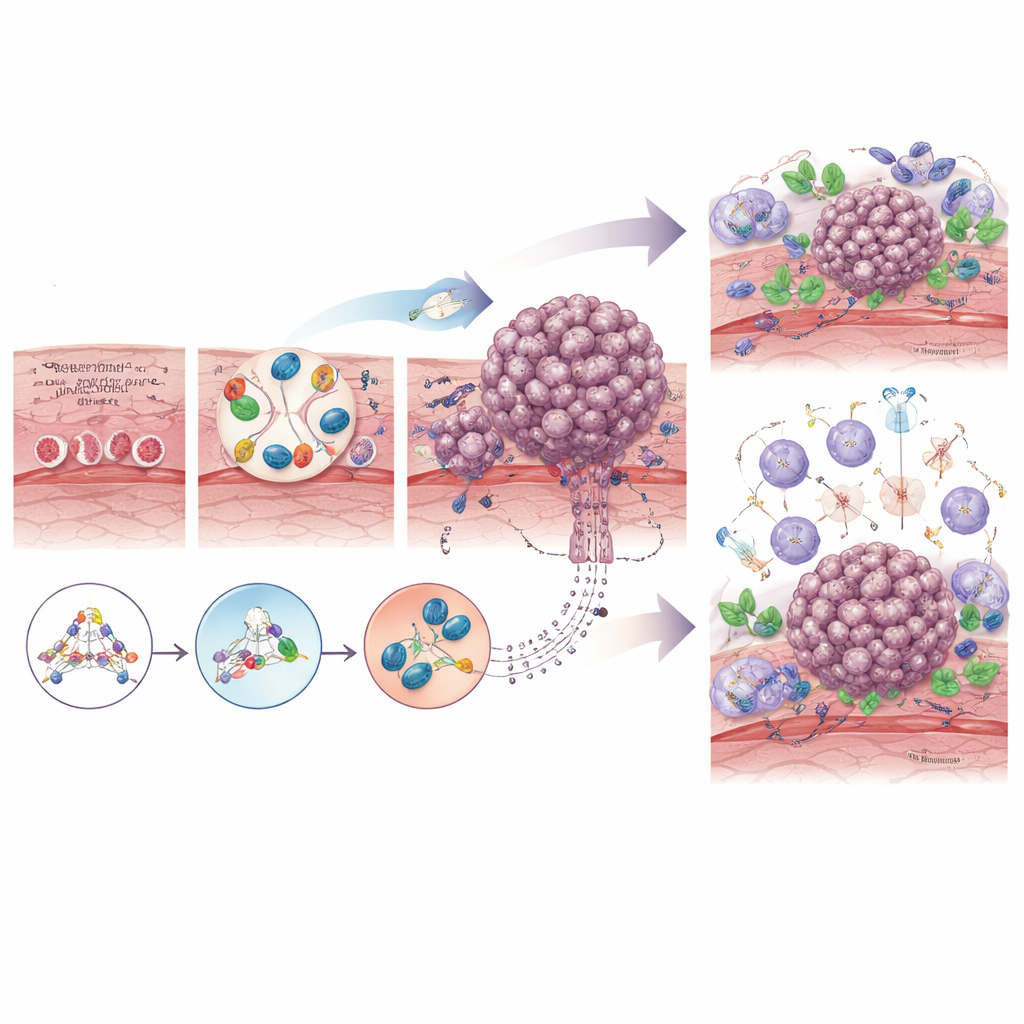
Op weg naar precisietherapieën voor gevorderde ziekte
Bij meer gevorderde tumoren blijven chirurgie, chemotherapie en bestraling de hoeksteen van de behandeling, maar de zorg wordt steeds meer op maat gemaakt. Sommige adenocarcinomen produceren te veel van specifieke receptoren zoals HER2 of VEGFR2, die kunnen worden geblokkeerd door gerichte geneesmiddelen die aan de chemotherapie worden toegevoegd. In beide hoofdsubtypen hebben immuuncheckpointremmers — geneesmiddelen die de remmen op T‑cellen wegnemen — de overleving verbeterd wanneer ze werden gecombineerd met chemotherapie of gegeven na chemoradiatie en chirurgie. Onderzoekers testen ook combinaties van immunotherapie met bestraling of gerichte middelen en verkennen next‑generation benaderingen zoals CAR‑T en TCR‑gemodificeerde T‑cellen. Tegelijkertijd gebruiken zij genetische en immuunkenmerken om te voorspellen wie het meest waarschijnlijk baat heeft en om te begrijpen waarom anderen hervallen, met als doel resistentie te overwinnen.
Wat dit betekent voor patiënten en de toekomst
De review besluit dat slokdarmkanker, ooit beschouwd als een uniform sombere diagnose, een tijdperk van meer precieze preventie en zorg ingaat. Door te verduidelijken hoe alledaagse blootstellingen, erfelijke aanleg en veranderingen in de micro‑omgeving samenwerken om tumoren aan te jagen, beginnen wetenschappers mensen met het hoogste risico lang voordat symptomen optreden te identificeren en screeningsinstrumenten te ontwerpen die bij verschillende settings passen. Voor degenen die wel kanker ontwikkelen, leidt gedetailleerde moleculaire profilering de keuze tussen endoscopische therapie, chirurgie, chemotherapie, gerichte middelen en immunotherapie. Er is nog veel werk nodig om vroegdetectie breed toegankelijk te maken en om behandelingsresistentie aan te pakken, maar het opkomende beeld is er een van gestage vooruitgang — een verschuiving van one‑size‑fits‑all naar interventies die beter getimed, minder invasief en nauwer afgestemd zijn op de tumorbiologie van elk individu.
Bronvermelding: Zhang, S., Shen, Y., Zhu, L. et al. Esophageal cancer: from pathogenesis to precision therapies. Sig Transduct Target Ther 11, 134 (2026). https://doi.org/10.1038/s41392-026-02614-7
Trefwoorden: slokdarmkanker, Barretts slokdarm, kankerscreening, tumormicro‑omgeving, immunotherapie