Clear Sky Science · fr
Cancer de l’œsophage : de la pathogenèse aux thérapies de précision
Pourquoi ce cancer vous concerne
Le cancer de l’œsophage touche le conduit qui transporte les aliments de la bouche vers l’estomac et fait partie des cancers digestifs les plus meurtriers dans le monde. Parce que la maladie précoce provoque souvent peu ou pas de symptômes, de nombreuses personnes sont diagnostiquées seulement lorsque la déglutition est déjà difficile et que les options de traitement sont limitées. Cette revue rassemble les connaissances actuelles sur le démarrage et la progression du cancer de l’œsophage et sur la manière dont les cliniciens apprennent à le détecter plus tôt et à le traiter de façon plus personnalisée, ce qui pourrait à terme améliorer la survie.
Deux principaux types de cancer, de nombreux facteurs de risque
Le cancer de l’œsophage existe en réalité sous deux formes majeures. La première, appelée carcinome épidermoïde (ou à cellules squameuses), tend à apparaître dans la partie moyenne et supérieure de l’œsophage et est particulièrement fréquente dans certaines régions d’Asie et d’Afrique. Elle est fortement liée au tabagisme, à une consommation excessive d’alcool, aux boissons très chaudes, à certains conservateurs alimentaires et à une mauvaise nutrition. L’autre, l’adénocarcinome, survient généralement à la jonction entre l’œsophage et l’estomac et est plus répandue dans les pays occidentaux. Il est associé au reflux acide chronique, à une affection appelée œsophage de Barrett dans laquelle la muqueuse change de nature, ainsi qu’à l’obésité et au tabagisme. Ensemble, ces cancers ont causé près d’un demi-million de décès dans le monde en 2022, et les hommes sont touchés beaucoup plus souvent que les femmes.
De la muqueuse saine à la tumeur
Les deux types de cancer se développent par étapes plutôt que d’apparaître du jour au lendemain. Dans le carcinome épidermoïde, des années d’irritation due au tabac, à l’alcool ou à d’autres expositions peuvent conduire les cellules épithéliales plates de l’œsophage à travers des stades d’épaississement, de croissance anormale, puis finalement de cancer invasif. Dans l’adénocarcinome, des reflux répétés d’acide et de bile peuvent transformer la muqueuse normale en tissu de Barrett, qui peut ensuite progresser par des lésions précancéreuses de bas grade puis de haut grade avant de devenir malin. Au cours de ce processus, les cellules accumulent des lésions de l’ADN, perdent des garde-fous clés comme le gène « gardien » TP53 et acquièrent des copies supplémentaires de gènes favorisant la croissance. Les auteurs décrivent comment les outils modernes « multi-omiques », qui lisent l’ADN, l’ARN, les protéines et les marques chimiques sur le génome, révèlent des cartes détaillées de ces changements et aident à distinguer les lésions susceptibles de rester stables de celles prêtes à devenir cancéreuses. 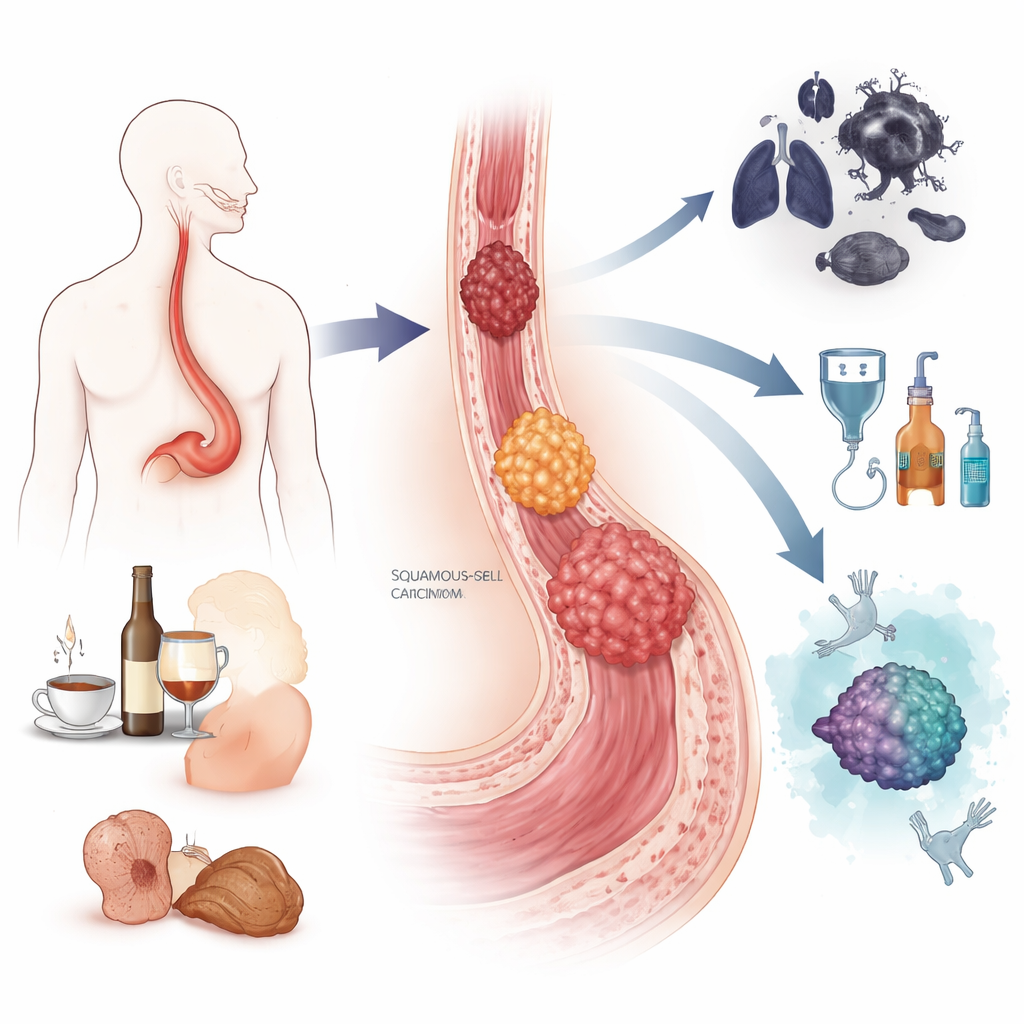
Le voisinage autour de la tumeur
Les cellules cancéreuses n’évoluent pas seules : elles communiquent en permanence avec leur environnement. Dans l’œsophage, les cellules pré‑cancéreuses et cancéreuses interagissent avec des cellules de soutien appelées fibroblastes, des cellules immunitaires qui peuvent soit attaquer soit protéger les tumeurs, des vaisseaux sanguins et même des bactéries résidentes. Avec le temps, les fibroblastes normaux sont « éduqués » en fibroblastes associés au cancer qui contribuent à remodeler le tissu, à construire une armature protectrice autour de la tumeur et à la protéger de la chimiothérapie et des attaques immunitaires. Au départ, les cellules immunitaires peuvent reconnaître et détruire les cellules anormales, mais à mesure que la tumeur progresse, elle crée souvent un environnement plus suppressif rempli de lymphocytes T épuisés et de macrophages spécialisés qui atténuent les réponses anti‑tumorales. Des modifications du microbiome local, comme la prolifération de certaines bactéries buccales, peuvent en outre entretenir l’inflammation chronique ou même réduire l’efficacité des traitements.
Prévention, détection précoce et traitements moins invasifs
Comme de nombreux facteurs de risque sont liés au mode de vie et à l’environnement, la prévention a un véritable impact. Arrêter de fumer et limiter la consommation d’alcool peut réduire considérablement le risque de carcinome épidermoïde au fil du temps, tandis que le contrôle du poids, la prise en charge du reflux acide et des régimes alimentaires sains riches en fruits et légumes peuvent diminuer le risque d’adénocarcinome. Dans les régions à forte incidence, des programmes d’endoscopie à grande échelle ont montré qu’examiner directement la muqueuse œsophagienne et enlever les lésions précancéreuses peut réduire la mortalité. De nouveaux outils visent à rendre le dépistage plus confortable et moins coûteux : des éponges avalables qui prélèvent des cellules, des tests sanguins détectant des profils de méthylation de l’ADN spécifiques au cancer, des profils de microARN salivaire et des systèmes d’intelligence artificielle aidant les endoscopistes à repérer de petites lésions. Lorsqu’ils sont dépistés tôt, de nombreux cancers de l’œsophage peuvent aujourd’hui être retirés par des techniques endoscopiques ou traités par Ablation ciblée, épargnant aux patients une chirurgie majeure et offrant des taux de guérison supérieurs à 90 %. 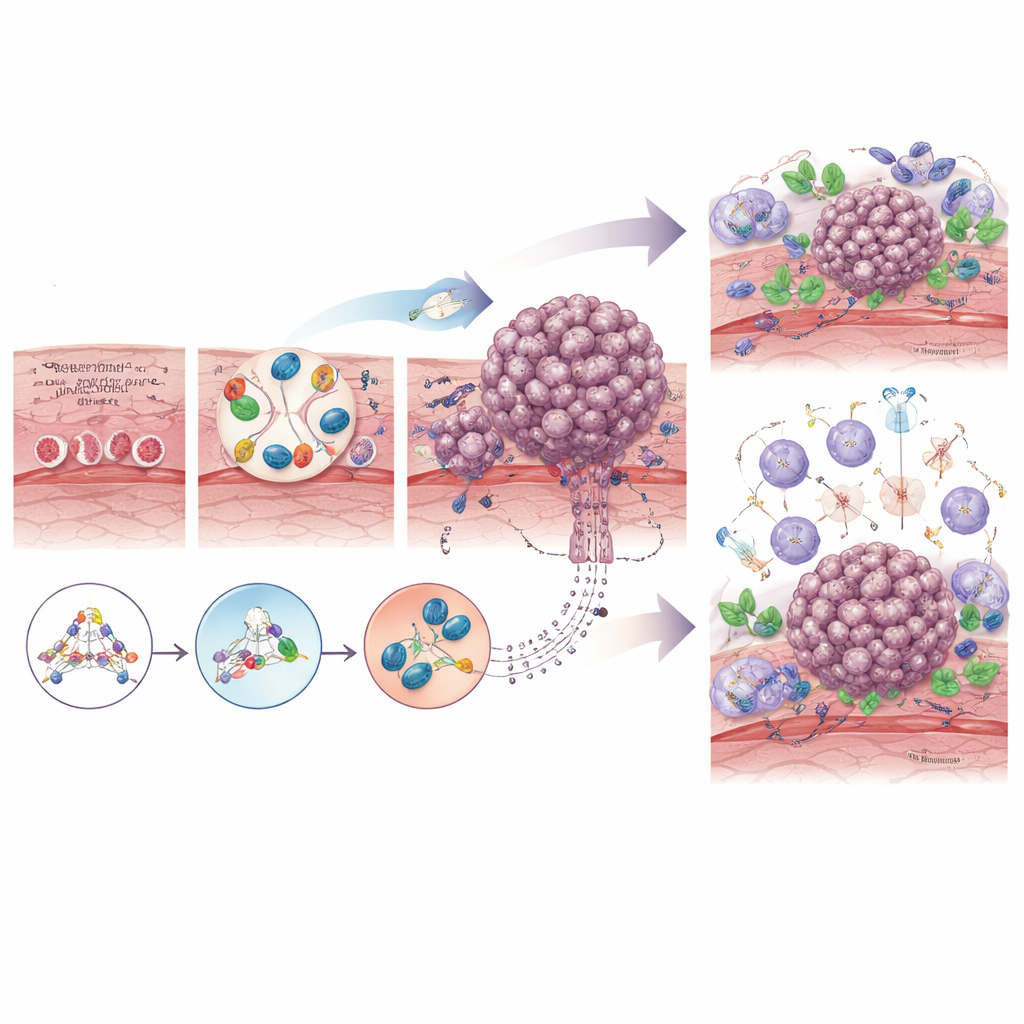
Vers des thérapies de précision pour les formes avancées
Pour les tumeurs plus avancées, l’ossature du traitement reste la chirurgie, la chimiothérapie et la radiothérapie, mais la prise en charge devient de plus en plus individualisée. Certains adénocarcinomes surexpriment des récepteurs spécifiques tels que HER2 ou VEGFR2, qui peuvent être bloqués par des médicaments ciblés associés à la chimiothérapie. Dans les deux grands sous‑types, les inhibiteurs de points de contrôle immunitaires — des médicaments qui relâchent les freins sur les lymphocytes T — ont amélioré la survie lorsqu’ils sont associés à la chimiothérapie ou administrés après une chimioradiation et une chirurgie. Les chercheurs testent également des combinaisons d’immunothérapie avec la radiothérapie ou des agents ciblés, et explorent des approches de nouvelle génération comme les cellules CAR‑T et les lymphocytes T génétiquement modifiés par récepteur TCR. En parallèle, ils utilisent des signatures génétiques et immunitaires pour prédire qui est le plus susceptible de bénéficier des traitements et pour comprendre pourquoi d’autres rechutent, dans le but de surmonter les mécanismes de résistance.
Ce que cela signifie pour les patients et l’avenir
La revue conclut que le cancer de l’œsophage, autrefois perçu comme un diagnostic uniformément sombre, entre dans une ère de prévention et de soins plus précis. En clarifiant comment les expositions quotidiennes, les prédispositions héréditaires et les changements micro‑environnementaux coopèrent pour favoriser les tumeurs, les scientifiques commencent à identifier les personnes à risque élevé bien avant l’apparition des symptômes et à concevoir des outils de dépistage adaptés à différents contextes. Pour ceux qui développent un cancer, le profilage moléculaire détaillé oriente le choix entre la thérapie endoscopique, la chirurgie, la chimiothérapie, les médicaments ciblés et l’immunothérapie. Il reste beaucoup à faire pour rendre la détection précoce largement accessible et pour lutter contre la résistance aux traitements, mais le tableau qui se dessine est celui d’un progrès constant — une transition d’approches uniformes vers des interventions mieux coordonnées, moins invasives et mieux adaptées à la biologie tumorale de chaque personne.
Citation: Zhang, S., Shen, Y., Zhu, L. et al. Esophageal cancer: from pathogenesis to precision therapies. Sig Transduct Target Ther 11, 134 (2026). https://doi.org/10.1038/s41392-026-02614-7
Mots-clés: cancer de l’œsophage, œsophage de Barrett, dépistage du cancer, <keyword>immunothérapie