Clear Sky Science · ru
Рак пищевода: от патогенеза до точных терапий
Почему этот рак важен для вас
Рак пищевода поражает трубку, по которой пища проходит от рта к желудку, и является одним из самых смертоносных заболеваний пищеварительной системы в мире. Поскольку на ранних стадиях болезнь часто вызывает мало или вообще не вызывает симптомов, многие люди диагностируются лишь тогда, когда глотание уже затруднено и возможности лечения ограничены. В этом обзоре собраны современные представления о том, как возникает рак пищевода, как он прогрессирует и как врачи учатся обнаруживать его раньше и лечить более персонализированно — что в перспективе может улучшить выживаемость.
Два основных типа рака и множество факторов риска
Рак пищевода фактически встречается в двух основных формах. Одна, называемая плоскоклеточной карциномой, обычно развивается в среднем и верхнем отделе пищевода и особенно распространена в некоторых регионах Азии и Африки. Она тесно связана с курением, чрезмерным употреблением алкоголя, очень горячими напитками, некоторыми пищевыми консервантами и плохим питанием. Другая форма, аденокарцинома, чаще появляется в месте соединения пищевода и желудка и более характерна для западных стран. Она ассоциирована с хроническим кислотным рефлюксом, состоянием, называемым пищеводом Барретта, при котором слизистая меняет свою структуру, а также с ожирением и курением. В совокупности эти типы рака в 2022 году вызвали почти полмиллиона смертей в мире, и мужчины страдают ими значительно чаще, чем женщины.
От здоровой слизистой к опухоли
Оба типа рака развиваются ступенчато, а не возникают внезапно. При плоскоклеточной карциноме годы раздражения от табака, алкоголя или других воздействий могут переводить плоские клетки поверхности пищевода через стадии утолщения, атипического роста и, в конечном счёте, инвазивной опухоли. При аденокарциноме повторяющийся заброс кислоты и желчи может трансформировать нормальную слизистую в ткань Барретта, которая затем может прогрессировать через низкозлокачественные и высокозлокачественные предраковые изменения перед переходом в злокачественное состояние. На этом пути клетки накапливают повреждения ДНК, теряют ключевые защитные механизмы, такие как ген-«страж» TP53, и приобретают дополнительные копии генов, стимулирующих рост. Авторы описывают, как современные «мультиомные» инструменты, считывающие ДНК, РНК, белки и химические метки на геноме, создают детальные карты этих изменений и помогают отличать поражения, которые, вероятно, останутся стабильными, от тех, которые склонны превратиться в рак. 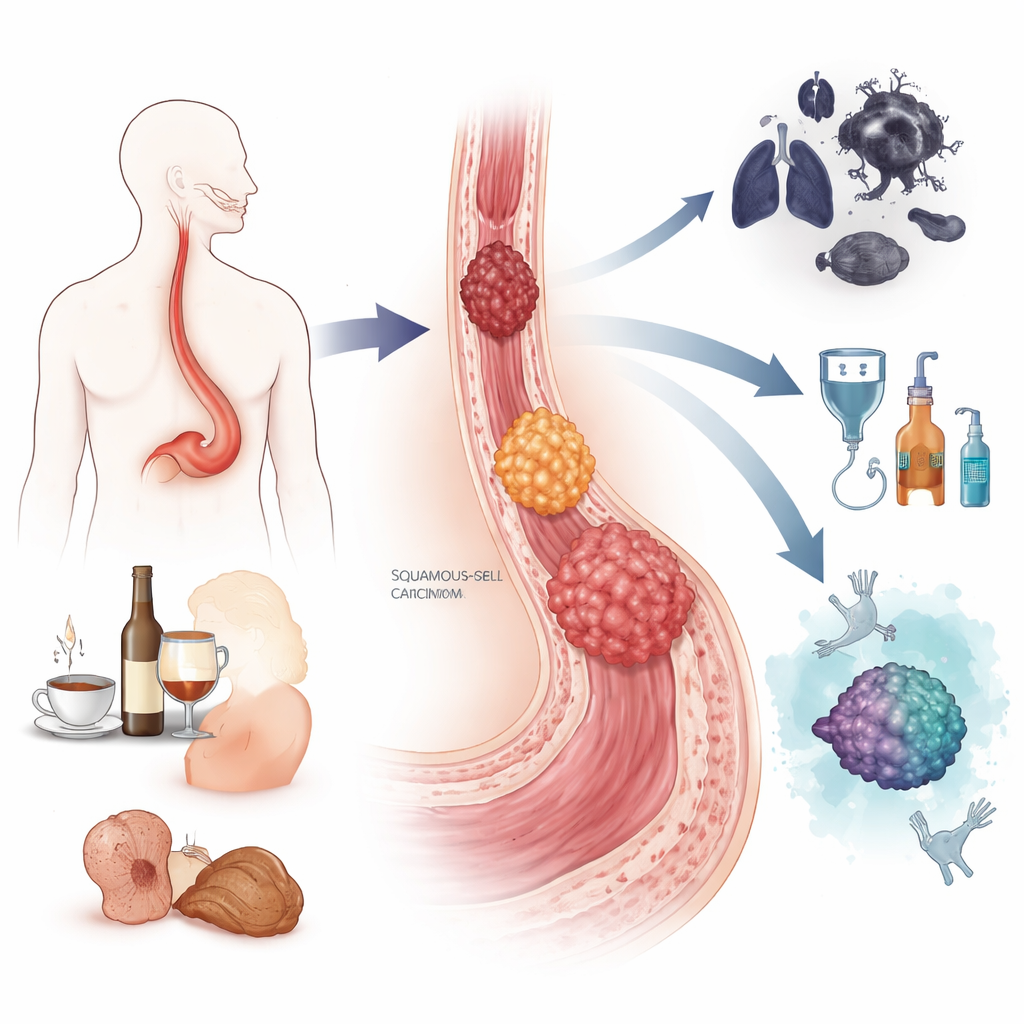
Окружающая опухоль среда
Раковые клетки не эволюционируют в одиночку: они постоянно взаимодействуют с окружением. В пищеводе предраковые и раковые клетки взаимодействуют с поддерживающими клетками — фибробластами, иммунными клетками, которые могут либо атаковать, либо защищать опухоль, кровеносными сосудами и даже с обитающими там бактериями. Со временем нормальные фибробласты «обучаются» и становятся ассоциированными с раком фибробластами, которые помогают перестраивать ткань, формировать защитный каркас вокруг опухоли и защищать её от химиотерапии и иммунной атаки. На ранних этапах иммунные клетки могут распознавать и уничтожать аномальные клетки, но по мере прогрессирования опухоль часто создаёт более подавляющую среду, заполненную истощёнными Т-клетками и специализированными макрофагами, которые ослабляют противоопухолевые ответы. Сдвиги в локальном микробиоте, например чрезмерный рост некоторых ротовых бактерий, могут дополнительно подпитывать хроническое воспаление или даже снижать эффективность лечения.
Профилактика, раннее выявление и менее инвазивное лечение
Поскольку многие факторы риска связаны с образом жизни и окружающей средой, профилактика обладает реальной силой. Отказ от курения и ограничение употребления алкоголя со временем существенно снижают риск плоскоклеточной карциномы, тогда как контроль веса, лечение кислотного рефлюкса и здоровое питание, богатое фруктами и овощами, могут уменьшить риск аденокарциномы. В регионах с очень высокой заболеваемостью масштабные программы эндоскопии показали, что прямой осмотр слизистой пищевода и удаление предраковых очагов могут снизить смертность. Новые инструменты стремятся сделать скрининг более комфортным и доступным: проглатываемые губки для сбора клеток, анализы крови, детектирующие характерные для рака паттерны метилирования ДНК, профили микРНК в слюне и системы искусственного интеллекта, помогающие эндоскопистам обнаруживать крошечные поражения. При ранней диагностике многие раки пищевода теперь можно удалить эндоскопическими методиками или лечить таргетной абляцией, что позволяет пациентам избежать крупной операции и обеспечивает показатели излечения выше 90 процентов. 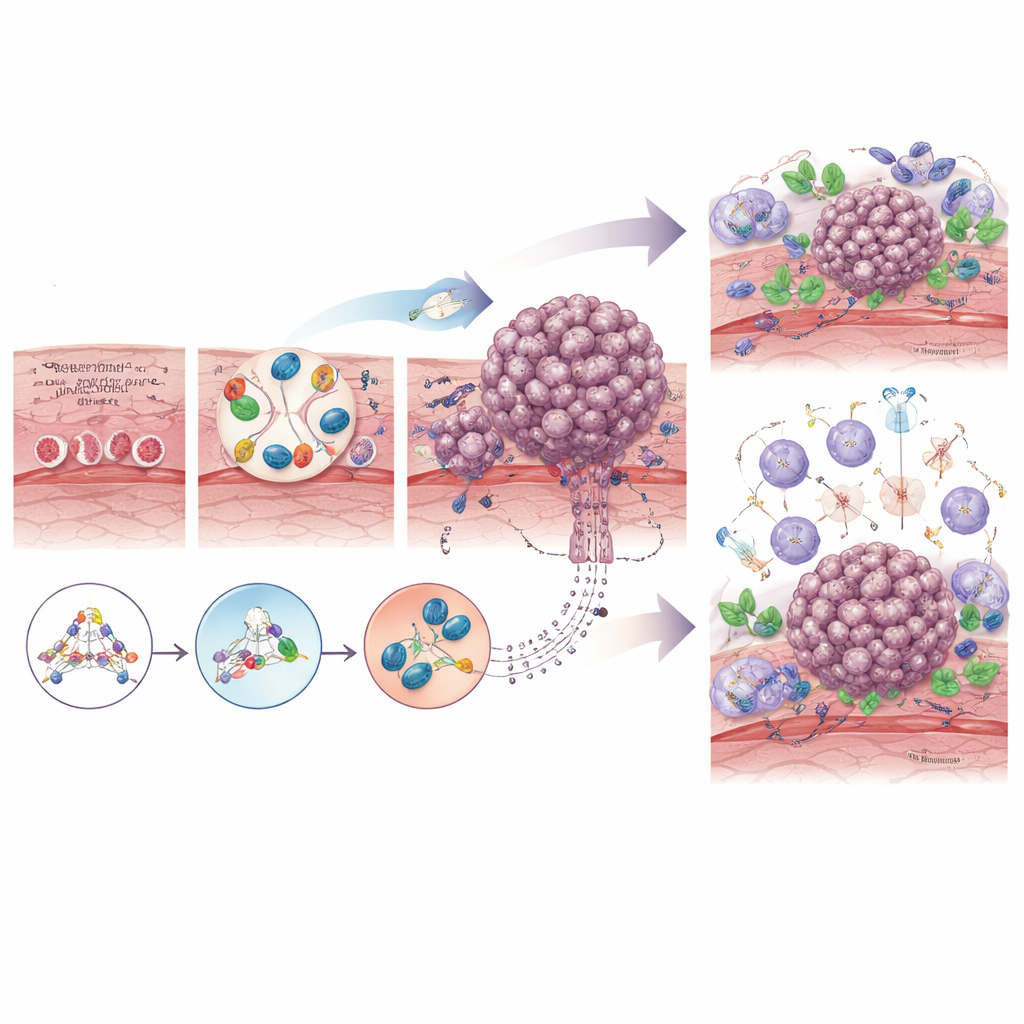
К точным терапиям при распространённой болезни
Для более продвинутых опухолей стандарт по-прежнему включает операцию, химиотерапию и облучение, но лечение становится всё более индивидуализированным. Некоторые аденокарциномы сверхэкспрессируют специфические рецепторы, такие как HER2 или VEGFR2, которые можно блокировать таргетными препаратами в сочетании с химиотерапией. В обоих основных подтипах ингибиторы иммунных контрольных точек — препараты, снимающие «тормоза» с Т-клеток — улучшили выживаемость при комбинировании с химиотерапией или при применении после химиолучевой терапии и операции. Исследователи также испытывают сочетания иммунотерапии с облучением или таргетными агентами и изучают методы следующего поколения, такие как CAR-T и Т-клетки с отредактированными TCR. Одновременно они используют генетические и иммунные подписи, чтобы предсказывать, кто с наибольшей вероятностью получит пользу, и понимать, почему у других возникает рецидив, с целью преодолеть резистентность.
Что это значит для пациентов и будущего
Авторы приходят к выводу, что рак пищевода, когда-то рассматривавшийся как практически безнадёжный диагноз, вступает в эпоху более точной профилактики и ухода. Уточняя, как повседневные воздействия, наследственная предрасположенность и изменения микроокружения совместно приводят к развитию опухоли, учёные начинают выявлять людей с высоким риском задолго до появления симптомов и разрабатывать скрининговые инструменты, подходящие для разных условий. Для тех, у кого всё же развивается рак, детальное молекулярное профилирование помогает выбирать между эндоскопической терапией, операцией, химиотерапией, таргетными препаратами и иммунотерапией. Много работы ещё предстоит, чтобы сделать раннее выявление доступным для всех и бороться с лекарственной устойчивостью, но складывающаяся картина — это прогресс: движение от универсальных подходов к вмешательствам, лучше соответствующим времени, менее инвазивным и более точно ориентированным на биологию опухоли каждого пациента.
Цитирование: Zhang, S., Shen, Y., Zhu, L. et al. Esophageal cancer: from pathogenesis to precision therapies. Sig Transduct Target Ther 11, 134 (2026). https://doi.org/10.1038/s41392-026-02614-7
Ключевые слова: рак пищевода, пищевод Барретта, скрининг рака, микроокружение опухоли, иммунотерапия