Clear Sky Science · ar
سرطان المريء: من الآلية المرضية إلى العلاجات الدقيقة
لماذا يهمك هذا السرطان
يصيب سرطان المريء الأنبوب الذي ينقل الطعام من الفم إلى المعدة، ويعد من أكثر سرطانات الجهاز الهضمي فتكا في العالم. وبما أن المرض المبكر غالبا ما يسبب أعراضاً قليلة أو لا يسبب أعراضاً إطلاقاً، يُشخَّص كثير من الناس فقط عندما تصبح عملية البلع صعبة بالفعل وتصبح خيارات العلاج محدودة. تجمع هذه المراجعة ما يعرفه العلماء الآن عن كيفية بدء سرطان المريء وكيفية نموه، وكيف يتعلم الأطباء اكتشافه مبكراً ومعالجته بطرق أكثر تخصيصاً قد تُحسّن البقاء على المدى الطويل.
نوعان رئيسيان من السرطان، ومخاطر متعددة
ينقسم سرطان المريء فعلاً إلى شكلين رئيسيين. الأول، المسمى سرطان الخلايا الحرشفية، يميل إلى النشوء في الجزء الأوسط والعلوي من المريء وهو شائع بشكل خاص في أجزاء من آسيا وإفريقيا. ويرتبط بقوة بالتدخين، والاستهلاك المفرط للكحول، والمشروبات شديدة السخونة، وبعض المواد الحافظة في الطعام، وسوء التغذية. الثاني، الورم الغدي، يظهر عادة حيث يلتقي المريء بالمعدة ويشيع أكثر في البلدان الغربية. ويرتبط بالارتجاع الحمضي المزمن، وحالة تسمى مريء باريت حيث يتغير نسيج البطانة، وبالسمنة والتدخين. مجتمعة تسبب هذه السرطانات ما يقرب من نصف مليون وفاة عالمياً في عام 2022، ويتأثر الرجال بها أكثر بكثير من النساء.
من بطانة سليمة إلى ورم
يتطور كلا النوعين عبر رحلة تدريجية بدلاً من الظهور بين عشية وضحاها. في سرطان الخلايا الحرشفية، يمكن لسنوات من التهيج الناجم عن التبغ أو الكحول أو تعرضات أخرى أن تدفع الخلايا السطحية المسطحة للمريء عبر مراحل من السُمك، والنمو غير الطبيعي، وأخيراً السرطان الغازي. في الورم الغدي، يمكن للارتجاع المتكرر للعصارة الحمضية والصفراء أن يحول البطانة الطبيعية إلى نسيج باريت، الذي قد يتقدم بعد ذلك عبر تغيُّرات ما قبل السرطانية منخفضة وعالية الدرجة قبل أن يتحول إلى خبيث. على طول هذا المسار، تتراكم الخلايا على تلف في الحمض النووي، وتفقد حواجز أمان أساسية مثل جين الحارس TP53، وتكتسب نسخاً إضافية من جينات محفزة للنمو. يصف المؤلفون كيف تكشف أدوات "متعددة الأوميات" الحديثة، التي تقرأ الحمض النووي والحمض النووي الريبي والبروتينات والوسوم الكيميائية على الجينوم، خرائط مفصّلة لهذه التغيرات وتساعد في تمييز الآفات التي يحتمل أن تبقى مستقرة عن تلك التي هي مستعدة لأن تصبح سرطانية. 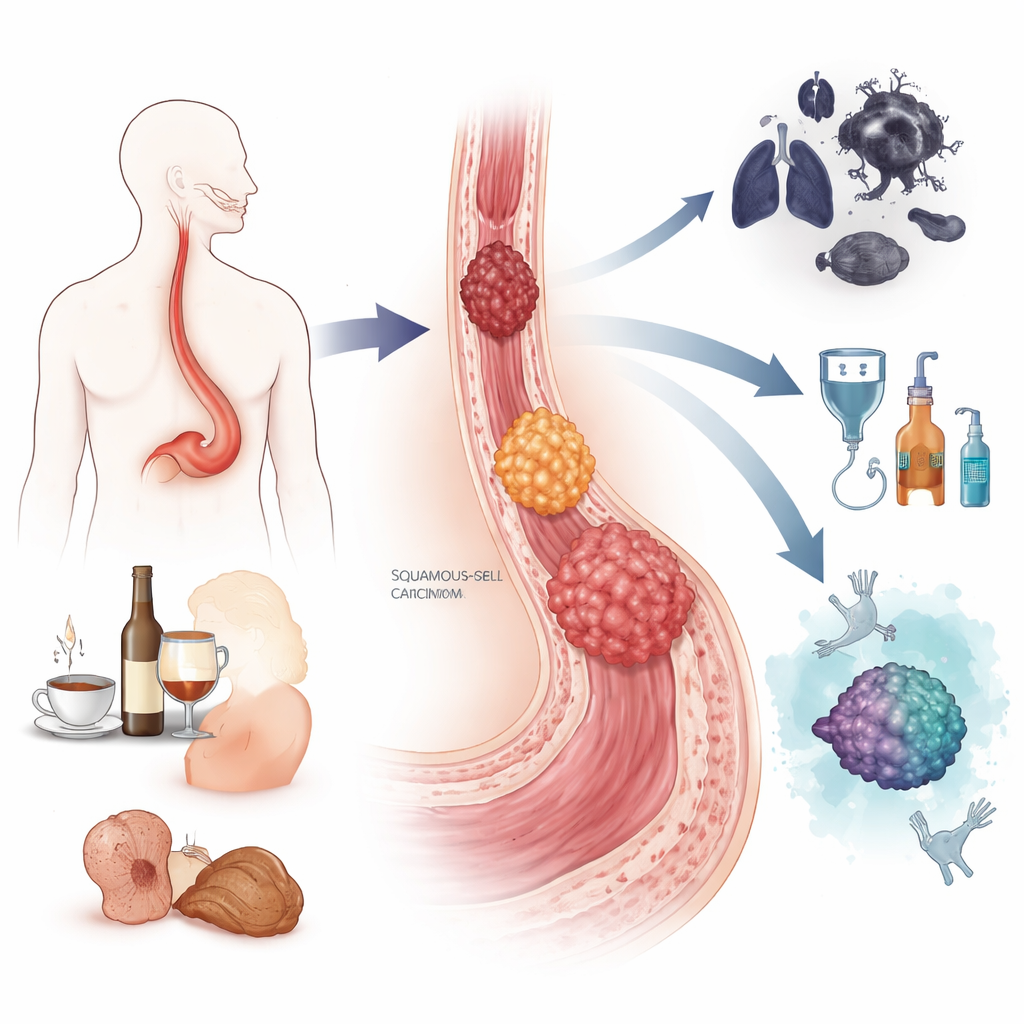
الحي المحيط بالورم
الخلايا السرطانية لا تتطور بمفردها: فهي تتواصل باستمرار مع محيطها. في المريء، تتفاعل الخلايا ما قبل السرطانية والسرطانية مع خلايا داعمة تسمى الأرومات الليفية، وخلايا مناعية يمكنها مهاجمة الأورام أو حمايتها، والأوعية الدموية، وحتى البكتيريا المقيمة. مع مرور الوقت، تُـ"مَــرن" الأرومات الليفية الطبيعية لتصبح أرومات ليفية مرتبطة بالسرطان تساعد على إعادة تشكيل النسيج، وبناء سقالة واقية حول الورم، وحمايته من العلاج الكيميائي والهجوم المناعي. في المراحل المبكرة، يمكن للخلايا المناعية أن تتعرف على الخلايا الشاذة وتدمرها، لكن مع تقدم الورم، غالباً ما يخلق بيئة أكثر كبحاً تمتلئ بخلايا تي منهكة وماكروفاجات متخصصة تُضعف الاستجابات المناعية المضادة للورم. قد تساهم التغيرات في الميكروبيوم المحلي، مثل التكاثر المفرط لبعض بكتيريا الفم، في تأجيج الالتهاب المزمن أو حتى تقليل فعالية الاستجابة للعلاج.
الوقاية، والكشف المبكر، والعلاج الأقل توغلاً
بما أن العديد من عوامل الخطر مرتبطة بنمط الحياة والبيئة، فإن للوقاية فعالية حقيقية. يمكن للإقلاع عن التدخين والحد من تناول الكحول أن يقللا بشكل كبير من خطر سرطان الخلايا الحرشفية مع مرور الوقت، بينما قد يحد التحكم في الوزن، وإدارة الارتجاع الحمضي، والنظم الغذائية الصحية الغنية بالفواكه والخضراوات من خطر الورم الغدي. في المناطق ذات المعدلات المرتفعة جداً، أظهرت برامج المنظار واسعة النطاق أن فحص بطانة المريء وإزالة الآفات ما قبل السرطانية يمكن أن يخفض الوفيات. تهدف أدوات جديدة لجعل الفحص أكثر راحة وتكلفة أقل: إسفنجات يُبتلعَت تجمع خلايا، وفحوصات دم تكشف أنماط مثيلة محددة للحمض النووي المسرطنة، وبروفايلات microRNA في اللعاب، وأنظمة ذكاء اصطناعي تساعد أطباء التنظير على رصد آفات صغيرة. عند اكتشافها مبكراً، يمكن الآن إزالة العديد من سرطانات المريء تقنياً عبر إجراءات منظارية أو معالجتها بالاستئصال الموجه، مما يجنّب المرضى جراحة كبرى ويقدم معدلات شفاء تتجاوز 90 بالمئة. 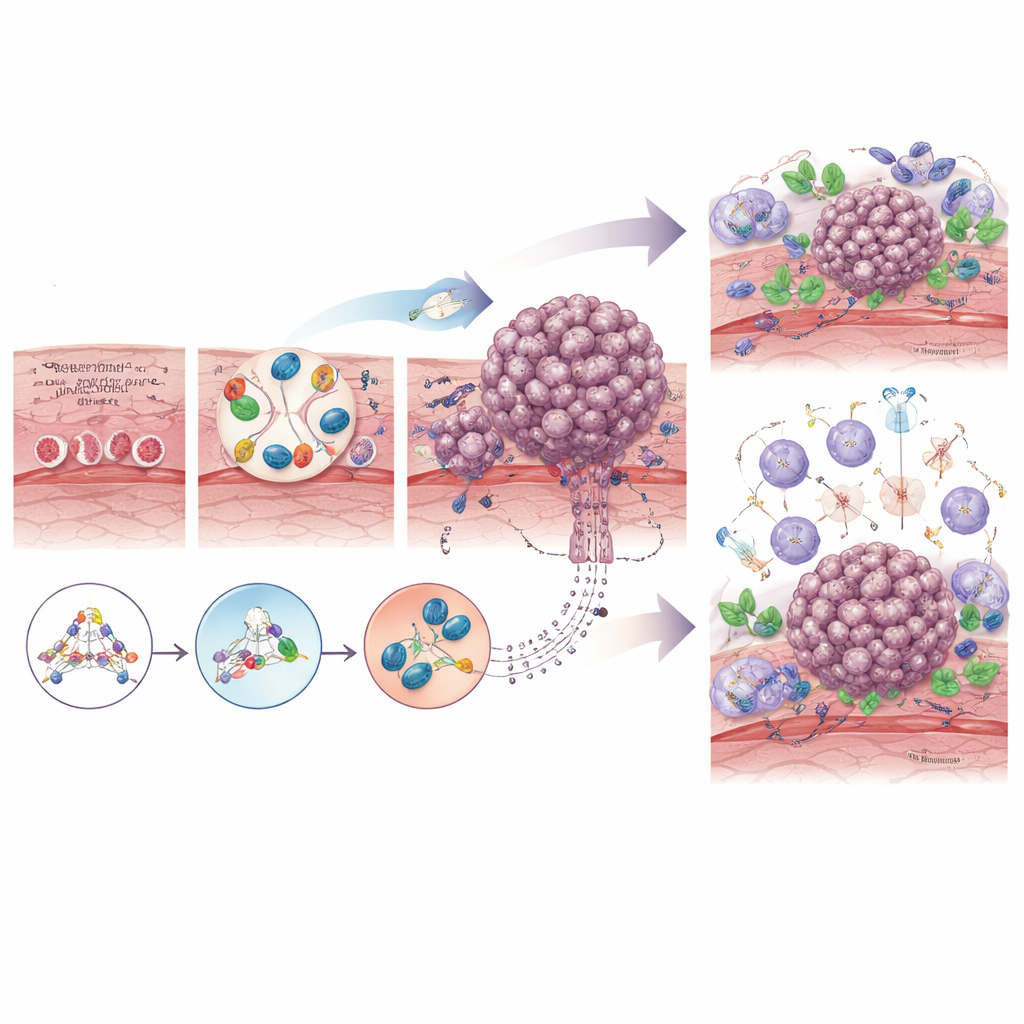
نحو علاجات دقيقة للأمراض المتقدمة
بالنسبة للأورام الأكثر تقدماً، يبقى العمود الفقري للعلاج الجراحة والعلاج الكيميائي والإشعاعي، لكن العلاج أصبح أكثر تخصيصاً. بعض الأورام الغدية تفرط في إنتاج مستقبلات محددة مثل HER2 أو VEGFR2، التي يمكن حجبها بأدوية مستهدفة تضاف إلى العلاج الكيميائي. في كلا النمطين الرئيسيين، حسّنَت مُثبِّطات نقاط التفتيش المناعية — أدوية ترفع الكوابح عن خلايا تي — من البقاء عندما تُستخدم مع العلاج الكيميائي أو بعد العلاج الكيميائي الإشعاعي والجراحة. يختبر الباحثون أيضاً تركيبات من العلاج المناعي مع الإشعاع أو العوامل المستهدفة، ويستكشفون نهجاً من الجيل التالي مثل خلايا CAR-T وخلايا تي المعدلة بمستقبلات TCR. وفي الوقت نفسه، يستخدمون البصمات الجينية والمناعية للتنبؤ بمن المرجح أن يستفيد وفهم سبب انتكاس الآخرين، بهدف التغلب على المقاومة.
ماذا يعني هذا للمرضى والمستقبل
تخلص المراجعة إلى أن سرطان المريء، الذي كان يُنظر إليه سابقاً على أنه تشخيص قاتم بشكل موحّد، يدخل عصر الوقاية والرعاية الأكثر دقة. من خلال توضيح كيفية تضافر التعرضات اليومية، والميل الوراثي، والتغيرات في البيئة الدقيقة لدفع تطور الأورام، بدأ العلماء في تحديد الأشخاص الأكثر عرضة للخطر قبل وقت طويل من ظهور الأعراض وتصميم أدوات فحص ملائمة لإعدادات مختلفة. بالنسبة لأولئك الذين يتطور لديهم السرطان، توجه التحاليل الجزيئية المفصّلة الاختيارات بين العلاج المنظاري، والجراحة، والعلاج الكيميائي، والأدوية المستهدفة، والعلاج المناعي. لا يزال ثمة الكثير من العمل لجعل الكشف المبكر متاحاً على نطاق واسع ولمواجهة مقاومة العلاج، لكن الصورة الناشئة هي صورة تقدم ثابت — الانتقال من نهج واحد يناسب الجميع نحو تدخلات مُؤقتة أفضل، وأقل توغلاً، وأكثر توافقاً مع بيولوجيا ورم كل شخص.
الاستشهاد: Zhang, S., Shen, Y., Zhu, L. et al. Esophageal cancer: from pathogenesis to precision therapies. Sig Transduct Target Ther 11, 134 (2026). https://doi.org/10.1038/s41392-026-02614-7
الكلمات المفتاحية: سرطان المريء, مريء باريت, فحص السرطان, البيئة الدقيقة للأورام, العلاج المناعي