Clear Sky Science · he
סרטן הוושט: ממנגנוני המחלה ועד טיפולים מותאמים
למה סרטן זה חשוב עבורך
סרטן הוושט פוגע בצינור שמוביל מזון מהפה לקיבה והוא נחשב לאחד הסוגים הקטלניים של מחלות העיכול בעולם. מאחר שהמחלה המוקדמת לעיתים גורמת למעט תסמינים או לא גורמת לתסמינים כלל, רבים מאובחנים רק כאשר כבר יש קושי בבליעה ואפשרויות הטיפול מוגבלות. סקירה זו מאחדת מה שמדענים יודעים כיום על איך סרטן הוושט מתחיל, איך הוא גדל, וכיצד הרופאים לומדים לזהותו מוקדם יותר ולהתאים את הטיפול בדרכים אישיות יותר שעשויות בסופו של דבר לשפר את ההישרדות.
שני סוגי סרטן עיקריים, סיכונים שונים
למעשה קיימים שני סוגים עיקריים של סרטן הוושט. אחד, הנקרא קרצינומה קשקשית, נוטה להופיע בחלק האמצעי והעליון של הוושט והוא שכיח במיוחד באזורים מסוימים באסיה ובאפריקה. הוא קשור במידה רבה לעישון, לשימוש מופרז באלכוהול, למשקאות חמים מאוד, לחומרי שימור מסוימים במזון ולתת‑תזונה. השני, אדנוקרצינומה, מופיע בדרך כלל במקום שבו הוושט פוגש את הקיבה ושכיח יותר במדינות המערב. היא קשורה בריפלוקס חומצי כרוני, במצב הקרוי וושט של בראוּט שבו הרירית משנה את אופייה, וכן בהשמנה ובעישון. יחד גרמו סוגי הסרטן הללו לכמעט חצי מיליון מקרי מוות ברחבי העולם בשנת 2022, וגברים נפגעים הרבה יותר מאשר נשים.
מרירית בריאה לגידול סרטני
שני סוגי הסרטן מתפתחים דרך שלבים סדירים ולא מופיעים בן לילה. בקרצינומה הקשקשית, שנות גירוי מעישון, אלכוהול או חשיפות אחרות יכולות לדחוף את תאי השכבה השטוחה של הוושט דרך שלבים של התרבות, גדילה בלתי נורמלית ולבסוף סרטן חודר. באדנוקרצינומה, ריפלוקס חוזר של חומצה ומרה יכול להפוך את הרירית הנורמלית לרקמת בראוּט, שיכולה להתקדם לשינויים טרום‑נאופלסטיים בדרגות נמוכה וגבוהה לפני הטרנספורמציה לממאירות. לאורך מסלול זה, תאים צוברים נזק ל‑DNA, מאבדים מנגנוני הגנה מרכזיים כמו הגן השומר TP53, וצוברים העתקים נוספים של גנים המקדמים גדילה. הכותבים מתארים כיצד כלים מודרניים של "מולטי‑אומיקס", שקוראים DNA, RNA, חלבונים ותוויות כימיות על הגנום, מגלים מיפויים מפורטים של שינויים אלה ועוזרים להבחין בין נגעים שסביר שיישארו יציבים לבין אלו שמועדות להפוך לסרטניות. 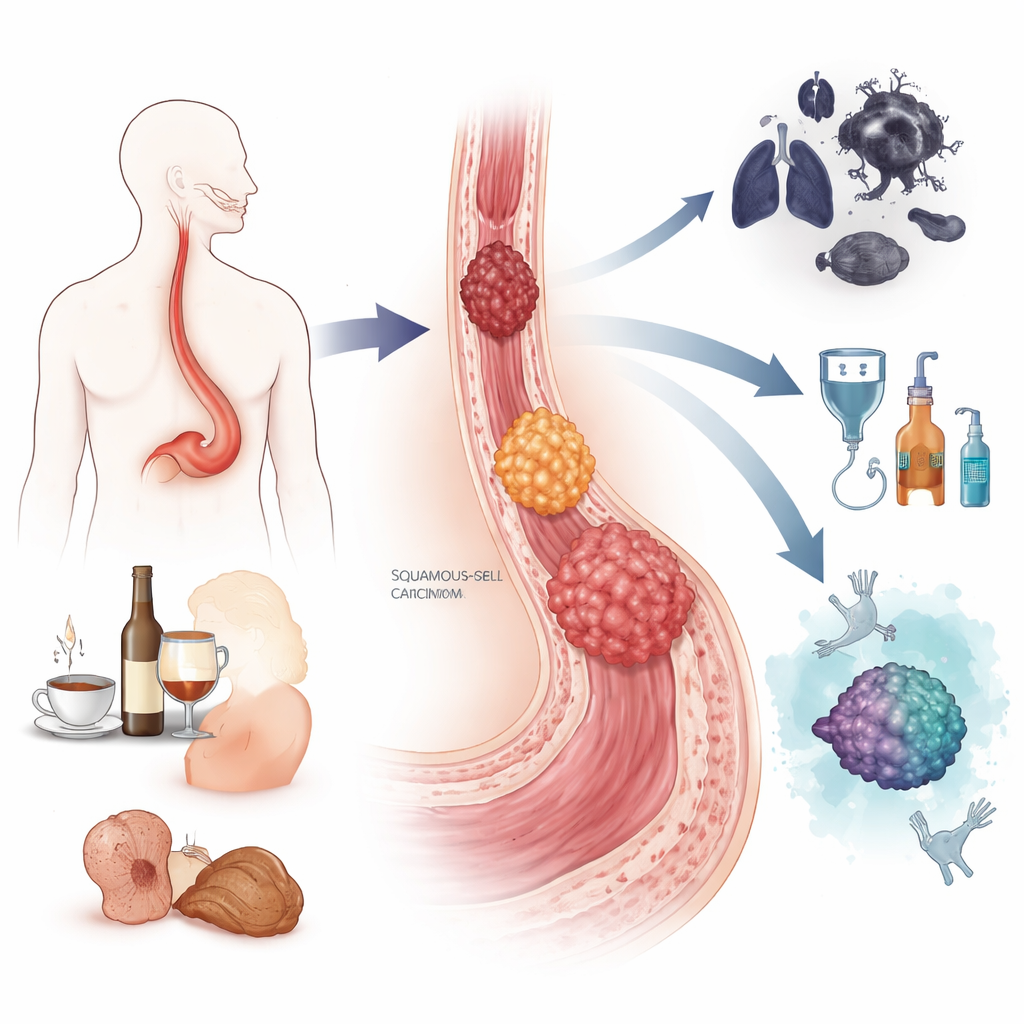
השכונה סביב הגידול
תאי הסרטן אינם מתפתחים לבד: הם מתקשרים כל הזמן עם סביבתם. בוושט, תאים טרום‑סרטניים וסרטניים מתקשרים עם תאי תמיכה שנקראים פיברובלסטים, תאי מערכת חיסון שיכולים לתקוף או להגן על הגידול, כלי דם, ואף חיידקים מקומיים. עם הזמן, פיברובלסטים נורמליים "מחונכים" להפוך לפיברובלסטים קשורים לסרטן שעוזרים לשקם רקמה, לבנות מעין שלד מגן סביב הגידול ולמגן אותו מפני כימותרפיה ומתקיפת מערכת החיסון. בשלבים המוקדמים, תאי חיסון יכולים לזהות ולהשמיד תאים בלתי‑נורמליים, אך ככל שהגידול מתקדם הוא לעתים יוצר סביבה מדכאת יותר המלאה בתאי T מותשים ומאקרופאגים מיוחדים שממעיטים את התגובה נגד הגידול. שינויים במיקרוביום המקומי, כמו גידול יתר של חיידקים מסוימים מהפה, עשויים עוד להסית דלקת כרונית או אפילו להחליש תגובה לטיפול.
מניעה, גילוי מוקדם וטיפול פחות פולשני
מכיוון שרבים מגורמי הסיכון קשורים לאורח חיים וסביבה, למניעה יש כוח ממשי. הפסקת עישון והגבלת צריכת אלכוהול יכולות להפחית משמעותית את הסיכון לקרצינומה קשקשית לאורך זמן, בעוד שליטה במשקל, ניהול ריפלוקס חומצי ותזונה בריאה עשירה בפירות וירקות עשויים להקטין את הסיכון לאדנוקרצינומה. באזורים עם שיעורי תחלואה גבוהים הראו תוכניות אנדוסקופיה בהיקפים גדולים שצפייה ישירה ברירית הוושט והסרת נגעים טרום‑סרטניים יכולים להוריד את שיעורי התמותה. כלים חדשים שואפים להפוך סקרינג לנוח וזול יותר: ספוגים ניתנים לבליעה שאוספים תאים, בדיקות דם שמזהות דפוסי מתילציה ספציפיים ל‑DNA סרטני, פרופילים של microRNA ברוק, ומערכות בינה מלאכותית שעוזרות לרופאי אנדוסקופיה לזהות נגעים זעירים. כשמזהים מוקדם, ניתן כיום להסיר הרבה סרטןי וושט בטכניקות אנדוסקופיות או לטפל בהם בכיבוי ממוקד, מה שמחליף ניתוחים גדולים ומציע שיעורי ריפוי מעל 90%. 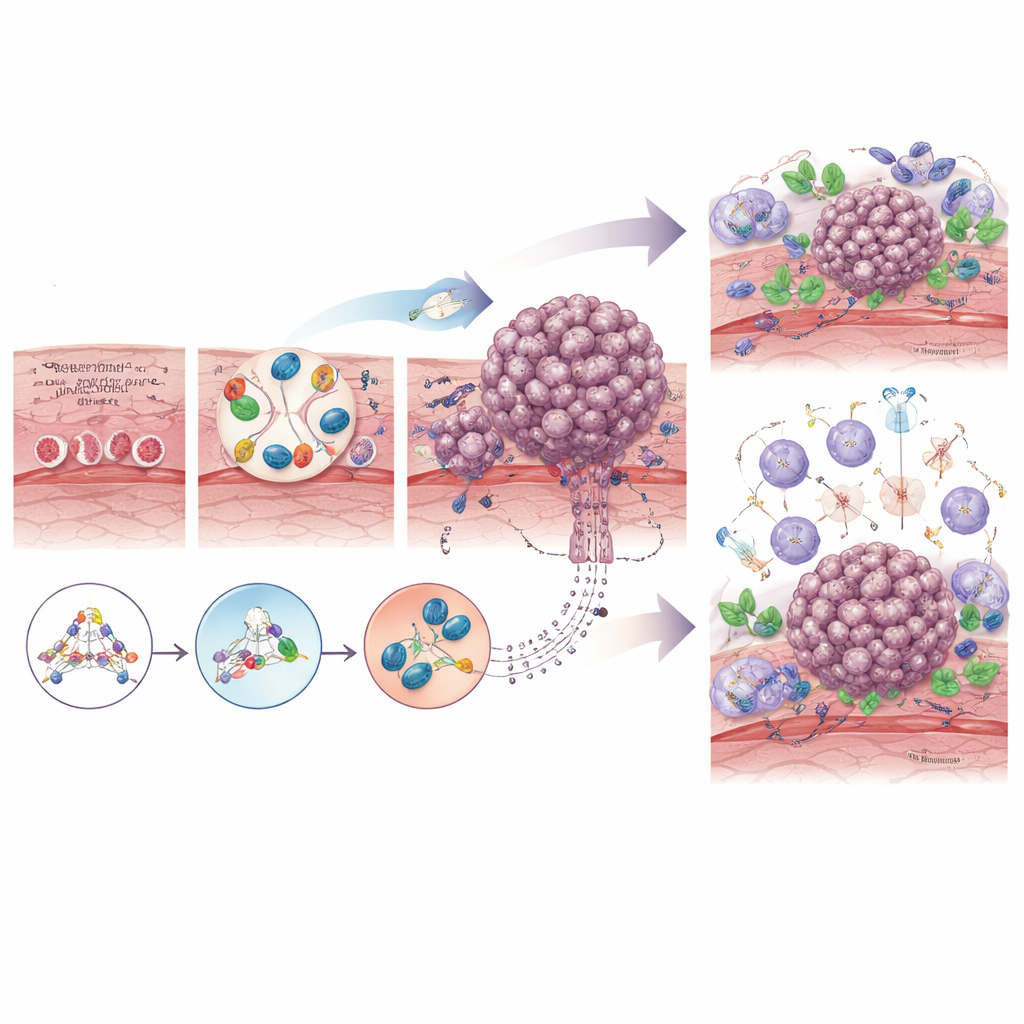
אל טיפול מדויק למחלה מתקדמת
לגידולים מתקדמים יותר, עמוד התווך הסטנדרטי נשאר ניתוח, כימותרפיה והקרנות, אך הטיפול נעשה הולך ומתאים אישית. חלק מהאדנוקרצינומות מפיקות בכמויות גבוהות קולטנים ספציפיים כמו HER2 או VEGFR2, שניתן לחסום באמצעות תרופות ממוקדות המתווספות לכימותרפיה. בשני הסוגים העיקריים, מעכבי נקודות בדיקה חיסוניות — תרופות שמשחררות את הבלמים על תאי T — שיפרו הישרדות כששולבו בכימותרפיה או ניתנו לאחר כימו‑רדיותרפיה וניתוח. חוקרים גם בוחנים שילובים של אימונותרפיה עם הקרנה או סוכנים ממוקדים, ובוחנים גישות מהדור הבא כמו תאי CAR‑T ותאי T מהונדסי‑TCR. במקביל משתמשים בחתימות גנטיות וחיסוניות כדי לחזות מי עתיד להפיק תועלת ולנסות להבין מדוע אחרים חוזרים עם המחלה, מתוך מטרה להתגבר על עמידות.
מה משמעות הדבר לחולים ולעתיד
הסקירה מסכמת כי סרטן הוושט, שבעבר נחשב לאבחנה פסימית ואחידה, נכנס לעידן של מניעה וטיפול מדויקים יותר. על‑ידי הבהרת האופן שבו חשיפות יומיומיות, נטיות תורשתיות ושינויים במיקרו‑הסביבה פועלים יחד כדי להניע גידולים, מדענים מתחילים לזהות אנשים בסיכון גבוה זמן רב לפני הופעת התסמינים ולעצב כלי סינון המתאימים לסביבות שונות. עבור אלה שפיתחו סרטן, פרופיל מולקולרי מפורט מנחה בחירה בין טיפול אנדוסקופי, ניתוח, כימותרפיה, תרופות ממוקדות ואימונותרפיה. נותר הרבה עבודה כדי להפוך גילוי מוקדם לנגיש בכל מקום ולפתור את בעיית העמידות לטיפול, אך התמונה המתבהרת היא של התקדמות מתמדת — מעבר לגישות אחידות לכיוון התערבויות שמתוזמנות טוב יותר, פחות פולשניות ומתאימות ביתר דיוק לביולוגיה של הגידול של כל אדם.
ציטוט: Zhang, S., Shen, Y., Zhu, L. et al. Esophageal cancer: from pathogenesis to precision therapies. Sig Transduct Target Ther 11, 134 (2026). https://doi.org/10.1038/s41392-026-02614-7
מילות מפתח: סרטן הוושט, וושט של בראוּט, סריקה לגילוי סרטן, מיקרו‑סביבת הגידול, אימונותרפיה