Clear Sky Science · sv
Endoplasmatiskt retikulum‑stress i sjukdomspatogenes: dess implikationer för behandling
När cellernas fabriker går fel
Varje cell i din kropp innehåller en liten fabrik kallad det endoplasmatiska retikulumet, eller ER, där de flesta proteiner viks till sina fungerande former. Denna översikt förklarar vad som händer när den fabriken blir överbelastad eller skadad — ett tillstånd som kallas ER‑stress — och hur det tyst bidrar till många stora sjukdomar, från cancer och hjärtsjukdom till Alzheimers, diabetes och autoimmuna sjukdomar. Att förstå detta dolda stressvar hjälper inte bara att förklara varför så olika sjukdomar delar vanliga drag som inflammation och cellförlust, utan pekar också på nya typer av behandlingar som finjusterar cellens egna reparationssystem.
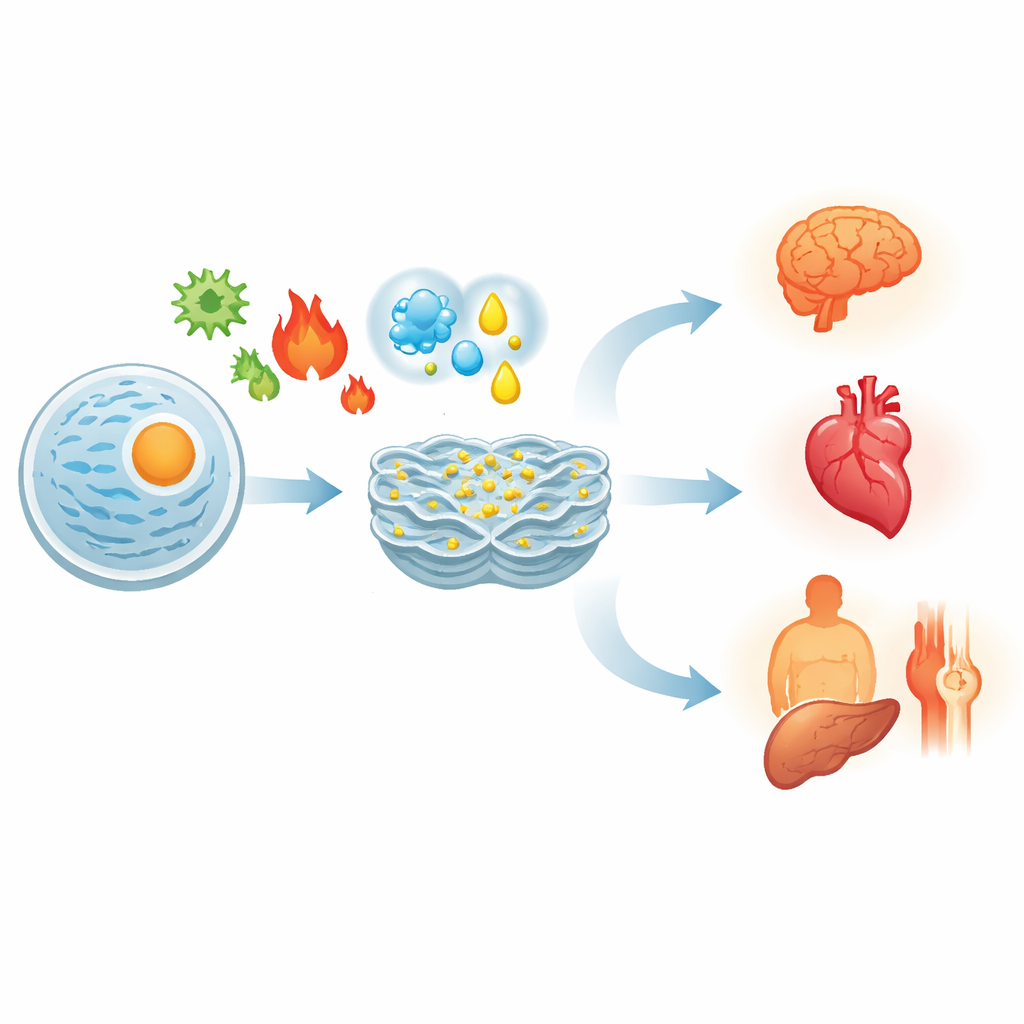
Hur celler känner av problem inuti
Proteiner tillverkas som sladdriga kedjor som måste vikas omsorgsfullt. Värme, syrebrist, överskott av näringsämnen, toxiner eller genetiska mutationer kan alla få missvikta proteiner att staplas upp i ER. För att hantera detta utlöser cellerna ett samordnat försvarsprogram kallat det ofullständiga veckningssvaret (UPR). Tre sensorproteiner inbäddade i ER‑membranet — IRE1, ATF6 och PERK — fungerar som larm som slår på när de känner av missvikta proteiner. Tillsammans bromsar de inflödet av nya proteiner, ökar produktionen av veckningshjälpare och kvalitetskontrollfaktorer, och förbättrar bortforslingen av defekta proteiner. Om detta svar lyckas återställs balansen och cellen överlever.
När anpassning blir skadlig
Samma säkerhetssystem kan bli skadligt när stressen är för intensiv eller varar för länge. Under kronisk belastning skiftar UPR från att vara skyddande till att driva cellerna mot självförstörelse. Pro‑dödsignaler aktiveras, reaktiva molekyler byggs upp och kommunikationen med andra delar av cellen, såsom mitokondrier, bryts ned. Denna långvariga ER‑stress kan döda sårbara celler direkt eller lämna överlevare förändrade på sätt som driver sjukdom — genom att ändra hur de växer, använder energi eller kommunicerar med immunsystemet. Översikten kartlägger dessa stegvisa förändringar och visar hur ER blir en kontrollpunkt för cellens öde, metabolism och inflammation.
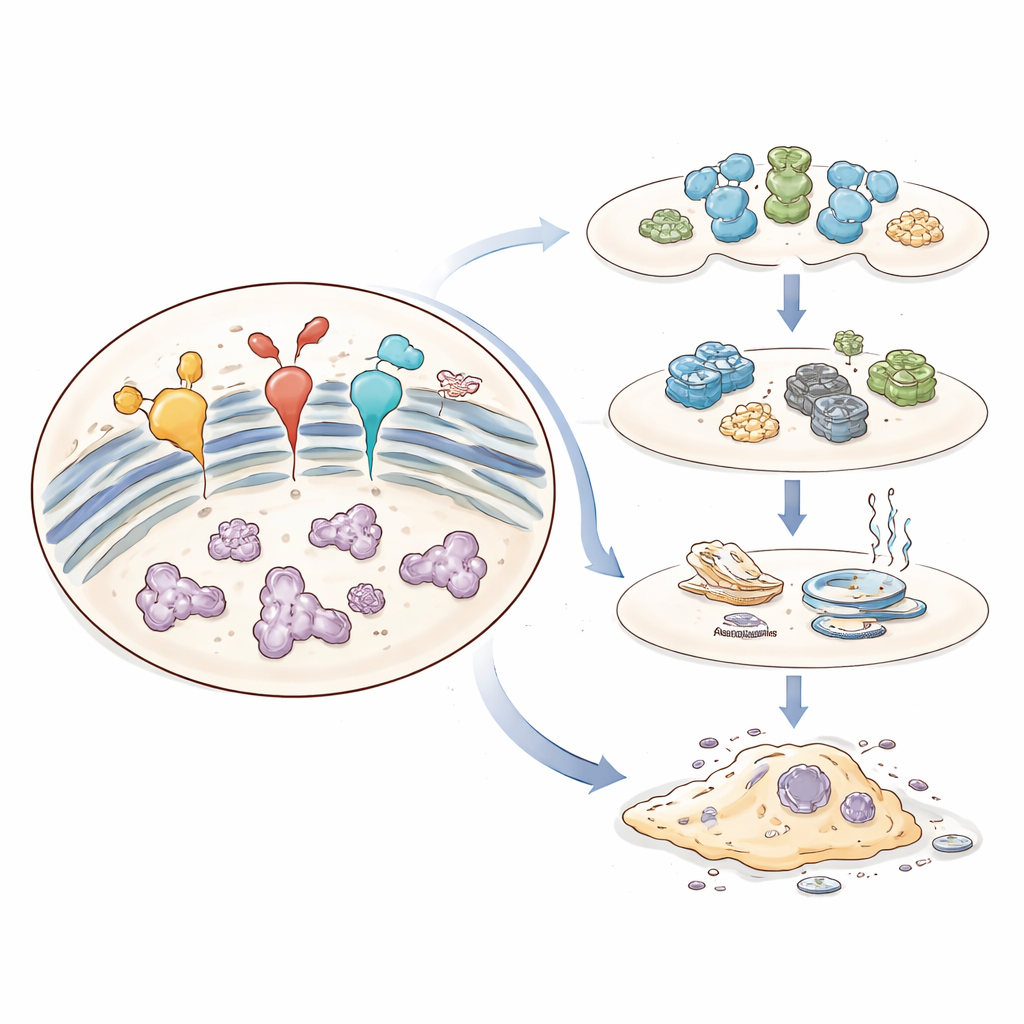
En gemensam tråd i många sjukdomar
Eftersom alla organ är beroende av korrekt vikta proteiner visar sig ER‑stress i mycket olika tillstånd. I cancer lever tumörceller på gränsen till konstant ER‑stress på grund av snabb tillväxt och dålig blodtillförsel. De utnyttjar UPR för att fortsätta dela sig och undkomma immunsvar, men kan tvingas in i död om stressen ytterligare ökas. I hjärtat och blodkärlen bidrar ER‑stress till tilltäppta artärer, skador efter hjärtinfarkt och hjärtsvikt genom att skada muskel‑ och kärlceller. I hjärnan kopplas det till de giftiga proteinklumpar som ses vid Alzheimers, Parkinsons och Huntingtons sjukdom och till den gradvisa förlusten av neuroner. Vid fetma och typ 2‑diabetes stör ER‑stress i levern, fettväven och bukspottkörteln insulinets verkan och hormonsekretion, vilket främjar högt blodsocker. Vid autoimmuna sjukdomar som reumatoid artrit eller inflammatorisk tarmsjukdom förstärker ER‑stress i immunceller och barriärceller inflammation och vävnadsskada.
Att vända en svaghet till ett mål
Eftersom ER‑stress ligger i korsningen för så många vägar erbjuder det flera ingångspunkter för terapi. Läkemedelstillverkare har designat molekyler som antingen dämpar överaktiva stressignaler eller medvetet förstärker dem i cancerceller för att utlösa deras död. Vissa föreningar riktar sig mot de tre huvudsensorerna; andra boostar veckningshjälpare som GRP78, förbättrar borttagningen av felaktiga proteiner eller skyddar mitokondrier. Översikten listar också tidiga kliniska prövningar av befintliga läkemedel — såsom gallsyraderivat, diabetesmedel och kolesterolsänkande preparat — som tycks lätta ER‑stress hos människor. Samtidigt utvecklas nya verktyg som fluorescerande prober, nanogeler och experimentella cancervacciner för att mer precist spåra eller manipulera ER‑stress i tumörer och andra vävnader.
Vägen framåt för ER‑baserade behandlingar
Författarna drar slutsatsen att ER‑stress både är en tidig drivkraft och en bestående kraft i många kroniska sjukdomar. Eftersom UPR dock kan hjälpa eller skada beroende på dos och timing måste framtida behandlingar finjusteras snarare än enkelt slås på eller av. Bättre djurmodeller som kombinerar flera sjukdomstillstånd, tillsammans med omics‑tekniker som mäter stressignaler över hela organ, bör klargöra när intervention är fördelaktig. Om dessa utmaningar kan övervinnas kan terapier som återbalanserar cellens interna fabrik komplettera befintliga läkemedel och erbjuda nya sätt att bromsa cancer, skydda hjärta och hjärna, förbättra metabolismen och dämpa felriktade immunsvar.
Citering: Wei, S., Zhang, N., Zhang, H. et al. Endoplasmic reticulum stress in disease pathogenesis: its implications for therapy. Sig Transduct Target Ther 11, 136 (2026). https://doi.org/10.1038/s41392-026-02600-z
Nyckelord: endoplasmatiskt retikulum‑stress, ofullständigt veckningssvar, cancerterapi, neurodegenerativ sjukdom, metabola störningar