Clear Sky Science · fr
Stress du réticulum endoplasmique dans la pathogenèse des maladies : implications pour la thérapie
Quand les usines cellulaires déraillent
Chaque cellule de votre corps contient une petite « usine » appelée réticulum endoplasmique, ou RE, où la plupart des protéines sont repliées pour acquérir leur forme fonctionnelle. Cette revue explique ce qui se passe lorsque cette usine est surchargée ou endommagée — un état connu sous le nom de stress du RE — et comment il contribue discrètement à de nombreuses maladies majeures, du cancer et des maladies cardiaques à Alzheimer, le diabète et les maladies auto‑immunes. Comprendre cette réponse au stress cachée aide non seulement à expliquer pourquoi des maladies si différentes partagent des traits communs comme l’inflammation et la perte cellulaire, mais pointe aussi vers de nouveaux types de traitements qui ajustent finement les propres systèmes de réparation de la cellule.
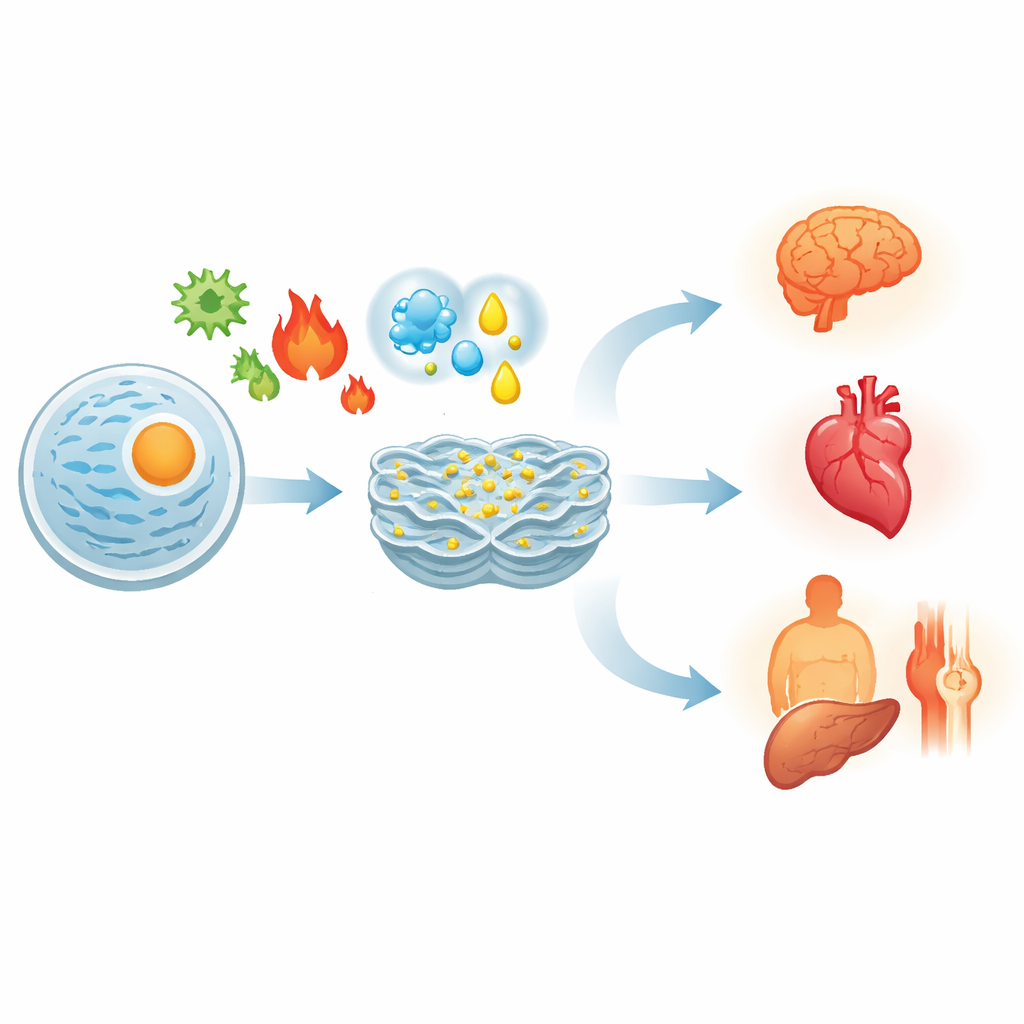
Comment les cellules détectent les problèmes à l’intérieur
Les protéines sont synthétisées sous forme de chaînes souples qui doivent être repliées avec soin. La chaleur, le manque d’oxygène, un excès de nutriments, des toxines ou des mutations génétiques peuvent tous provoquer l’accumulation de protéines mal repliées dans le RE. Pour y faire face, les cellules déclenchent un programme de défense coordonné appelé réponse aux protéines mal repliées (UPR en anglais). Trois protéines détectrices intégrées dans la membrane du RE — IRE1, ATF6 et PERK — agissent comme des alarmes qui s’activent lorsqu’elles perçoivent des protéines mal repliées. Ensemble, elles ralentissent l’arrivée de nouvelles protéines, augmentent la production d’assistants de repliement et de facteurs de contrôle de qualité, et renforcent l’élimination des protéines défectueuses. Si cette réponse réussit, l’équilibre est rétabli et la cellule survit.
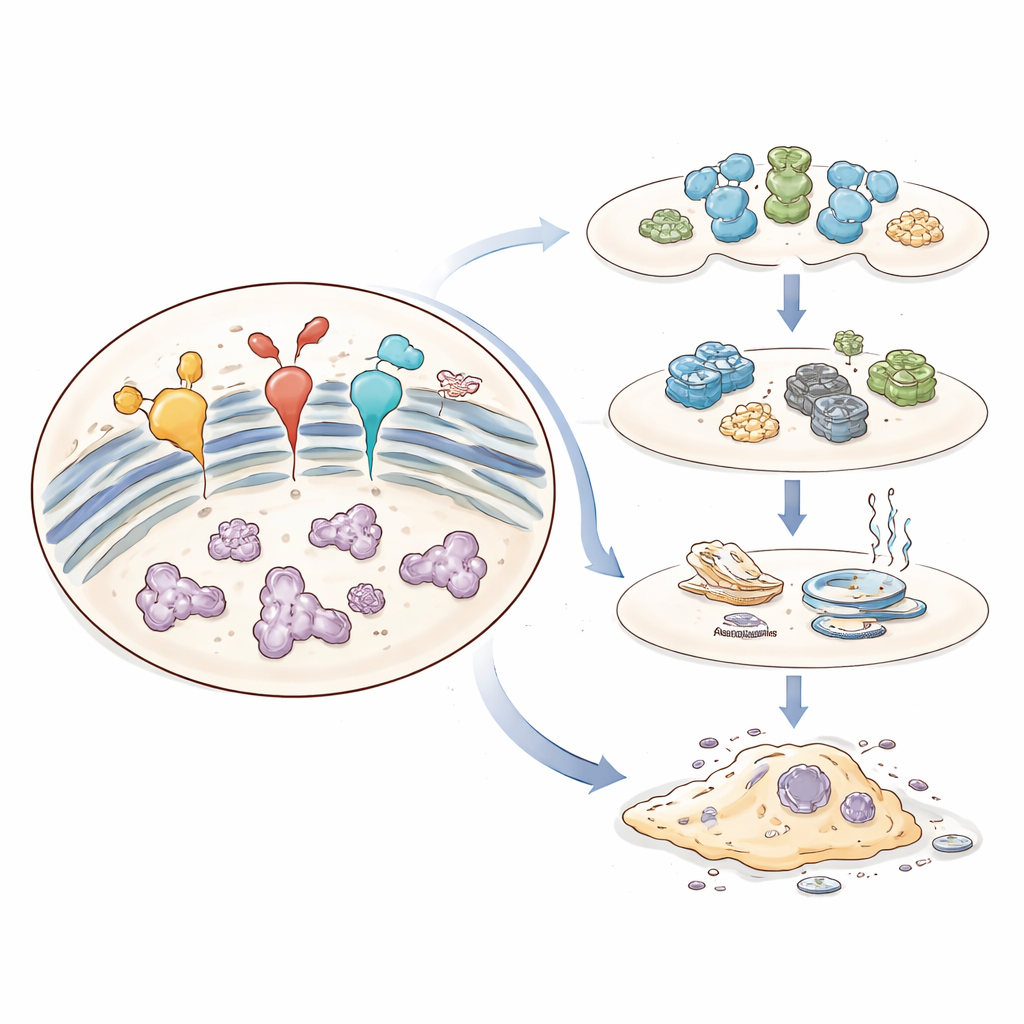
Quand l’adaptation tourne au dommage
Le même système de sécurité peut devenir délétère lorsque le stress est trop intense ou trop prolongé. Sous une pression chronique, l’UPR passe d’un mode protecteur à un mode qui pousse la cellule vers l’autodestruction. Des signaux pro‑mort sont activés, des molécules réactives s’accumulent, et la communication avec d’autres compartiments cellulaires comme les mitochondries se détériore. Ce stress prolongé du RE peut tuer directement les cellules vulnérables ou laisser des survivants modifiés d’une manière qui favorise la maladie — en changeant leur croissance, leur utilisation de l’énergie ou leur manière de dialoguer avec le système immunitaire. La revue retrace ces changements étape par étape, montrant comment le RE devient un centre de contrôle du destin cellulaire, du métabolisme et de l’inflammation.
Un fil conducteur commun à de nombreuses maladies
Parce que tous les organes dépendent d’un repliement protéique correct, le stress du RE apparaît dans des contextes très variés. Dans les cancers, les cellules tumorales vivent au bord d’un stress RE constant en raison de leur croissance rapide et d’un apport sanguin insuffisant. Elles exploitent l’UPR pour continuer à se diviser et échapper à l’attaque du système immunitaire, mais peuvent être poussées vers la mort si le stress est encore aggravé. Dans le cœur et les vaisseaux, le stress du RE contribue à l’obstruction des artères, aux lésions après un infarctus et à l’insuffisance cardiaque en endommageant les cellules musculaires et vasculaires. Dans le cerveau, il est associé aux amas protéiques toxiques observés dans la maladie d’Alzheimer, la maladie de Parkinson et la maladie de Huntington, ainsi qu’à la perte progressive de neurones. Dans l’obésité et le diabète de type 2, le stress du RE dans le foie, le tissu adipeux et le pancréas perturbe l’action de l’insuline et la sécrétion hormonale, favorisant l’hyperglycémie. Dans les maladies auto‑immunes telles que la polyarthrite rhumatoïde ou les maladies inflammatoires de l’intestin, le stress du RE dans les cellules immunitaires et les cellules de barrière amplifie l’inflammation et les lésions tissulaires.
Transformer une faiblesse en cible
Parce que le stress du RE se situe au carrefour de tant de voies, il offre de multiples points d’entrée thérapeutiques. Les industriels ont conçu des molécules qui atténuent les signaux de stress hyperactifs ou, au contraire, les amplifient délibérément dans les cellules tumorales pour déclencher leur mort. Certains composés visent les trois détecteurs principaux ; d’autres renforcent les chaperons protéiques tels que GRP78, améliorent l’élimination des protéines défectueuses ou protègent les mitochondries. La revue recense aussi des essais cliniques précoces d’agents existants — comme des dérivés d’acides biliaires, des médicaments contre le diabète et des hypolipémiants — qui semblent alléger le stress du RE chez l’humain. Parallèlement, de nouveaux outils tels que des sondes fluorescentes, des nanogels et des vaccins anticancéreux expérimentaux sont développés pour suivre ou manipuler plus précisément le stress du RE au sein des tumeurs et d’autres tissus.
La voie à suivre pour des traitements ciblant le RE
Les auteurs concluent que le stress du RE est à la fois un moteur précoce et une force de maintien dans de nombreuses maladies chroniques. Toutefois, parce que l’UPR peut aider ou nuire selon la dose et le timing, les traitements futurs devront être finement ajustés plutôt que simplement activés ou désactivés. De meilleurs modèles animaux combinant plusieurs pathologies, ainsi que des technologies « omiques » mesurant les signaux de stress à l’échelle des organes, devraient clarifier quand une intervention sera bénéfique. Si ces défis sont relevés, des thérapies visant à rééquilibrer la « usine » interne de la cellule pourraient compléter les médicaments existants, offrant de nouvelles voies pour ralentir le cancer, protéger le cœur et le cerveau, améliorer le métabolisme et apaiser les réponses immunitaires mal dirigées.
Citation: Wei, S., Zhang, N., Zhang, H. et al. Endoplasmic reticulum stress in disease pathogenesis: its implications for therapy. Sig Transduct Target Ther 11, 136 (2026). https://doi.org/10.1038/s41392-026-02600-z
Mots-clés: stress du réticulum endoplasmique, réponse aux protéines mal repliées, thérapie contre le cancer, maladie neurodégénérative, troubles métaboliques