Clear Sky Science · it
Stress del reticolo endoplasmatico nella patogenesi delle malattie: implicazioni per la terapia
Quando le fabbriche cellulari vanno in avaria
Ogni cellula del corpo contiene una piccola «fabbrica» chiamata reticolo endoplasmatico, o RE, dove la maggior parte delle proteine viene ripiegata nelle forme funzionali. Questa review spiega cosa accade quando quella fabbrica è sovraccarica o danneggiata — uno stato noto come stress del RE — e come ciò contribuisca silenziosamente a molte malattie importanti, dal cancro e dalle patologie cardiache all’Alzheimer, al diabete e ai disturbi autoimmuni. Comprendere questa risposta allo stress nascosta non solo aiuta a spiegare perché malattie così diverse condividano caratteristiche comuni come infiammazione e perdita cellulare, ma indica anche nuovi approcci terapeutici che modulano i sistemi di riparazione intrinseci della cellula.
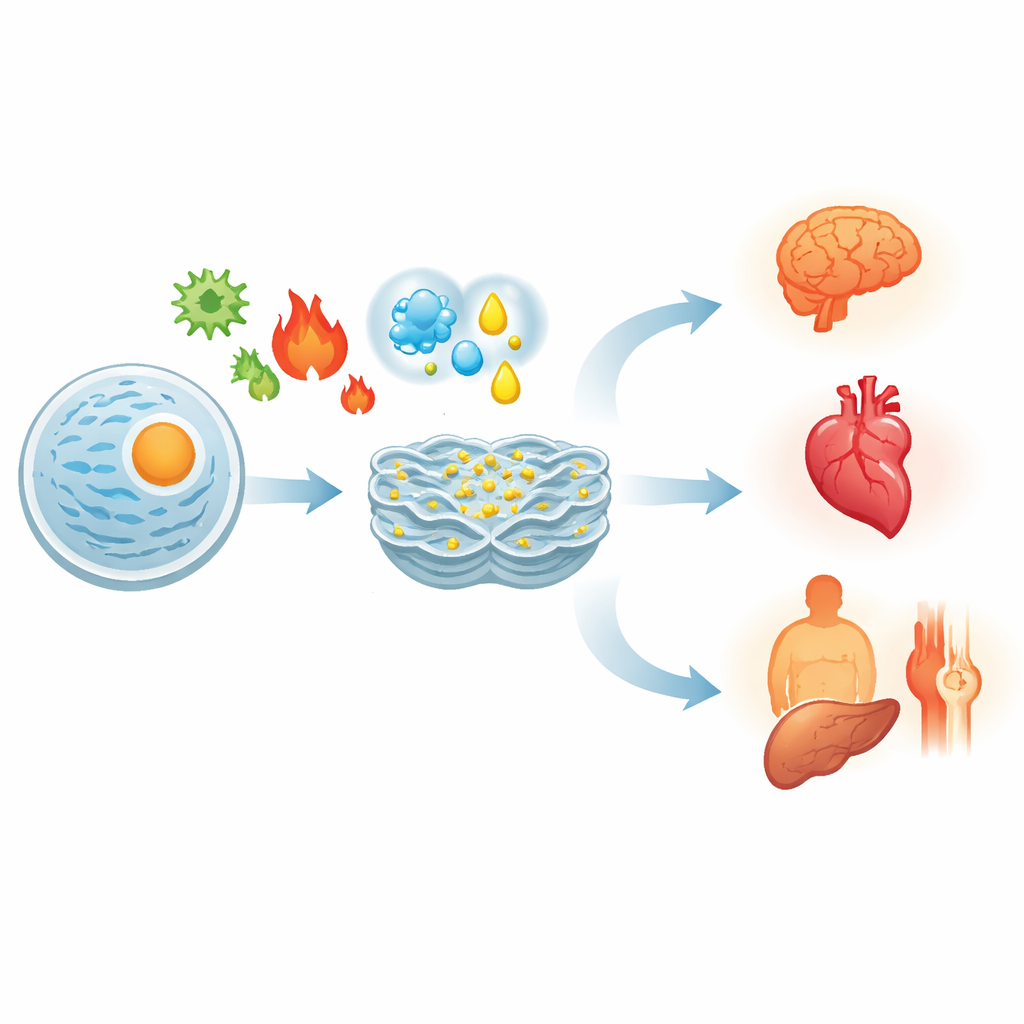
Come le cellule percepiscono i guai interni
Le proteine vengono sintetizzate come catene flessibili che devono essere ripiegate con cura. Calore, mancanza di ossigeno, eccesso di nutrienti, tossine o mutazioni genetiche possono tutti causare l’accumulo di proteine mal ripiegate nel RE. Per far fronte a ciò, le cellule attivano un programma di difesa coordinato chiamato risposta alle proteine non ripiegate (UPR). Tre proteine sensore incastonate nella membrana del RE — IRE1, ATF6 e PERK — funzionano come allarmi che si attivano quando rilevano proteine mal ripiegate. Insieme rallentano l’afflusso di nuove proteine, aumentano la produzione di chaperoni e fattori di controllo qualità e potenziano lo smaltimento delle proteine difettose. Se questa risposta ha successo, l’equilibrio viene ripristinato e la cellula sopravvive.
Quando l’adattamento si trasforma in danno
Lo stesso sistema di sicurezza può diventare dannoso quando lo stress è troppo intenso o perdura nel tempo. Sotto pressione cronica, l’UPR passa dall’essere protettiva a spingere le cellule verso l’autodistruzione. Segnali pro‑morte vengono attivati, si accumulano molecole reattive e la comunicazione con altre parti cellulari come i mitocondri si deteriora. Questo stress prolungato del RE può uccidere le cellule più vulnerabili o lasciare sopravvissuti alterati in modi che favoriscono la malattia — cambiando il loro modo di crescere, utilizzare energia o interagire con il sistema immunitario. La review traccia questi cambiamenti passo dopo passo, mostrando come il RE diventi un centro di controllo per il destino cellulare, il metabolismo e l’infiammazione.
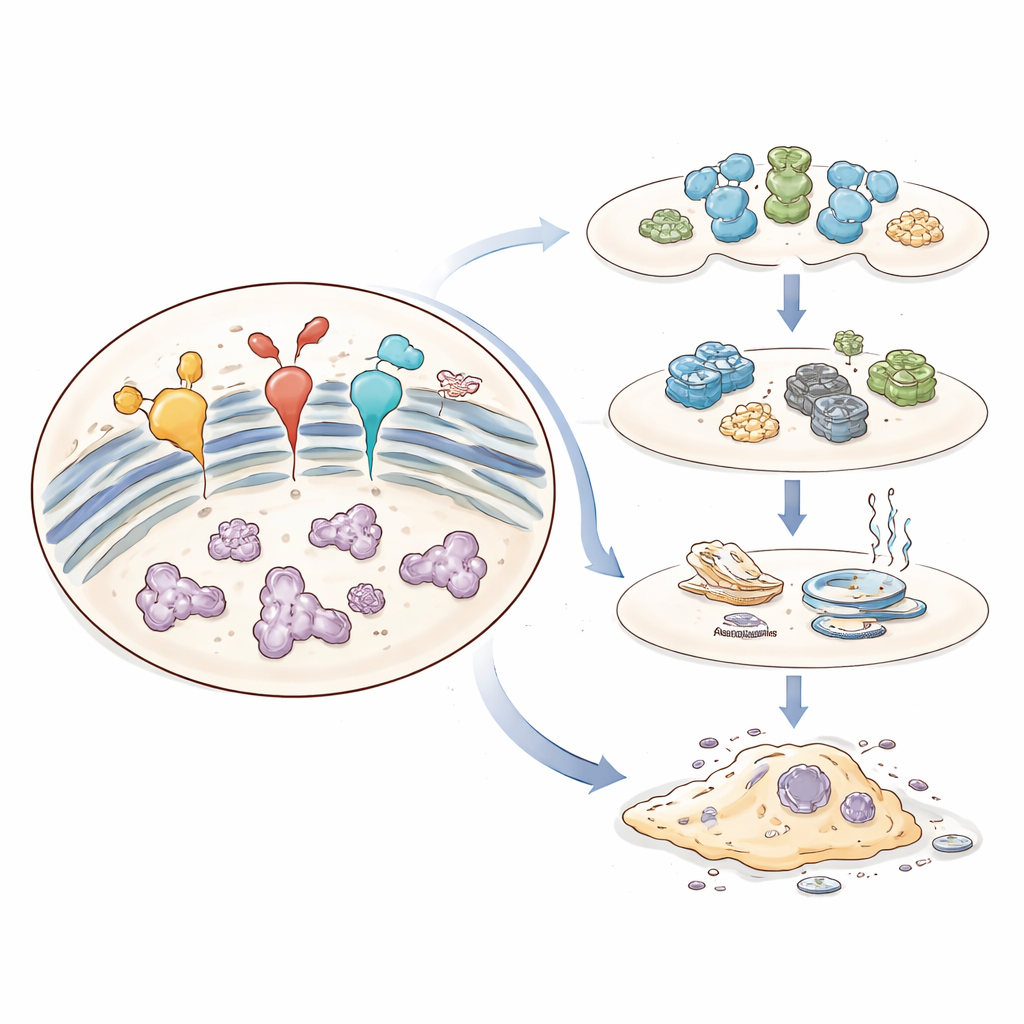
Un filo comune in molte malattie
Poiché tutti gli organi dipendono da proteine correttamente ripiegate, lo stress del RE compare in condizioni molto differenti. Nei tumori, le cellule neoplastiche vivono ai limiti di uno stress RE costante dovuto alla rapida crescita e al ridotto apporto di sangue. Sfruttano l’UPR per continuare a dividersi e sfuggire all’attacco immune, ma possono essere portate alla morte se lo stress viene ulteriormente aumentato. Nel cuore e nei vasi sanguigni, lo stress del RE contribuisce all’arteriosclerosi, al danno post‑infarto e all’insufficienza cardiaca danneggiando cellule muscolari e vascolari. Nel cervello è associato agli ammassi tossici di proteine osservati in Alzheimer, Parkinson e malattia di Huntington e alla progressiva perdita di neuroni. Nell’obesità e nel diabete di tipo 2, lo stress del RE nel fegato, nel tessuto adiposo e nel pancreas altera l’azione dell’insulina e la secrezione ormonale, alimentando l’iperglicemia. Nelle malattie autoimmuni come l’artrite reumatoide o le malattie infiammatorie intestinali, lo stress del RE nelle cellule immunitarie e nelle cellule di barriera amplifica l’infiammazione e il danno tissutale.
Trasformare una debolezza in un bersaglio
Poiché lo stress del RE sta all’incrocio di tanti percorsi, offre molteplici punti di ingresso per la terapia. Gli sviluppatori di farmaci hanno ideato molecole che abbassano segnali di stress iperattivi o che li esagerano deliberatamente nelle cellule tumorali per indurne la morte. Alcuni composti mirano ai tre sensori principali; altri potenziano i chaperoni come GRP78, migliorano la rimozione delle proteine difettose o proteggono i mitocondri. La review cataloga anche trial clinici iniziali con farmaci esistenti — come derivati degli acidi biliari, farmaci per il diabete e agenti ipocolesterolemizzanti — che sembrano ridurre lo stress del RE nelle persone. Allo stesso tempo, nuovi strumenti come sonde fluorescenti, nanogel e vaccini antitumorali sperimentali vengono sviluppati per monitorare o manipolare lo stress del RE con maggiore precisione all’interno dei tumori e di altri tessuti.
La strada da percorrere per terapie basate sul RE
Gli autori concludono che lo stress del RE è sia un motore precoce sia una forza di mantenimento in molte malattie croniche. Tuttavia, poiché l’UPR può aiutare o danneggiare a seconda della dose e dei tempi, i futuri trattamenti devono essere finemente calibrati piuttosto che semplicemente attivati o disattivati. Modelli animali migliori che combinino più patologie, insieme alle tecnologie “omics” che misurano i segnali di stress nell’intero organo, dovrebbero chiarire quando l’intervento sarà utile. Se queste sfide verranno affrontate, le terapie che riequilibrano la «fabbrica» interna della cellula potrebbero integrare i farmaci esistenti, offrendo nuovi modi per rallentare il cancro, proteggere cuore e cervello, migliorare il metabolismo e placare risposte immunitarie disordinate.
Citazione: Wei, S., Zhang, N., Zhang, H. et al. Endoplasmic reticulum stress in disease pathogenesis: its implications for therapy. Sig Transduct Target Ther 11, 136 (2026). https://doi.org/10.1038/s41392-026-02600-z
Parole chiave: stress del reticolo endoplasmatico, risposta alle proteine non ripiegate, terapia antitumorale, malattie neurodegenerative, disturbi metabolici