Clear Sky Science · ru
Стресс эндоплазматического ретикулума в патогенезе заболеваний: его значение для терапии
Когда «заводы» клеток дают сбой
В каждой клетке вашего тела есть крошечная «фабрика» — эндоплазматический ретикулум (ЭР), где большинство белков сворачиваются в работоспособную форму. В этом обзоре объясняется, что происходит, когда эта фабрика перегружается или повреждается — состояние, известное как стресс ЭР — и как оно тихо способствует множеству серьёзных заболеваний, от рака и болезней сердца до болезни Альцгеймера, диабета и аутоиммунных расстройств. Понимание этой скрытой реакции на стресс помогает не только объяснить, почему такие разные болезни имеют общие черты, например воспаление и потерю клеток, но и указывает на новые подходы к лечению, которые тонко настраивают собственные системы восстановления клетки.
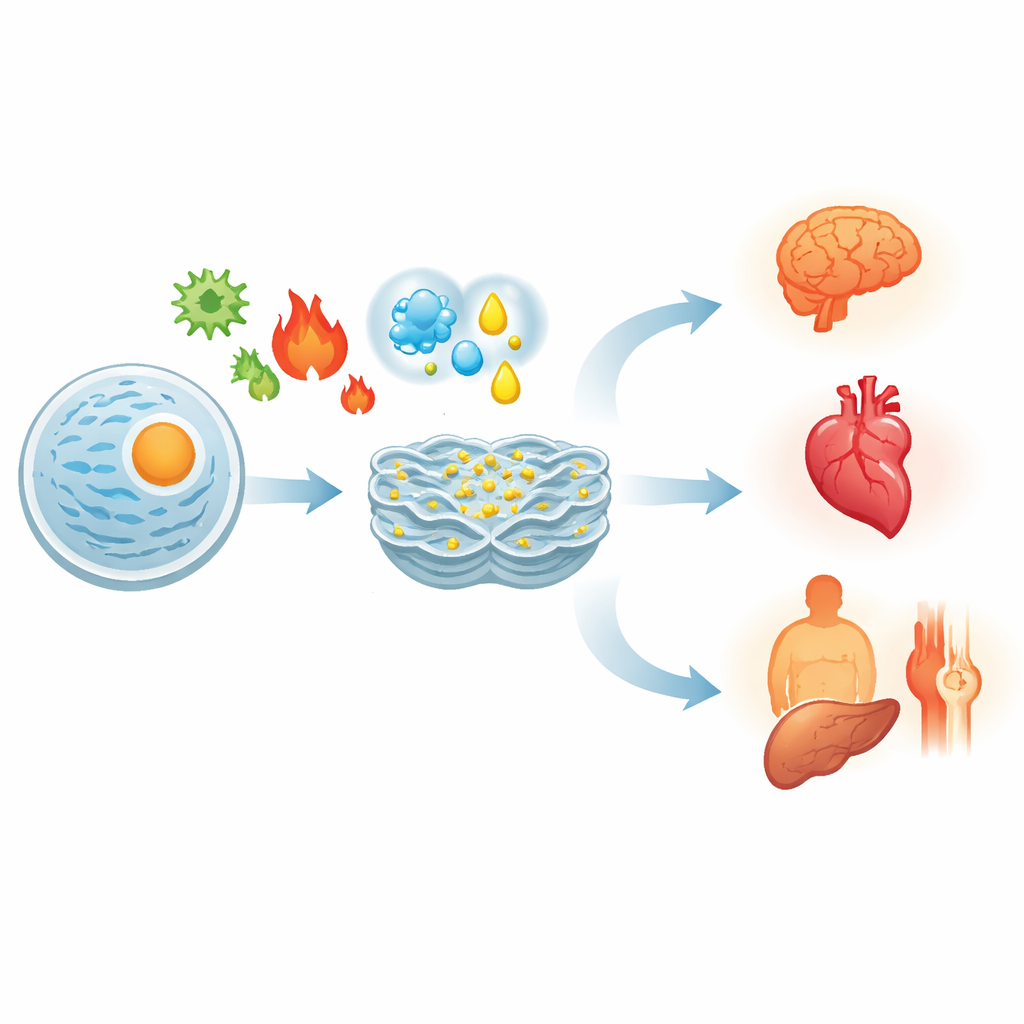
Как клетки ощущают внутренние проблемы
Белки синтезируются в виде гибких цепочек, которые должны аккуратно свернуться. Жар, недостаток кислорода, избыток питательных веществ, токсины или генетические мутации — всё это может привести к накоплению неправильно свернувшихся белков в ЭР. Чтобы справиться, клетки запускают скоординированную программу защиты, называемую ответом на накопление неправильно свернувшихся белков (UPR). Три сенсорных белка в мембране ЭР — IRE1, ATF6 и PERK — действуют как сигнализации, которые включаются при обнаружении сбоев в сворачивании. Вместе они замедляют приток новых белков, усиливают производство шаперонов и факторов контроля качества и увеличивают выведение дефектных белков. Если эта реакция удачна, равновесие восстанавливается, и клетка выживает.
Когда адаптация превращается в ущерб
Та же система безопасности может стать вредной, если стресс слишком силён или длится слишком долго. При хроническом давлении UPR смещается от защитной роли к стимуляции саморазрушения клеток. Включаются сигналы, ведущие к смерти, накапливаются реактивные молекулы, и нарушается связь с другими частями клетки, например митохондриями. Длительный стресс ЭР может либо убить уязвимые клетки, либо оставить выживших изменёнными таким образом, что это способствует заболеванию — изменяются их рост, использование энергии или взаимодействие с иммунной системой. Обзор прослеживает эти пошаговые изменения, показывая, как ЭР становится контрольным узлом для судьбы клетки, метаболизма и воспаления.
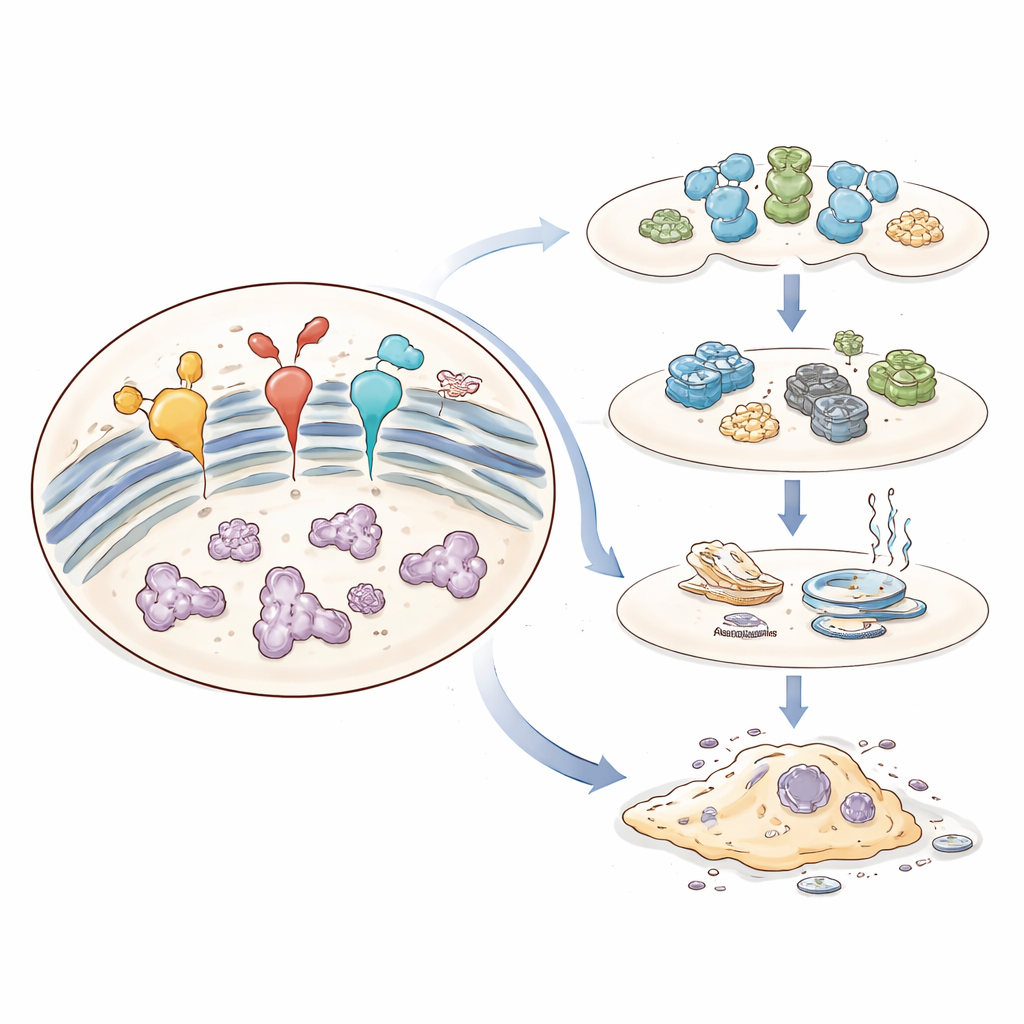
Общая нить в разных болезнях
Поскольку все органы зависят от правильно свернувшихся белков, стресс ЭР проявляется при самых разных состояниях. В опухолях клетки находятся на грани постоянного стресса ЭР из‑за быстрого роста и плохого кровоснабжения. Они используют UPR, чтобы продолжать делиться и уклоняться от атаки иммунной системы, но их можно подтолкнуть к гибели, если усилить стресс. В сердце и сосудах стресс ЭР способствует атеросклерозу, повреждению после инфаркта и сердечной недостаточности, повреждая мышечные и сосудистые клетки. В мозге он связан с токсическими скоплениями белков, наблюдаемыми при болезнях Альцгеймера, Паркинсона и Хантингтона, и с постепенной потерей нейронов. При ожирении и сахарном диабете 2 типа стресс ЭР в печени, жировой ткани и поджелудочной железе нарушает действие инсулина и секрецию гормонов, усугубляя гипергликемию. При аутоиммунных заболеваниях, таких как ревматоидный артрит или воспалительные заболевания кишечника, стресс ЭР в иммунных и барьерных клетках усиливает воспаление и повреждение тканей.
Превращение уязвимости в мишень
Поскольку стресс ЭР находится на перекрёстке множества путей, он даёт несколько точек входа для терапии. Разработчики лекарств создают молекулы, которые либо уменьшают чрезмерно активные сигналы стресса, либо целенаправленно усиливают их в раковых клетках, чтобы вызвать их гибель. Некоторые соединения нацелены на три основных сенсора; другие усиливают шапероны вроде GRP78, улучшают удаление дефектных белков или защищают митохондрии. В обзоре также приведён перечень ранних клинических испытаний существующих препаратов — таких как производные жёлчных кислот, средства для лечения диабета и препараты для снижения холестерина — которые, по-видимому, ослабляют стресс ЭР у людей. Одновременно разрабатываются новые инструменты, такие как флуоресцентные зонды, наногели и экспериментальные противоопухолевые вакцины, чтобы точнее отслеживать или манипулировать стрессом ЭР внутри опухолей и других тканей.
Дальнейший путь для терапии, основанной на ЭР
Авторы приходят к выводу, что стресс ЭР является как ранним драйвером, так и поддерживающей силой во многих хронических заболеваниях. Однако поскольку UPR может помогать или вредить в зависимости от дозы и времени, будущие лечения должны быть точно настроены, а не просто включаться или выключаться. Лучшие модели на животных, комбинирующие несколько заболеваний, вместе с «омикс»-технологиями, которые измеряют сигналы стресса по целым органам, должны прояснить, когда вмешательство будет полезным. Если эти задачи удастся решить, терапия, восстанавливающая баланс внутренней «фабрики» клетки, может дополнить существующие лекарства, предлагая новые способы замедлить развитие рака, защитить сердце и мозг, улучшить обмен веществ и успокоить ошибочные иммунные ответы.
Цитирование: Wei, S., Zhang, N., Zhang, H. et al. Endoplasmic reticulum stress in disease pathogenesis: its implications for therapy. Sig Transduct Target Ther 11, 136 (2026). https://doi.org/10.1038/s41392-026-02600-z
Ключевые слова: стресс эндоплазматического ретикулума, ответ на накопление неправильно свернувшихся белков, терапия рака, нейродегенеративные заболевания, метаболические нарушения