Clear Sky Science · de
Endoplasmatisches-Retikulum‑Stress in der Krankheitsentstehung: Bedeutung für die Therapie
Wenn die Zellfabriken schiefgehen
Jede Zelle in Ihrem Körper enthält eine winzige Fabrik, das endoplasmatische Retikulum (ER), in der die meisten Proteine in ihre funktionsfähigen Formen gefaltet werden. Dieses Review erklärt, was passiert, wenn diese Fabrik überlastet oder beschädigt ist – ein Zustand, der als ER‑Stress bezeichnet wird – und wie er leise zu vielen schweren Krankheiten beiträgt, von Krebs und Herzkrankheiten bis zu Alzheimer, Diabetes und Autoimmunerkrankungen. Das Verständnis dieser verborgenen Stressantwort hilft nicht nur zu erklären, warum so unterschiedliche Erkrankungen gemeinsame Merkmale wie Entzündung und Zelltod teilen, sondern weist auch auf neue Therapieansätze hin, die die zelleigenen Reparatursysteme feinjustieren.
Wie Zellen innere Probleme erkennen
Proteine entstehen als flexible Ketten, die sorgfältig gefaltet werden müssen. Hitze, Sauerstoffmangel, überschüssige Nährstoffe, Toxine oder genetische Mutationen können dazu führen, dass sich fehlgefaltete Proteine im ER ansammeln. Um damit fertigzuwerden, aktivieren Zellen ein koordiniertes Schutzprogramm, die sogenannte unfolded protein response (UPR). Drei in die ER‑Membran eingebettete Sensorproteine – IRE1, ATF6 und PERK – fungieren wie Alarme, die anspringen, sobald sie fehlgefaltete Proteine registrieren. Gemeinsam verlangsamen sie den Zustrom neuer Proteine, erhöhen die Produktion von Faltungshelfern und Qualitätskontrollfaktoren und steigern die Entfernung defekter Proteine. Gelingt diese Reaktion, wird das Gleichgewicht wiederhergestellt und die Zelle überlebt.
Wenn Anpassung in Schaden umschlägt
Dasselbe Sicherheitssystem kann schädlich werden, wenn der Stress zu stark oder zu langanhaltend ist. Unter chronischem Druck wandelt sich die UPR von einem Schutzmechanismus zu einem Weg, der die Zelle zur Selbstzerstörung treibt. Pro‑death‑Signale werden aktiviert, reaktive Moleküle häufen sich an und die Kommunikation mit anderen Zellkompartimenten wie den Mitochondrien bricht zusammen. Dieser anhaltende ER‑Stress kann verletzliche Zellen direkt töten oder Überlebende so verändern, dass sie Krankheiten vorantreiben – indem sie etwa Wachstum, Energiestoffwechsel oder die Interaktion mit dem Immunsystem verändern. Das Review verfolgt diese Schritt‑für‑Schritt‑Veränderungen und zeigt, wie das ER zu einem Steuerzentrum für Zellschicksal, Stoffwechsel und Entzündung wird.
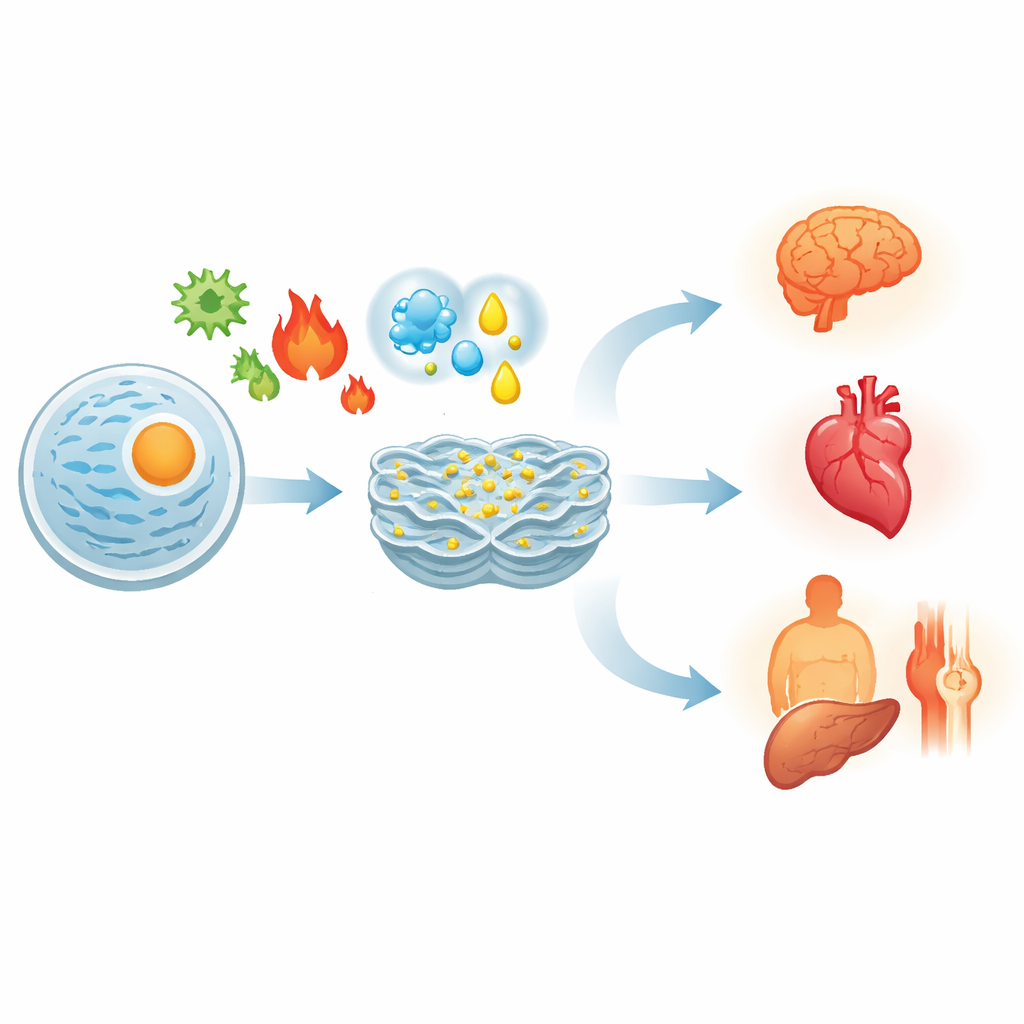
Ein gemeinsamer Faden in vielen Erkrankungen
Da alle Organe auf korrekt gefaltete Proteine angewiesen sind, tritt ER‑Stress in sehr unterschiedlichen Krankheitsbildern auf. Bei Krebs leben Tumorzellen am Rande ständigen ER‑Stresses wegen schnellen Wachstums und schlechter Durchblutung. Sie nutzen die UPR, um weiter zu proliferieren und einer Immunattacke zu entgehen, können aber in den Zelltod getrieben werden, wenn der Stress weiter erhöht wird. Im Herzen und den Blutgefäßen trägt ER‑Stress zu verkalkten Arterien, Schäden nach einem Herzinfarkt und Herzinsuffizienz bei, indem Muskel‑ und Gefäßzellen geschädigt werden. Im Gehirn steht er im Zusammenhang mit den toxischen Proteinansammlungen, die bei Alzheimer, Parkinson und Huntington beobachtet werden, sowie mit dem schrittweisen Neuronenverlust. Bei Adipositas und Typ‑2‑Diabetes stört ER‑Stress in Leber, Fettgewebe und Bauchspeicheldrüse die Insulinwirkung und Hormonsekretion und fördert so hohen Blutzucker. Bei Autoimmunerkrankungen wie Rheumatoider Arthritis oder entzündlichen Darmerkrankungen verstärkt ER‑Stress in Immun‑ und Barrierezellen Entzündung und Gewebeschaden.
Eine Schwäche zum Ziel machen
Weil ER‑Stress im Schnittpunkt so vieler Signalwege liegt, bietet er mehrere Ansatzpunkte für Therapien. Arzneimittelentwickler haben Moleküle entworfen, die überaktive Stresssignale dämpfen oder sie in Tumorzellen gezielt verstärken, um deren Tod auszulösen. Einige Verbindungen zielen auf die drei Hauptsensoren; andere stärken Faltungshelfer wie GRP78, verbessern die Beseitigung fehlerhafter Proteine oder schützen Mitochondrien. Das Review katalogisiert auch frühe klinische Studien zu bereits vorhandenen Medikamenten – etwa Gallensäurederivate, Diabetesmittel und cholesterinsenkende Wirkstoffe –, die beim Menschen offenbar ER‑Stress lindern. Gleichzeitig werden neue Werkzeuge wie fluoreszierende Sonden, Nanogel‑Träger und experimentelle Krebsimpfstoffe entwickelt, um ER‑Stress in Tumoren und anderen Geweben präziser nachzuverfolgen oder zu manipulieren.
Der Weg vorwärts für ER‑basierte Behandlungen
Die Autoren kommen zu dem Schluss, dass ER‑Stress sowohl ein früher Treiber als auch eine aufrechterhaltende Kraft vieler chronischer Krankheiten ist. Da die UPR jedoch je nach Stärke und Timing hilfreich oder schädlich sein kann, müssen künftige Therapien sorgfältig abgestimmt und nicht einfach ein‑ oder ausgeschaltet werden. Bessere Tiermodelle, die mehrere Krankheitsaspekte kombinieren, zusammen mit Omics‑Technologien, die Stresssignale über ganze Organe messen, sollten klären, wann eine Intervention nützt. Können diese Herausforderungen gemeistert werden, könnten Therapien, die die interne Zellenfabrik wieder ins Gleichgewicht bringen, bestehende Medikamente ergänzen und neue Wege eröffnen, Krebs zu verlangsamen, Herz und Gehirn zu schützen, den Stoffwechsel zu verbessern und fehlgeleitete Immunantworten zu dämpfen.
Zitation: Wei, S., Zhang, N., Zhang, H. et al. Endoplasmic reticulum stress in disease pathogenesis: its implications for therapy. Sig Transduct Target Ther 11, 136 (2026). https://doi.org/10.1038/s41392-026-02600-z
Schlüsselwörter: Stress des endoplasmatischen Retikulums, unfolded protein response, Krebstherapie, neurodegenerative Erkrankung, metabolische Störungen