Clear Sky Science · nl
Endoplasmatisch reticulum-stress in ziektepathogenese: implicaties voor therapie
Wanneer de fabrieken in cellen misgaan
Elke cel in uw lichaam bevat een kleine fabriek die het endoplasmatisch reticulum (ER) wordt genoemd, waar de meeste eiwitten in hun werkbare vormen worden gevouwen. Deze overzichtsartikel legt uit wat er gebeurt wanneer die fabriek overbelast of beschadigd raakt — een toestand bekend als ER-stress — en hoe dit stilletjes bijdraagt aan veel grote ziekten, van kanker en hartziekte tot Alzheimer, diabetes en auto-immuunziekten. Inzicht in deze verborgen stressreactie helpt niet alleen verklaren waarom zulke verschillende ziekten gemeenschappelijke kenmerken delen zoals ontsteking en celverlies, maar wijst ook op nieuwe behandelrichtingen die de eigen reparatiesystemen van de cel verfijnen.
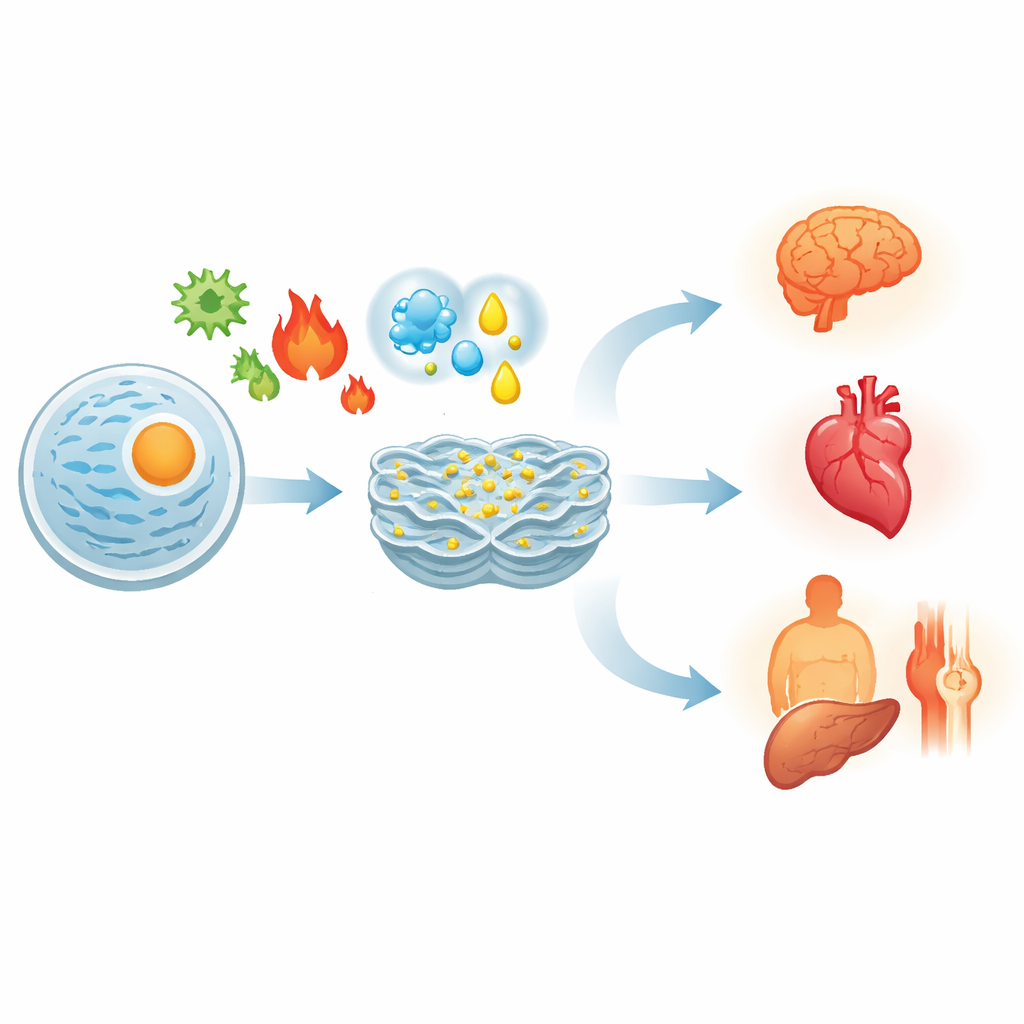
Hoe cellen intern problemen waarnemen
Eiwitten worden gemaakt als slappe ketens die zorgvuldig gevouwen moeten worden. Hitte, gebrek aan zuurstof, overtollige voedingsstoffen, toxines of genetische mutaties kunnen allemaal leiden tot ophoping van verkeerd gevouwen eiwitten in het ER. Om dit aan te pakken activeren cellen een gecoördineerd verdedigingsprogramma dat de unfolded protein response (UPR) wordt genoemd. Drie sensors-eiwitten ingebed in het ER‑membraan — IRE1, ATF6 en PERK — fungeren als alarmen die aangaan wanneer ze verkeerd gevouwen eiwitten detecteren. Gezamenlijk verminderen ze de instroom van nieuwe eiwitten, verhogen ze de productie van vouwhulpstoffen en kwaliteitscontrolefactoren, en bevorderen ze de afvoer van defecte eiwitten. Als deze reactie slaagt, wordt het evenwicht hersteld en overleeft de cel.
Wanneer aanpassing overgaat in schade
Datzelfde beveiligingssysteem kan schadelijk worden wanneer de stress te intens is of te lang aanhoudt. Onder chronische druk verschuift de UPR van beschermend naar het aanzetten tot zelfvernietiging van cellen. Pro‑doodsignalen worden geactiveerd, reactieve moleculen hopen zich op, en de communicatie met andere celonderdelen zoals mitochondriën raakt verstoord. Deze langdurige ER‑stress kan kwetsbare cellen helemaal doden of overlevenden zodanig veranderen dat ze ziekte aansturen — door te veranderen hoe ze groeien, energie gebruiken of met het immuunsysteem communiceren. De review beschrijft deze stapsgewijze veranderingen en toont hoe het ER een controledistributiecentrum wordt voor celfate, metabolisme en ontsteking.
Een gemeenschappelijke draad door veel ziekten
Aangezien alle organen afhankelijk zijn van goed gevouwen eiwitten, doet ER‑stress zich voor in zeer verschillende aandoeningen. Bij kankers leven tumorcellen voortdurend op het randje van ER‑stress door snelle groei en slechte bloedvoorziening. Ze benutten de UPR om te blijven delen en immuunaanvallen te ontlopen, maar kunnen tot celdood worden geduwd als de stress verder wordt verhoogd. In het hart en de bloedvaten draagt ER‑stress bij aan verstopte slagaders, schade na een hartaanval en hartfalen door schade aan spier- en vaatcellen. In de hersenen wordt het in verband gebracht met de toxische eiwitophopingen die gezien worden bij Alzheimer, Parkinson en Huntington, en met het geleidelijke verlies van neuronen. Bij obesitas en type 2 diabetes verstoort ER‑stress in lever, vetweefsel en alvleesklier de insulinewerking en hormoonsecretie, wat bijdraagt aan hoge bloedsuikers. Bij auto-immuunziekten zoals reumatoïde artritis of inflammatoire darmziekte versterkt ER‑stress in immuun- en barrièrecellen ontsteking en weefselbeschadiging.
Een zwakte omzetten in een doelwit
Aangezien ER‑stress op het kruispunt van zoveel paden ligt, biedt het meerdere aanknopingspunten voor therapie. Geneesmiddelenontwikkelaars hebben moleculen ontworpen die ofwel overactieve stresssignalen dempen of ze opzettelijk overdrijven in kankercellen om hun dood te veroorzaken. Sommige verbindingen richten zich op de drie hoofd‑sensors; andere versterken vouwhulpstoffen zoals GRP78, verbeteren de klaring van defecte eiwitten of beschermen mitochondriën. De review catalogueert ook vroege klinische onderzoeken met bestaande geneesmiddelen — zoals galzuurderivaten, diabetesmedicijnen en cholesterolverlagende middelen — die lijken te helpen bij het verminderen van ER‑stress bij mensen. Tegelijk worden nieuwe hulpmiddelen zoals fluorescerende sondes, nanogels en experimentele kanker‑vaccins ontwikkeld om ER‑stress preciezer te volgen of te manipuleren in tumoren en andere weefsels.
De weg vooruit voor op ER gebaseerde behandelingen
De auteurs concluderen dat ER‑stress zowel een vroege drijfveer als een besturende kracht is in veel chronische ziekten. Omdat de UPR echter kan helpen of schaden afhankelijk van dosis en timing, moeten toekomstige behandelingen zorgvuldig worden afgestemd in plaats van eenvoudigweg aan- of uitgezet. Betere diermodellen die meerdere ziekten combineren, samen met "omics"‑technologieën die stresssignalen over hele organen meten, zouden moeten verduidelijken wanneer interventie zinvol is. Als deze uitdagingen kunnen worden overwonnen, kunnen therapieën die de interne fabriek van de cel weer in balans brengen bestaande geneesmiddelen aanvullen en nieuwe manieren bieden om kanker te vertragen, het hart en de hersenen te beschermen, het metabolisme te verbeteren en verkeerd gerichte immuunreacties te kalmeren.
Bronvermelding: Wei, S., Zhang, N., Zhang, H. et al. Endoplasmic reticulum stress in disease pathogenesis: its implications for therapy. Sig Transduct Target Ther 11, 136 (2026). https://doi.org/10.1038/s41392-026-02600-z
Trefwoorden: endoplasmatisch reticulum-stress, onfolded protein response, kankertherapie, neurodegeneratieve ziekte, metabole aandoeningen