Clear Sky Science · es
Estrés del retículo endoplásmico en la patogenia de las enfermedades: implicaciones para la terapia
Cuando las fábricas celulares fallan
Cada célula de su cuerpo contiene una pequeña fábrica llamada retículo endoplásmico, o RE, donde la mayoría de las proteínas se pliegan hasta alcanzar su forma funcional. Esta revisión explica qué ocurre cuando esa fábrica se sobrecarga o se daña —un estado conocido como estrés del RE— y cómo contribuye de forma silente a muchas enfermedades importantes, desde el cáncer y las cardiopatías hasta el Alzheimer, la diabetes y los trastornos autoinmunes. Comprender esta respuesta oculta al estrés no solo ayuda a explicar por qué enfermedades tan diferentes comparten rasgos comunes como la inflamación y la pérdida celular, sino que también señala nuevos tipos de tratamientos que afinan los propios sistemas de reparación de la célula.
Cómo las células detectan problemas en su interior
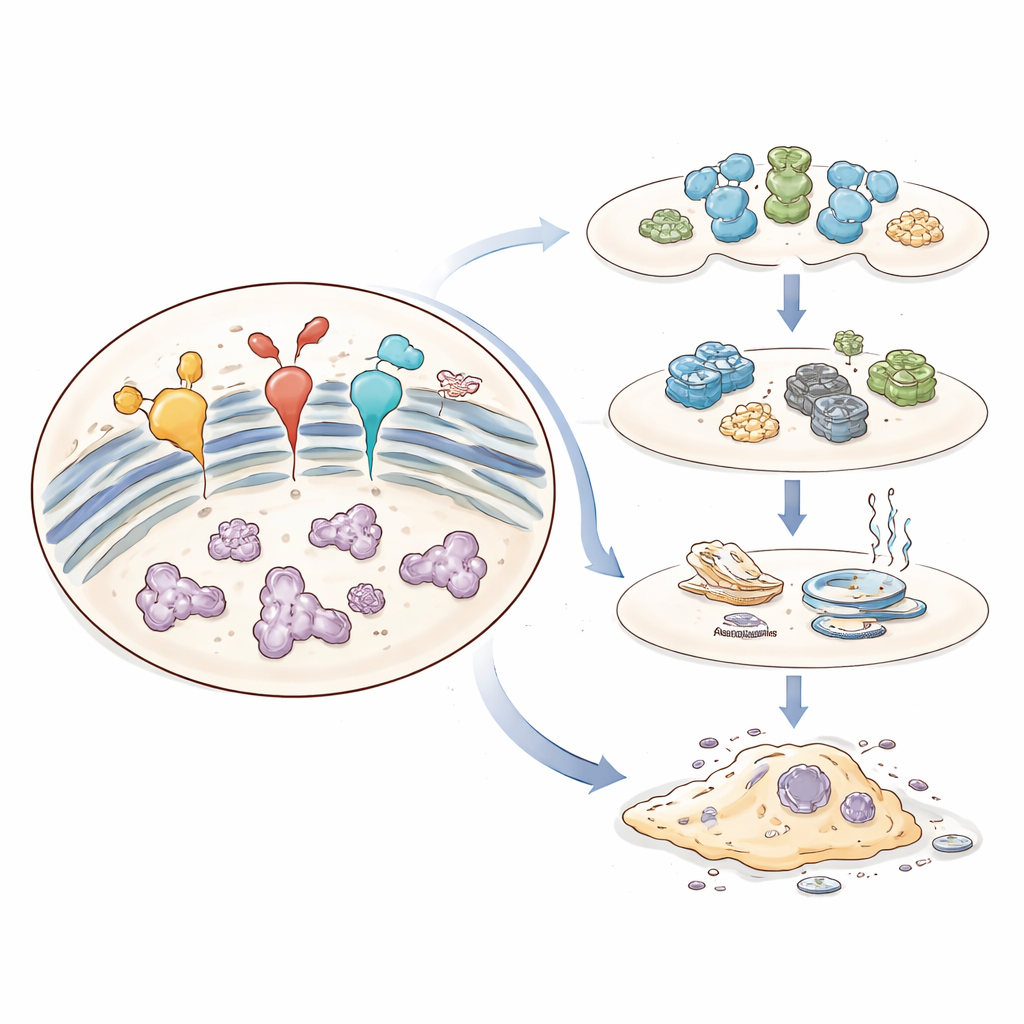
Las proteínas se sintetizan como cadenas flexibles que deben plegarse con cuidado. El calor, la falta de oxígeno, el exceso de nutrientes, las toxinas o mutaciones genéticas pueden provocar que proteínas mal plegadas se acumulen en el RE. Para hacer frente a esto, las células activan un programa de defensa coordinado llamado respuesta a proteínas desplegadas (UPR). Tres proteínas sensor incrustadas en la membrana del RE —IRE1, ATF6 y PERK— actúan como alarmas que se activan cuando detectan proteínas mal plegadas. En conjunto reducen la llegada de nuevas proteínas, incrementan la producción de ayudantes de plegamiento y factores de control de calidad, y aumentan la eliminación de proteínas defectuosas. Si esta respuesta tiene éxito, se restablece el equilibrio y la célula sobrevive.
Cuando la adaptación se convierte en daño
El mismo sistema de seguridad puede volverse perjudicial cuando el estrés es demasiado intenso o se prolonga demasiado. Bajo presión crónica, la UPR pasa de ser protectora a empujar a las células hacia la autodestrucción. Se activan señales pro-muerte, se acumulan moléculas reactivas y se altera la comunicación con otras partes celulares como las mitocondrias. Este estrés prolongado del RE puede matar directamente a células vulnerables o dejar supervivientes alterados de maneras que impulsan la enfermedad —cambiando cómo crecen, cómo usan la energía o cómo se comunican con el sistema inmune. La revisión sigue estos cambios paso a paso, mostrando cómo el RE se convierte en un centro de control del destino celular, el metabolismo y la inflamación.
Un hilo común en muchas enfermedades
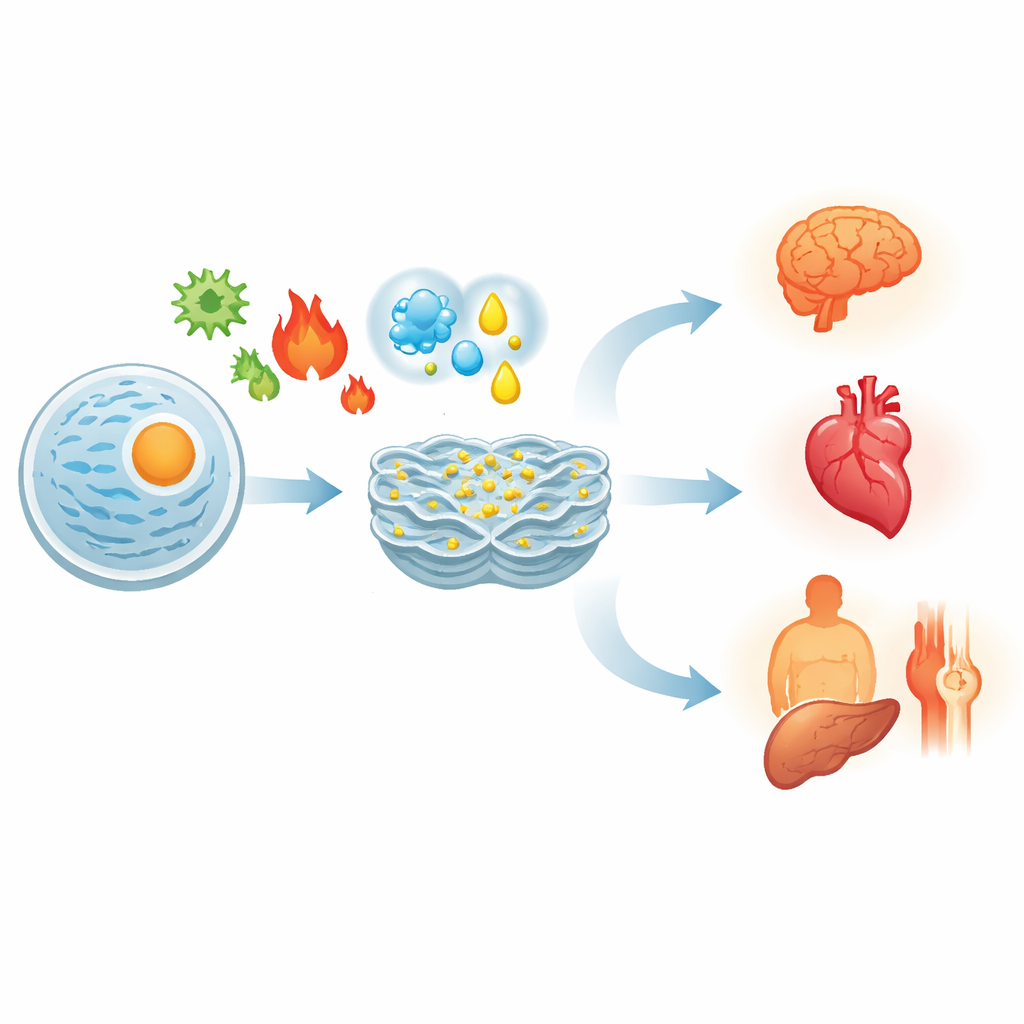
Dado que todos los órganos dependen de proteínas correctamente plegadas, el estrés del RE aparece en condiciones muy distintas. En los cánceres, las células tumorales viven al límite de un estrés constante del RE debido al rápido crecimiento y al débil suministro sanguíneo. Explotan la UPR para seguir dividiéndose y evadir el ataque inmune, pero pueden ser empujadas hacia la muerte si el estrés se intensifica. En el corazón y los vasos sanguíneos, el estrés del RE contribuye a la obstrucción arterial, al daño tras un infarto y a la insuficiencia cardíaca al perjudicar células musculares y vasculares. En el cerebro, se asocia a los depósitos proteicos tóxicos observados en el Alzheimer, el Parkinson y la enfermedad de Huntington, y a la pérdida gradual de neuronas. En la obesidad y la diabetes tipo 2, el estrés del RE en hígado, tejido adiposo y páncreas altera la acción de la insulina y la secreción hormonal, alimentando la hiperglucemia. En enfermedades autoinmunes como la artritis reumatoide o la enfermedad inflamatoria intestinal, el estrés del RE en células inmunes y de barrera amplifica la inflamación y el daño tisular.
Convertir una debilidad en un objetivo
Puesto que el estrés del RE se sitúa en la encrucijada de tantas vías, ofrece múltiples puntos de entrada para la terapia. Los desarrolladores de fármacos han diseñado moléculas que o bien atenúan señales de estrés sobreactivas o bien las exageran deliberadamente en células cancerosas para desencadenar su muerte. Algunos compuestos apuntan a los tres sensores principales; otros aumentan los ayudantes de plegamiento como GRP78, potencian la eliminación de proteínas defectuosas o protegen las mitocondrias. La revisión también cataloga ensayos clínicos tempranos con fármacos existentes —como derivados de ácidos biliares, medicamentos para la diabetes y agentes reductores del colesterol— que parecen aliviar el estrés del RE en pacientes. Al mismo tiempo, se están desarrollando nuevas herramientas como sondas fluorescentes, nanogeles y vacunas cancerígenas experimentales para rastrear o manipular el estrés del RE con mayor precisión dentro de tumores y otros tejidos.
El camino por delante para los tratamientos basados en el RE
Los autores concluyen que el estrés del RE es tanto un impulsor temprano como una fuerza que mantiene muchas enfermedades crónicas. Sin embargo, dado que la UPR puede ayudar o perjudicar según la dosis y el momento, los tratamientos futuros deben ajustarse con cuidado en lugar de limitarse a activarse o desactivarse. Mejores modelos animales que combinen múltiples enfermedades, junto con tecnologías «ómicas» que midan señales de estrés a través de órganos enteros, deberían aclarar cuándo la intervención será beneficiosa. Si estos retos se superan, las terapias que reequilibren la fábrica interna de la célula podrían complementar los fármacos existentes, ofreciendo nuevas vías para frenar el cáncer, proteger el corazón y el cerebro, mejorar el metabolismo y calmar respuestas inmunitarias descontroladas.
Cita: Wei, S., Zhang, N., Zhang, H. et al. Endoplasmic reticulum stress in disease pathogenesis: its implications for therapy. Sig Transduct Target Ther 11, 136 (2026). https://doi.org/10.1038/s41392-026-02600-z
Palabras clave: estrés del retículo endoplásmico, respuesta a proteínas desplegadas, terapia contra el cáncer, enfermedad neurodegenerativa, trastornos metabólicos