Clear Sky Science · ru
Структурные сведения о фотохимии комплекса LH1–RC морской пурпурной фототрофной бактерии Rhodovulum sulfidophilum
Как крошечная морская бактерия превращает свет и серу в энергию
В мелких, богатых серой отложениях прибрежных морей обитает пурпурная бактерия, которая тихо перерабатывает химические вещества и улавливает солнечный свет. В этом исследовании подробно рассмотрен ее главный «солнечный аппарат», раскрывающий данные на атомном уровне о том, как свет захватывается и преобразуется в пригодную для клетки энергию. Понимание этой естественной «микросолнечной панели» углубляет наше представление о жизни в океанах и может вдохновить будущие светозависимые технологии.
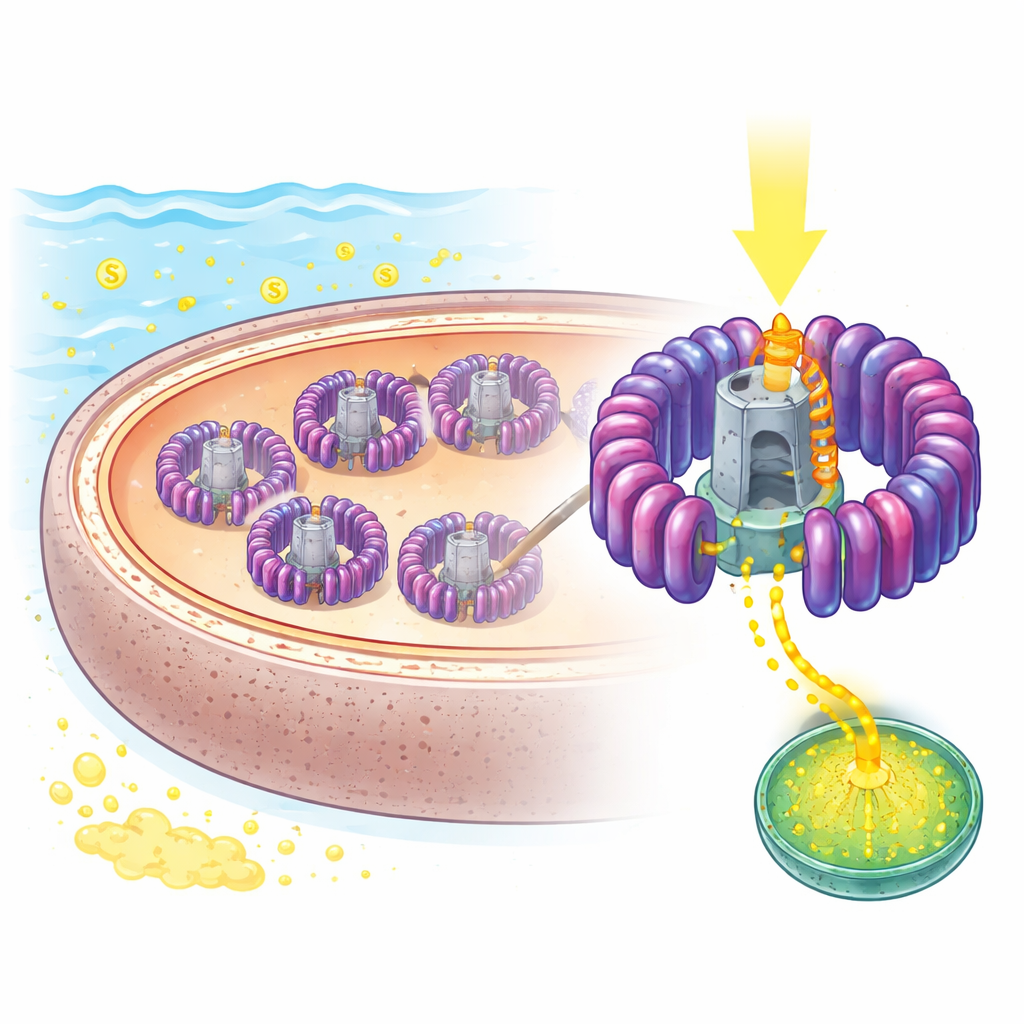
Внимательный взгляд на природную микросолнечную панель
Исследователи сосредоточились на морском микроорганизме Rhodovulum sulfidophilum, долго используемом в качестве модели бактериального фотосинтеза, поскольку он может расти как в слабоокислительных условиях при свете, так и в полностью аэробной среде, а также выдерживает высокие концентрации серы. Его основной светопоглощающий аппарат — объединённый комплекс light‑harvesting 1–reaction center, или LH1–RC, встроенный во внутренние мембраны. С помощью высокоразрешающей криоэлектронной микроскопии команда определила структуру этого комплекса с разрешением до 1,81 ангстрема — достаточно, чтобы увидеть отдельные пигменты, липиды и даже сотни молекул воды. Они обнаружили незамкнутое кольцо из 16 повторяющихся светосборных единиц, обвивающее центральный реакционный центр, где происходит разделение зарядов, с преднамеренным разрывом, по-видимому являющимся единственным путём для движения ключевых молекул внутрь и наружу.
Специальный «провод» для переноса электронов
В основе реакционного центра находится субъединица белка, действующая как встроенный провод для переноса электронов, известная как цитохром. У многих родственных бактерий этот «провод» содержит четыре гемсодержащих группы, но у Rhodovulum sulfidophilum их только три. Это породило вопрос: как электроны эффективно перетекают без обычного внешнего гема? Новая структура показывает, что средний гем (названный гем‑2) лиганирован—то есть связан—необычной аминокислотой цистеином вместо метионина, встречающегося у других видов. Эта тонкая замена значительно понижает его редокс‑потенциал, заставляя его вести себя подобно отсутствующему наружному гему у других бактерий. Поверхность вокруг этого гема открыта и сформирована так, чтобы позволять подходить растворимым белкам‑донаторам электронов, что намекает на то, что это ключевое «посадочное» место для входящих электронов.
Дополнительный металлический помощник рядом с путём электронов
Неожиданно команда обнаружила не‑гемное железо, расположенное близко к этому среднему гему, координированное гистидином из цитохрома и пятью молекулами воды. Спектроскопические измерения подтвердили его присутствие и показали, что оно находится очень близко к гему‑2, но дальше от других двух гемов. Это наводит на мысль, что дополнительное железо может выступать в роли ретранслятора, кратковременно принимая электроны от растворимых доноров, прежде чем передать их металлическим центрам цитохрома. Сочетая структурные данные и измерения электронного спинового состояния, авторы утверждают, что гем‑2, при участии этого соседнего железного узла, является самым вероятным первым приёмником электронов от растворимых цитохромов бактерии, помогая организму справляться с большими энергетическими разрывами между донорами и акцепторами в его серосодержащей среде.
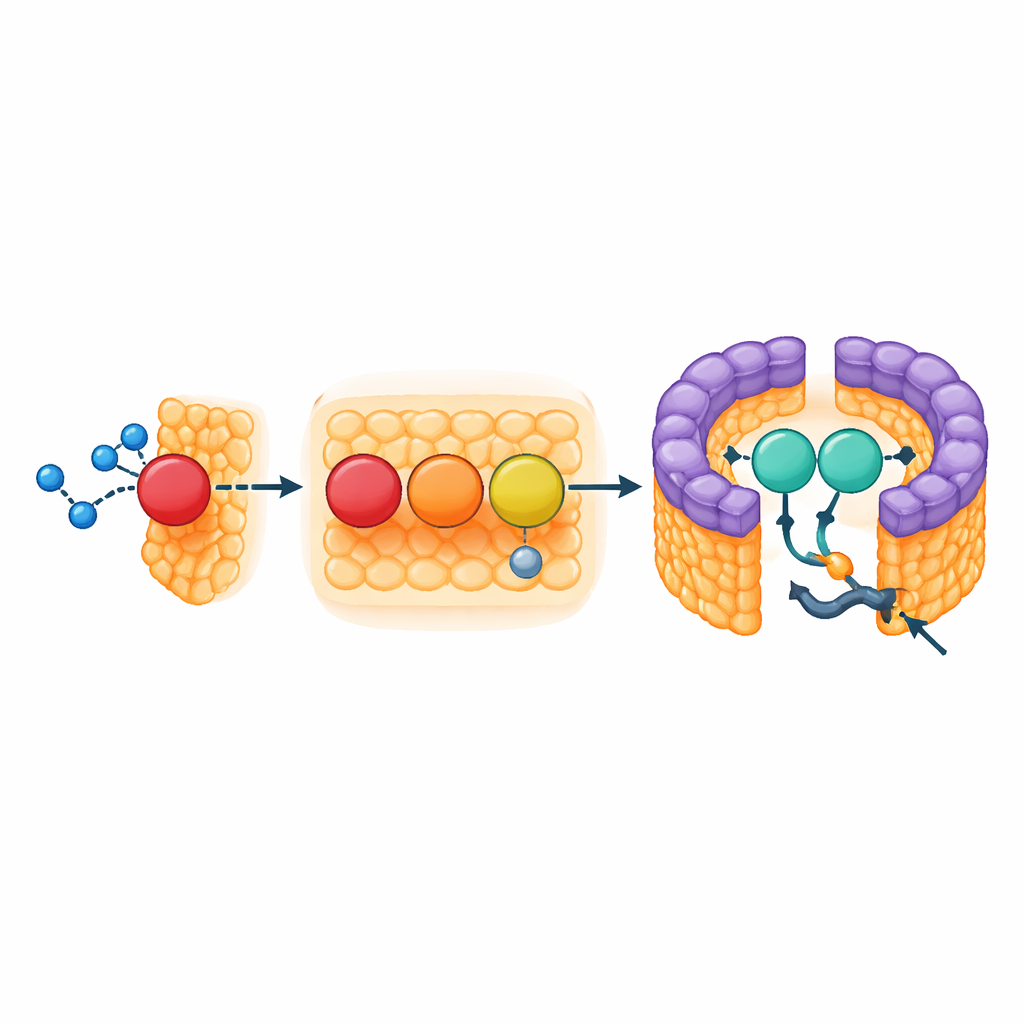
Поддерживающая опора у разрыва кольца
Часть комплекса LH1 образует плотный, насыщенный пигментами «забор», который улавливает свет и направляет возбуждение в реакционный центр, но его кольцо не полностью замкнуто. В зазоре расположены два структурных элемента: мембранно‑пронизывающий N‑конец субъединицы цитохрома и небольшой трёхспиральный белок, который авторы называют protein‑3h. Protein‑3h происходит от более крупного гена в дыхательной цепи бактерии (псевдогена, известного как urf1) и, по-видимому, был перепрофилирован. В комплексе LH1–RC он вклинивается в разрыв и захватывает как цитохром, так и соседние светосборные единицы, выступая в роли распорки, стабилизирующей отверстие. Поскольку плотные каротиноидные пигменты блокируют другие пути, это отверстие, вероятно, служит единственным шлюзом для молекул хинона, которые отводят электроны из реакционного центра в более широкую мембранную сеть.
Почему эта микромашина важна
В совокупности результаты показывают, как Rhodovulum sulfidophilum тонко настроил своё фотосинтетическое «оборудование» для жизни в переменных, богатых серой прибрежных водах. Он использует тригемовый цитохром с необычным металло‑связывающим участком, чтобы гибко принимать электроны от различных доноров, плотно закрытое кольцо для эффективного захвата и удержания энергии и перепрофилированный трёхспиральный белок, который одновременно стабилизирует и формирует единственный выход для подвижных переносчиков. Для неспециалистов ключевая мысль такова: даже одноклеточные организмы способны развивать замысловатые модульные «солнечные» устройства, части которых меняются, укорачиваются и переназначаются с течением времени — что предлагает природные принципы проектирования для надёжных и эффективных светозависимых систем.
Цитирование: Yue, XY., Wang, GL., Kosaki, S. et al. Structural insights into the photochemistry of the LH1–RC complex from the marine purple phototrophic bacterium Rhodovulum sulfidophilum. Commun Biol 9, 502 (2026). https://doi.org/10.1038/s42003-026-09755-z
Ключевые слова: бактериальный фотосинтез, комплекс сбора света, перенос электронов, криоэлектронная микроскопия, цикл серы