Clear Sky Science · pl
Wgląd strukturalny w fotochemię kompleksu LH1–RC u morskiej purpurowej bakterii fototroficznej Rhodovulum sulfidophilum
Jak maleńka morska bakteria zamienia światło i siarkę w energię
W płytkich, bogatych w siarkę mułach przybrzeżnych mórz żyje purpurowa bakteria, która cicho recyklinguje związki chemiczne i wychwytuje światło słoneczne. To badanie przybliża jej główną maszynę solarną, ujawniając szczegóły na poziomie atomowym tego, jak światło jest przechwytywane i przekształcane w użyteczną energię. Zrozumienie tego naturalnego „mikro‑panelu słonecznego” nie tylko pogłębia nasze wyobrażenie o życiu w oceanach, lecz także dostarcza inspiracji dla przyszłych technologii napędzanych światłem.
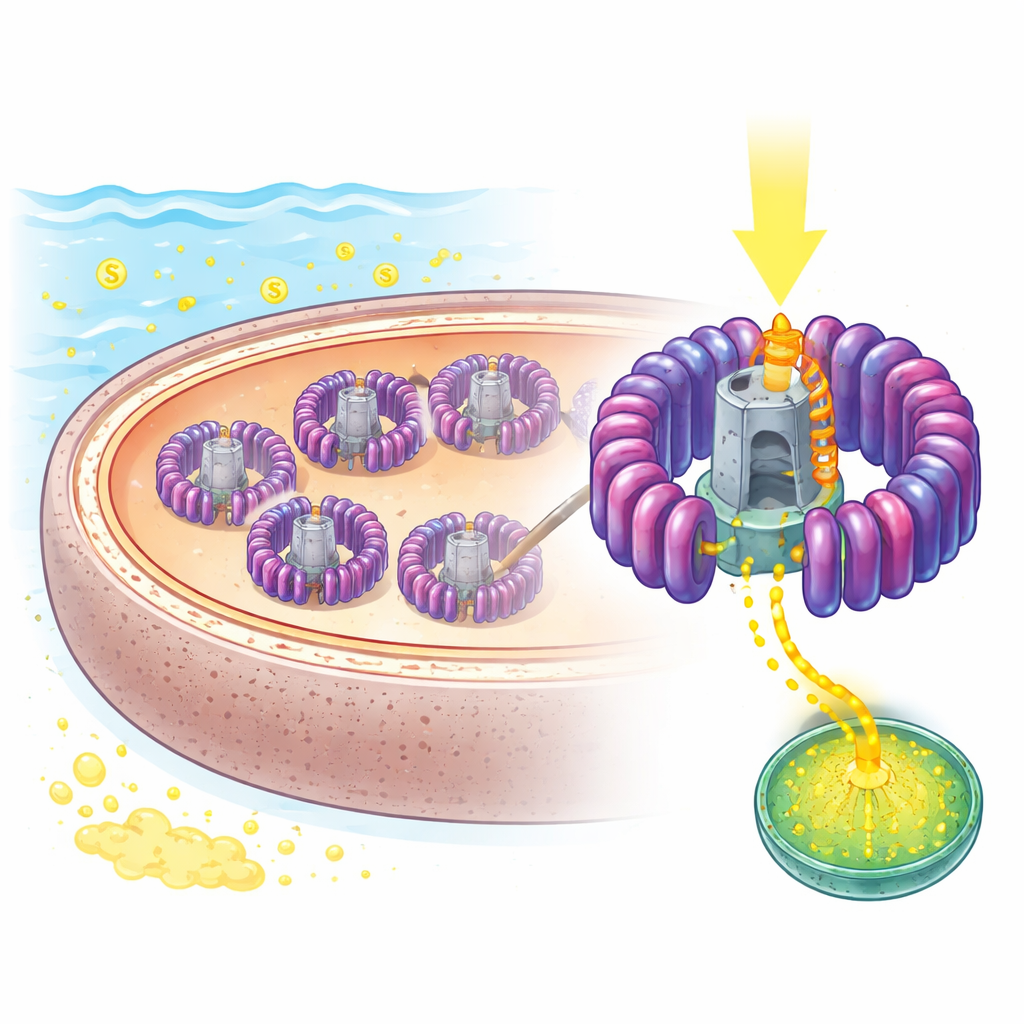
Bliższe spojrzenie na naturalny mikro panel słoneczny
Naukowcy skupili się na morskim mikroorganizmie zwanym Rhodovulum sulfidophilum, od dawna używanym jako model fotosyntezy bakteryjnej, ponieważ potrafi rosnąć zarówno przy małej zawartości tlenu przy świetle, jak i w pełni tlenowych warunkach oraz toleruje wysokie stężenia siarki. Jego podstawową maszyną korzystającą ze światła jest połączony kompleks light‑harvesting 1–reaction center, czyli LH1–RC, osadzony w błonach wewnętrznych. Wykorzystując wysokorozdzielczą kriomikroskopię elektronową zespół określił strukturę tego kompleksu do 1,81 Å — na tyle szczegółowo, by zobaczyć poszczególne pigmenty, lipidy, a nawet setki cząsteczek wody. Stwierdzono otwartą pierścieniową strukturę z 16 powtarzającymi się jednostkami wychwytu światła otaczającymi centralny centum reakcji, w którym zachodzi separacja ładunku, z celowo obecną szczeliną, która wydaje się być jedyną drogą dla kluczowych molekuł do przemieszczania się na zewnątrz i do wnętrza.
Szczególny przewód do przemieszczania elektronów
W sercu centrum reakcji znajduje się podjednostka białkowa pełniąca rolę wbudowanego przewodu do przenoszenia elektronów, znana jako cytochrom. U wielu spokrewnionych bakterii ten przewód niesie cztery hemy zawierające metal, lecz u Rhodovulum sulfidophilum są tylko trzy. To rodziło pytanie: jak elektrony mogą przepływać efektywnie bez zwykłego najbardziej zewnętrznego hemu? Nowa struktura pokazuje, że środkowy hem (zwany hem‑2) jest ligowany, czyli utrzymywany, przez nietypowy aminokwas cysteinę zamiast metioniny obserwowanej w innych gatunkach. Ta subtelna zamiana obniża w znacznym stopniu jego potencjał redoks, sprawiając, że zachowuje się bardziej jak brakujący zewnętrzny hem u innych bakterii. Powierzchnia wokół tego hemu jest odsłonięta i ukształtowana tak, by dopuszczać podejście rozpuszczalnych białek-dawców elektronów, co sugeruje, że jest to kluczowe miejsce przyjmowania nadchodzących elektronów.
Dodatkowy metalowy pomocnik przy ścieżce elektronowej
Nieoczekiwanie zespół odkrył atom żelaza niebędący hemem, umieszczony blisko tego środkowego hemu, koordynowany przez histydynę z cytochromu i pięć cząsteczek wody. Pomiary spektroskopowe potwierdziły jego obecność i wykazały, że leży bardzo blisko hemu‑2, ale dalej od pozostałych dwóch hemów. Sugeruje to, że dodatkowe żelazo może działać jako stacja przekaźnikowa, momentalnie akceptując elektrony od rozpuszczalnych donorów, zanim przekaże je do metalicznych centrów cytochromu. Łącząc dane strukturalne i pomiary spinowe elektronów, autorzy argumentują, że hem‑2, wspomagany przez pobliski klaster żelaza, jest najprawdopodobniejszym pierwszym odbiorcą elektronów od rozpuszczalnych cytochromów bakterii, pomagając organizmowi radzić sobie z dużymi różnicami energetycznymi między donorami a akceptorami w środowisku bogatym w siarkę.
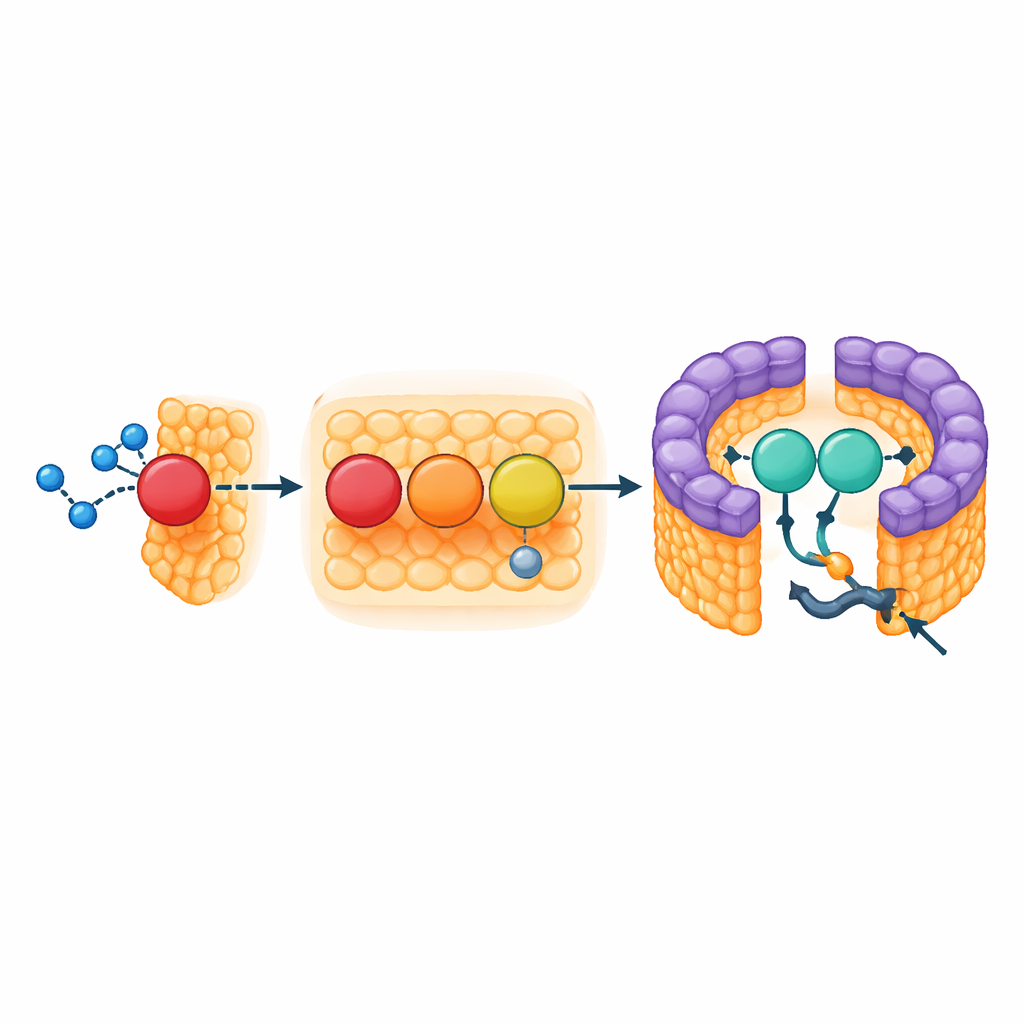
Wspierający wzmocnienie przy otwarciu pierścienia
Część LH1 kompleksu tworzy ciasny, naładowany pigmentami płot, który wychwytuje światło i kieruje wzbudzenie do centrum reakcji, ale jego pierścień nie jest całkowicie zamknięty. W szczelinie znajdują się dwa elementy strukturalne: zaczynająca się w błonie część podjednostki cytochromu oraz małe trzy‑heliksowe białko, które autorzy nazywają proteiną‑3h. Proteina‑3h pochodzi od większego genu w łańcuchu oddechowym bakterii (pseudogen zwanego urf1) i wydaje się została przeznaczona do nowej funkcji. W kompleksie LH1–RC klinuje się w szczelinie i przyczepia zarówno do cytochromu, jak i sąsiednich jednostek wychwytu światła, działając jak wzmocnienie stabilizujące otwarcie. Ponieważ gęste karotenoidowe pigmenty blokują inne drogi, to otwarcie prawdopodobnie służy jako jedyna brama dla cząsteczek chinonu, które przenoszą elektrony z centrum reakcji do szerszej sieci błonowej.
Dlaczego ta mikro‑maszyna ma znaczenie
Podsumowując, wyniki pokazują, jak Rhodovulum sulfidophilum dopracował swoje fotosyntetyczne wyposażenie pod kątem życia w zmiennych, bogatych w siarkę wodach przybrzeżnych. Wykorzystuje trihemowy cytochrom z nietypowym miejscem wiązania metalu, by elastycznie przyjmować elektrony od różnych donorów, ciasno zamknięty pierścień wychwytu światła do przechwytywania i zatrzymywania energii oraz przeznaczone do innej funkcji trzy‑heliksowe białko, które stabilizuje i kształtuje jedyną drogę wyjścia dla ruchomych przenośników. Dla czytelników niebędących specjalistami kluczowy wniosek jest taki, że nawet organizmy jednokomórkowe mogą wyewoluować skomplikowane, modułowe urządzenia solarne, których części są wymieniane, przycinane i przekierowywane z czasem — dostarczając naturalnych zasad projektowania dla solidnych, wydajnych systemów napędzanych światłem.
Cytowanie: Yue, XY., Wang, GL., Kosaki, S. et al. Structural insights into the photochemistry of the LH1–RC complex from the marine purple phototrophic bacterium Rhodovulum sulfidophilum. Commun Biol 9, 502 (2026). https://doi.org/10.1038/s42003-026-09755-z
Słowa kluczowe: fotosynteza bakteryjna, kompleks wychwytu światła, transfer elektronów, kriomikroskopia elektronowa, obieg siarki