Clear Sky Science · nl
Structurele inzichten in de fotochemie van het LH1–RC-complex van de mariene paarse fototrofe bacterie Rhodovulum sulfidophilum
Hoe een kleine mariene bacterie licht en zwavel omzet in energie
In de ondiepe, zwavelrijke modder van kustzeeën leeft een paarse bacterie die stilletjes chemicaliën recyclet en zonlicht opvangt. Deze studie zoomt in op haar belangrijkste zonne‑machine en onthult atoomniveau‑details van hoe licht wordt opgevangen en omgezet in bruikbare energie. Begrip van dit natuurlijke "micro‑zonnepaneel" verdiept niet alleen ons beeld van het leven in de oceanen, maar biedt ook inspiratie voor toekomstige lichtgedreven technologieën.
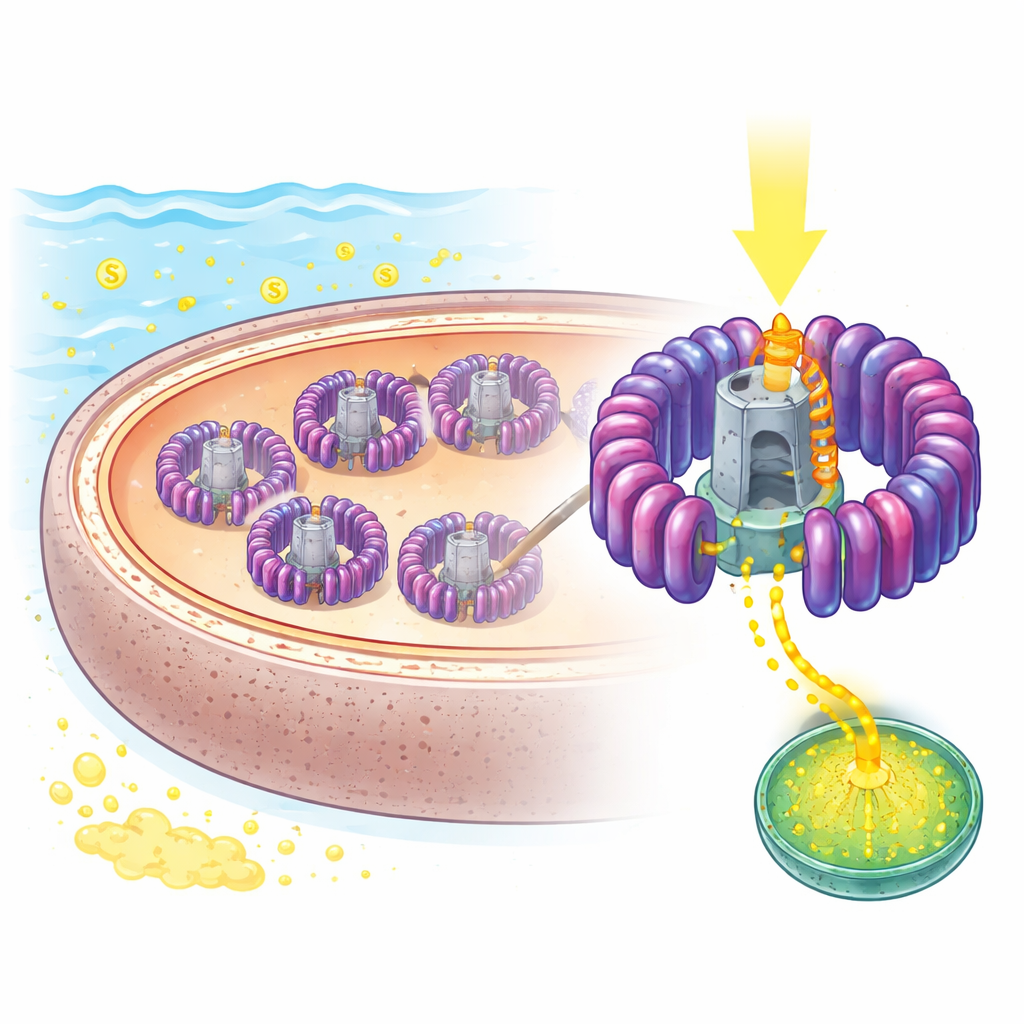
Een nadere blik op de microzonnecel van de natuur
De onderzoekers concentreerden zich op een mariene microbe genaamd Rhodovulum sulfidophilum, al lang gebruikt als model voor bacteriële fotosynthese omdat hij zowel in zuurstofarme lichtomstandigheden als in volledig zuurstofrijke omstandigheden kan groeien en hoge zwavelconcentraties verdrraagt. Zijn kernachtige lichtgebruikende machine is een gecombineerd light‑harvesting 1–reactiecentrumcomplex, of LH1–RC, ingebed in interne membranen. Met hoogresolutie cryo‑elektronenmicroscopie bepaalde het team de structuur van dit complex tot 1,81 ångström — fijn genoeg om individuele pigmenten, lipiden en zelfs honderden watermoleculen te zien. Ze vonden een open ring van 16 herhalende lichtopvangunits die zich om een centraal reactiecentrum wikkelen waar ladingsscheiding plaatsvindt, met een doelbewuste opening die lijkt de enige doorgang voor belangrijke moleculen om in en uit te bewegen.
Een speciale draad voor elektronenvervoer
In het hart van het reactiecentrum bevindt zich een eiwitsubunit die functioneert als een ingebouwde draad voor het verplaatsen van elektronen, bekend als een cytochroom. Bij veel verwante bacteriën draagt deze draad vier metaalhoudende heemgroepen, maar in Rhodovulum sulfidophilum zijn er slechts drie. Dit riep een raadsel op: hoe kunnen elektronen efficiënt stromen zonder het gebruikelijke buitenste heem? De nieuwe structuur laat zien dat het middelste heem (genoemd heem‑2) is geligeerd, of vastgehouden, door een ongewone cysteïne‑aminozuur in plaats van de methionine die in andere soorten wordt gezien. Deze subtiele verwisseling verlaagt sterk zijn redoxpotentiaal, waardoor het zich meer gedraagt als het ontbrekende buitenste heem in andere bacteriën. Het oppervlak rond dit heem is open en zodanig gevormd dat oplosbare elektrondonerende eiwitten kunnen naderen, wat erop wijst dat dit een belangrijk landingspunt is voor inkomende elektronen.
Een extra metalen helper nabij het elektronentraject
Onverwacht ontdekte het team een niet‑heemijzeratoom genesteld dicht bij dit middelste heem, gecoördineerd door een histidine van het cytochroom en vijf watermoleculen. Spectroscopische metingen bevestigden de aanwezigheid en toonden aan dat het zeer dicht bij heem‑2 ligt, maar verder verwijderd is van de andere twee heems. Dit suggereert dat het extra ijzer kan fungeren als een relaisstation, het kortstondig accepteren van elektronen van oplosbare donors voordat het deze doorgeeft aan de metaalcentra van het cytochroom. Door structurele en elektronspinmetingen te combineren, betogen de auteurs dat heem‑2, geholpen door dit nabijgelegen ijzercluster, de meest waarschijnlijke eerste ontvanger is van elektronen van de oplosbare cytochromen van de bacterie, waarmee de organisme omgaat met grote energiekloffen tussen donors en acceptoren in zijn zwavelrijke omgeving.
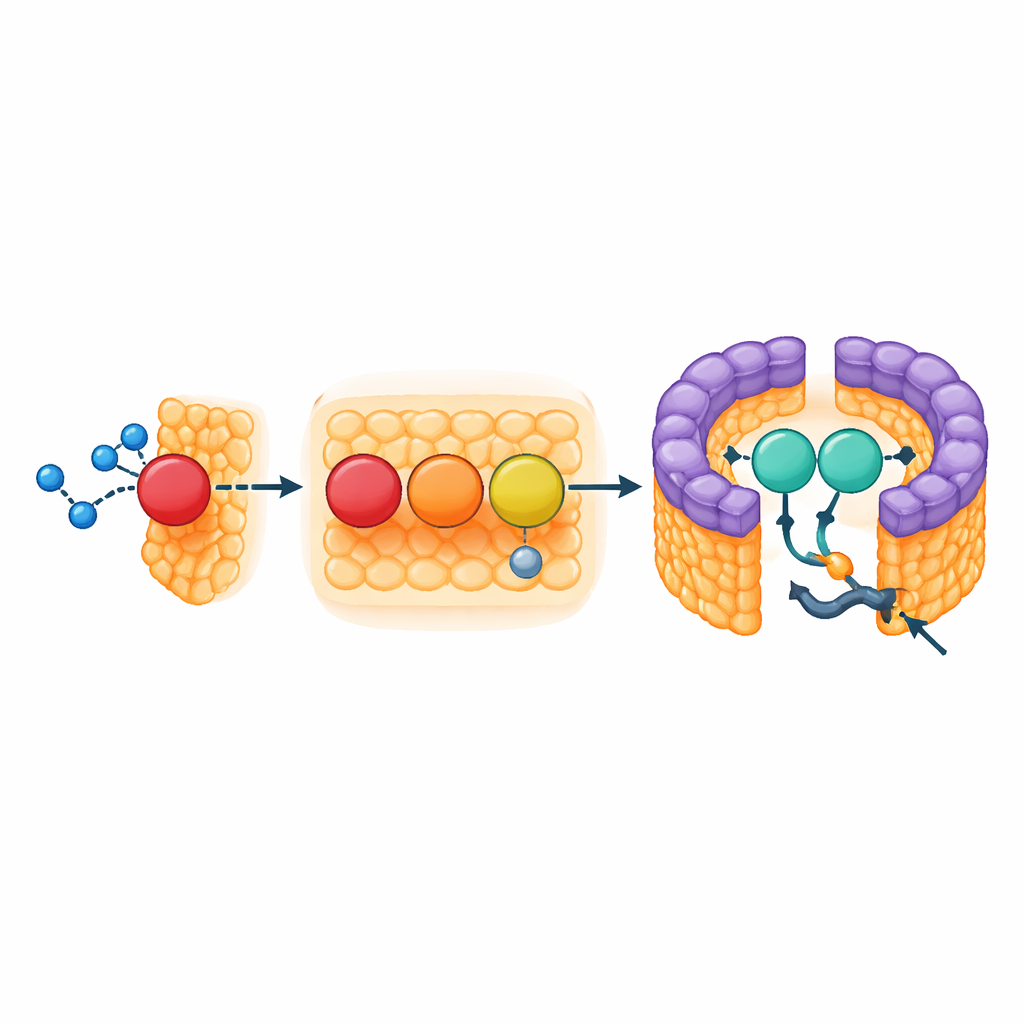
Een ondersteunende beugel bij de opening van de ring
Het LH1‑deel van het complex vormt een dichte, pigmentrijke omheining die licht opvangt en de excitatie naar het reactiecentrum leidt, maar de ring is niet volledig gesloten. Bij de opening zitten twee structurele elementen: het membraanoverspannende begin van de cytochromesubunit en een klein driehelix‑eiwit dat de auteurs eiwit‑3h noemen. Eiwit‑3h is afgeleid van een groter gen in de respiratoire keten van de bacterie (een pseudo‑gen bekend als urf1) en lijkt te zijn herbestemd. In het LH1–RC‑complex klemt het zich in de opening en grijpt zowel het cytochroom als aangrenzende lichtopvangunits vast, en fungeert als een beugel die de opening stabiliseert. Omdat de dichte carotenoïdepigmenten andere routes blokkeren, dient deze opening waarschijnlijk als de enige doorgang voor chinonmoleculen die elektronen van het reactiecentrum afvoeren naar het bredere membraannetwerk.
Waarom deze micromachine ertoe doet
Gezamenlijk laten de resultaten zien hoe Rhodovulum sulfidophilum zijn fotosynthetische hardware heeft verfijnd voor het leven in variabele, zwavelrijke kustwateren. Het gebruikt een triheemcytochroom met een ongewone metaalbindingsplaats om elektronen flexibel van verschillende donors te accepteren, een strak afgesloten lichtopvangring om energie te vangen en vast te houden, en een herbestemd driehelix‑eiwit om zowel de stabiliteit te geven als de enige uitgangsroute voor mobiele dragers vorm te geven. Voor niet‑specialisten is de kernboodschap dat zelfs eencellige organismen ingewikkelde, modulaire zonneapparaten kunnen evolueren waarvan onderdelen door de tijd heen worden verwisseld, bijgesneden en herverdeeld — wat natuurlijke ontwerpprincipes biedt voor robuuste, efficiënte lichtgedreven systemen.
Bronvermelding: Yue, XY., Wang, GL., Kosaki, S. et al. Structural insights into the photochemistry of the LH1–RC complex from the marine purple phototrophic bacterium Rhodovulum sulfidophilum. Commun Biol 9, 502 (2026). https://doi.org/10.1038/s42003-026-09755-z
Trefwoorden: bacteriële fotosynthese, lichtopvangcomplex, elektronentransfer, cryo-elektronenmicroscopie, zwavelkringloop