Clear Sky Science · it
Approfondimenti strutturali sulla fotochimica del complesso LH1–RC del batterio fototrofo viola marino Rhodovulum sulfidophilum
Come un minuscolo batterio marino trasforma luce e zolfo in energia
Nei fanghi costieri poco profondi e ricchi di zolfo vive un batterio viola che silenziosamente ricicla sostanze chimiche e cattura la luce solare. Questo studio si concentra sulla sua principale macchina solare, rivelando dettagli a livello atomico di come la luce venga catturata e convertita in energia utilizzabile. Comprendere questo “micro‑pannello solare” naturale non solo approfondisce la nostra visione della vita negli oceani, ma offre anche ispirazione per future tecnologie a energia luminosa.
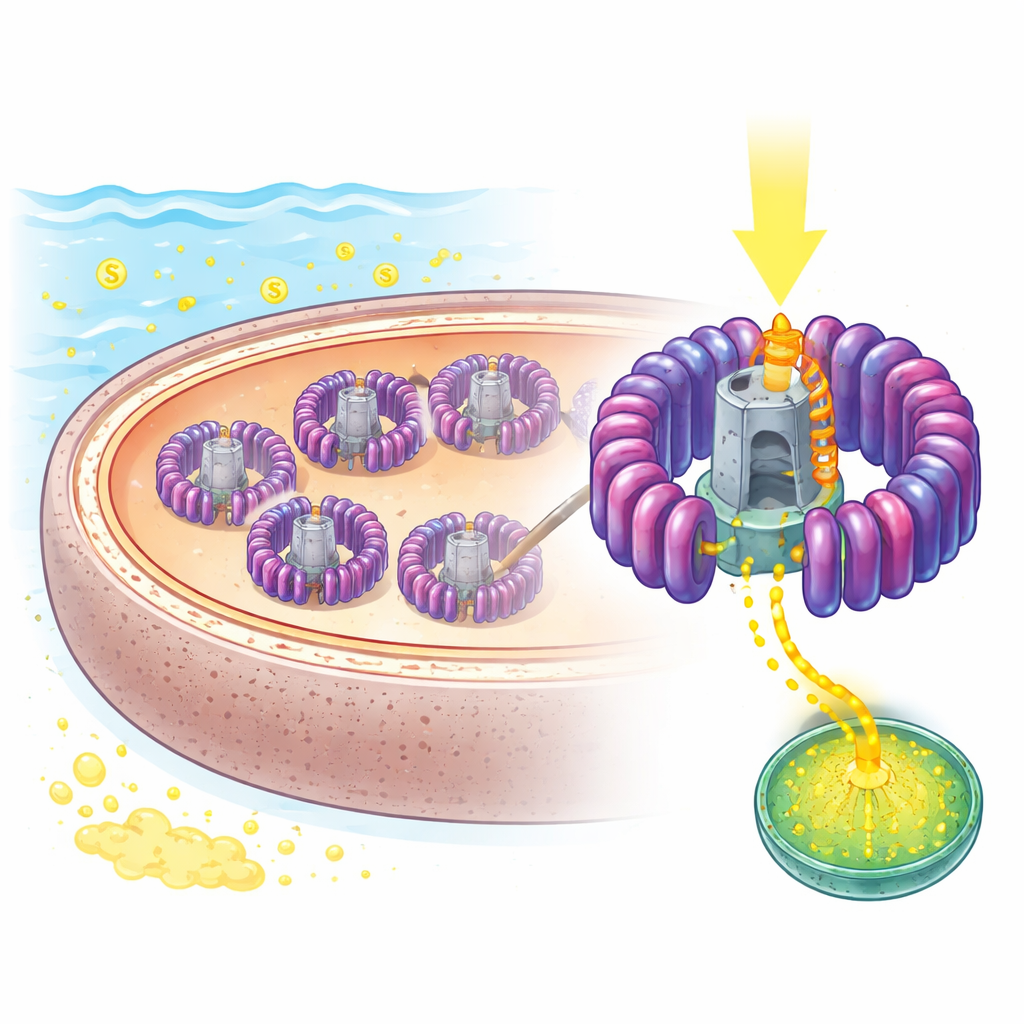
Uno sguardo ravvicinato al micro pannello solare della natura
I ricercatori si sono concentrati su un microbo marino chiamato Rhodovulum sulfidophilum, da tempo usato come modello per la fotosintesi batterica perché può crescere sia in condizioni di luce povere di ossigeno sia in condizioni completamente ossigenate, e tollera elevati livelli di zolfo. La sua macchina centrale per l’uso della luce è un complesso combinato di raccolta della luce 1–centro di reazione, o LH1–RC, inserito nelle membrane interne. Utilizzando la crio‑microscopia elettronica ad alta risoluzione, il team ha determinato la struttura di questo complesso fino a 1,81 angstrom — sufficiente per distinguere pigmenti, lipidi e persino centinaia di molecole d’acqua. Hanno osservato un anello aperto composto da 16 unità ripetute di raccolta della luce che avvolgono un centro di reazione centrale dove avviene la separazione di carica, con un’apertura deliberata che sembra essere l’unico percorso per il movimento delle molecole chiave dentro e fuori.
Un filo speciale per il trasferimento di elettroni
Al cuore del centro di reazione c’è una subunità proteica che funziona come un filo integrato per il trasferimento di elettroni, nota come citocromo. In molti batteri correlati questo filo porta quattro gruppi eme contenenti metallo, ma in Rhodovulum sulfidophilum ce ne sono soltanto tre. Questo ha posto un interrogativo: come possono gli elettroni fluire efficientemente senza l’eme più esterno tipico? La nuova struttura mostra che l’eme centrale (chiamato eme‑2) è legato, o coordinato, da un’insolita cisteina invece della metionina osservata in altre specie. Questa sottile sostituzione abbassa notevolmente il suo potenziale redox, facendolo comportare più come l’eme esterno mancante in altri batteri. La superficie attorno a questo eme è aperta e modellata per permettere l’avvicinamento di proteine solubili donatrici di elettroni, suggerendo che questo sia un sito d’atterraggio chiave per gli elettroni in arrivo.
Un aiuto metallico supplementare vicino al percorso elettronico
In modo inaspettato, il team ha scoperto un atomo di ferro non eme annidato vicino a questo eme centrale, coordinato da un’istidina del citocromo e da cinque molecole d’acqua. Misure spettroscopiche ne hanno confermato la presenza e mostrato che si trova molto vicino all’eme‑2, ma più distante dagli altri due emei. Ciò suggerisce che il ferro aggiuntivo possa agire come una stazione di rimbalzo, accettando temporaneamente elettroni da donatori solubili prima di passarli ai centri metallici del citocromo. Combinando dati strutturali e misure di spin elettronico, gli autori sostengono che l’eme‑2, assistito da questo cluster di ferro vicino, sia il più probabile primo ricevitore di elettroni dai citocromi solubili del batterio, aiutando l’organismo a gestire i grandi salti energetici tra donatori e accettori nel suo ambiente ricco di zolfo.
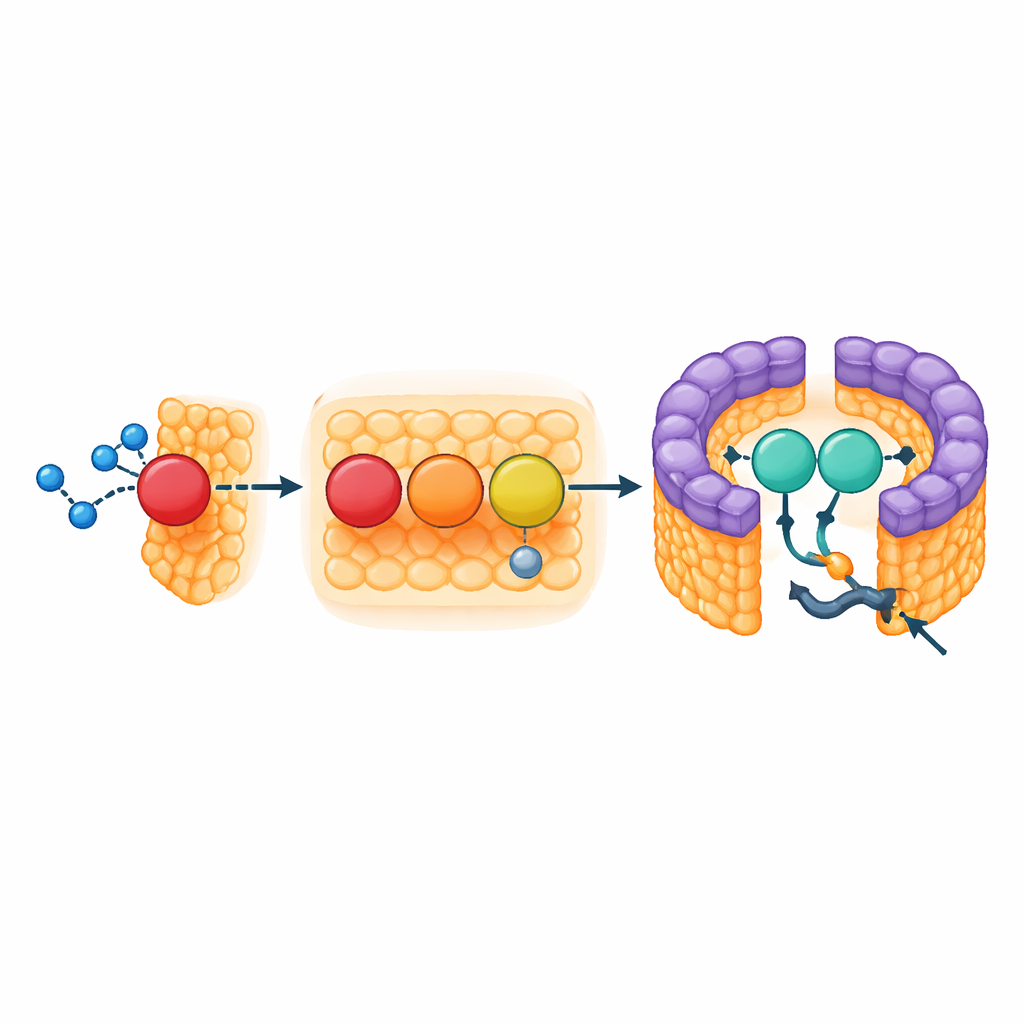
Un supporto di rinforzo all’apertura dell’anello
La porzione LH1 del complesso forma una barriera densa di pigmenti che cattura la luce e convoglia l’eccitazione al centro di reazione, ma il suo anello non è completamente chiuso. All’apertura si trovano due elementi strutturali: l’inizio transmembrana della subunità citocromo e una piccola proteina a tre eliche che gli autori chiamano protein‑3h. Protein‑3h deriva da un gene più grande della catena respiratoria del batterio (un pseudo‑gene noto come urf1) e sembra essere stato riutilizzato. Nel complesso LH1–RC, si infila nell’apertura e si aggrappa sia al citocromo sia alle unità di raccolta della luce adiacenti, fungendo da rinforzo che stabilizza l’apertura. Poiché i densi carotenoidi bloccano altre vie, questa apertura probabilmente serve come unico passaggio per le molecole di chinone che trasportano elettroni dal centro di reazione verso la rete di membrana più ampia.
Perché questa micro macchina è importante
Nel complesso, i risultati mostrano come Rhodovulum sulfidophilum abbia messo a punto il suo hardware fotosintetico per la vita in acque costiere variabili e ricche di zolfo. Usa un citocromo trieme con un insolito sito di legame metallico per accettare elettroni in modo flessibile da diversi donatori, un anello di raccolta della luce strettamente sigillato per catturare e trattenere energia, e una proteina a tre eliche riadattata per stabilizzare e modellare l’unica via d’uscita per i trasportatori mobili. Per i non specialisti, il messaggio chiave è che anche organismi unicellulari possono evolvere dispositivi solari modulari e complessi i cui componenti vengono scambiati, assottigliati e riassegnati nel tempo — offrendo principi di progetto naturali per sistemi a energia luminosa robusti ed efficienti.
Citazione: Yue, XY., Wang, GL., Kosaki, S. et al. Structural insights into the photochemistry of the LH1–RC complex from the marine purple phototrophic bacterium Rhodovulum sulfidophilum. Commun Biol 9, 502 (2026). https://doi.org/10.1038/s42003-026-09755-z
Parole chiave: fotosintesi batterica, complesso di raccolta della luce, trasferimento elettronico, crio microscopia elettronica, ciclo dello zolfo