Clear Sky Science · fr
Perspectives structurelles sur la photochimie du complexe LH1–RC de la bactérie phototrophe marine Rhodovulum sulfidophilum
Comment une minuscule bactérie marine transforme lumière et soufre en énergie
Dans les boues peu profondes et riches en soufre des mers côtières vit une bactérie pourpre qui recycle discrètement les composés chimiques et capte la lumière du soleil. Cette étude se concentre sur sa principale machine solaire, révélant des détails à l'échelle atomique sur la façon dont la lumière est recueillie et convertie en énergie utilisable. Comprendre ce « micro‑panneau solaire » naturel enrichit non seulement notre vision de la vie océanique, mais inspire aussi des idées pour de futures technologies alimentées par la lumière.
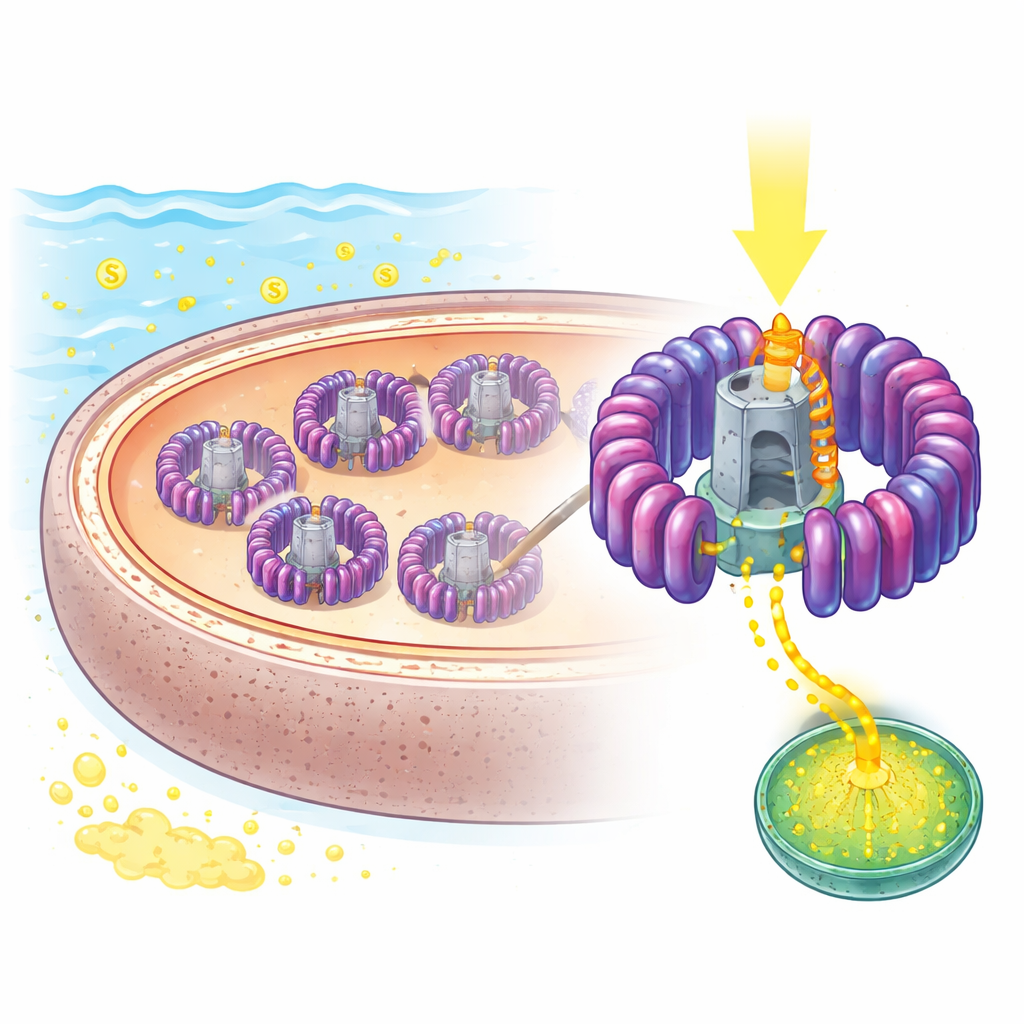
Un regard rapproché sur le micro‑panneau solaire de la nature
Les chercheurs se sont intéressés à un microbe marin nommé Rhodovulum sulfidophilum, longtemps utilisé comme modèle de photosynthèse bactérienne car il peut croître aussi bien en présence de lumière et de faibles niveaux d'oxygène qu'en conditions pleinement oxygénées, et tolère des concentrations élevées de soufre. Sa machine centrale d'utilisation de la lumière est un complexe combiné d'antenne de type light‑harvesting 1 et de centre réactionnel, ou LH1–RC, intégré dans des membranes internes. Grâce à la cryo‑microscopie électronique à haute résolution, l'équipe a déterminé la structure de ce complexe jusqu'à 1,81 angström — suffisamment précis pour distinguer les pigments individuels, les lipides et même des centaines de molécules d'eau. Ils ont observé un anneau ouvert composé de 16 unités répétées de capture de lumière entourant un centre réactionnel central où se produit la séparation de charge, avec une ouverture délibérée qui semble être la seule voie permettant aux molécules clés d'entrer et de sortir.
Un fil conducteur spécial pour le déplacement des électrons
Au cœur du centre réactionnel se trouve une sous‑unité protéique qui fonctionne comme un fil intégré pour transporter les électrons, connue sous le nom de cytochrome. Chez de nombreuses bactéries apparentées, ce « fil » porte quatre groupements heme métalliques, mais chez Rhodovulum sulfidophilum il n'y en a que trois. Cela pose une question : comment les électrons peuvent‑ils circuler efficacement sans l'heme externe habituel ? La nouvelle structure montre que l'heme médian (appelé heme‑2) est ligaturé, ou maintenu, par un acide aminé cystéine inhabituel au lieu de la méthionine observée chez d'autres espèces. Ce changement subtil abaisse fortement son potentiel rédox, le faisant se comporter davantage comme l'heme externe manquant chez d'autres bactéries. La surface autour de cet heme est ouverte et façonnée pour laisser approcher des protéines donneuses d'électrons solubles, ce qui suggère qu'il s'agit d'un site d'atterrissage clé pour les électrons entrants.
Un atout métallique supplémentaire près du trajet des électrons
De façon inattendue, l'équipe a découvert un atome de fer non‑heme niché à proximité de cet heme médian, coordonné par une histidine du cytochrome et cinq molécules d'eau. Des mesures spectroscopiques ont confirmé sa présence et montré qu'il se situe très près de l'heme‑2, mais plus éloigné des deux autres hemes. Cela suggère que ce fer supplémentaire peut agir comme une station relais, acceptant brièvement des électrons de donneurs solubles avant de les transmettre aux centres métalliques du cytochrome. En combinant des données structurales et des mesures du spin électronique, les auteurs soutiennent que l'heme‑2, aidé par ce cluster ferrique voisin, est le plus probable premier récepteur des électrons provenant des cytochromes solubles de la bactérie, aidant l'organisme à compenser les larges écarts d'énergie entre donneurs et accepteurs dans son environnement riche en soufre.
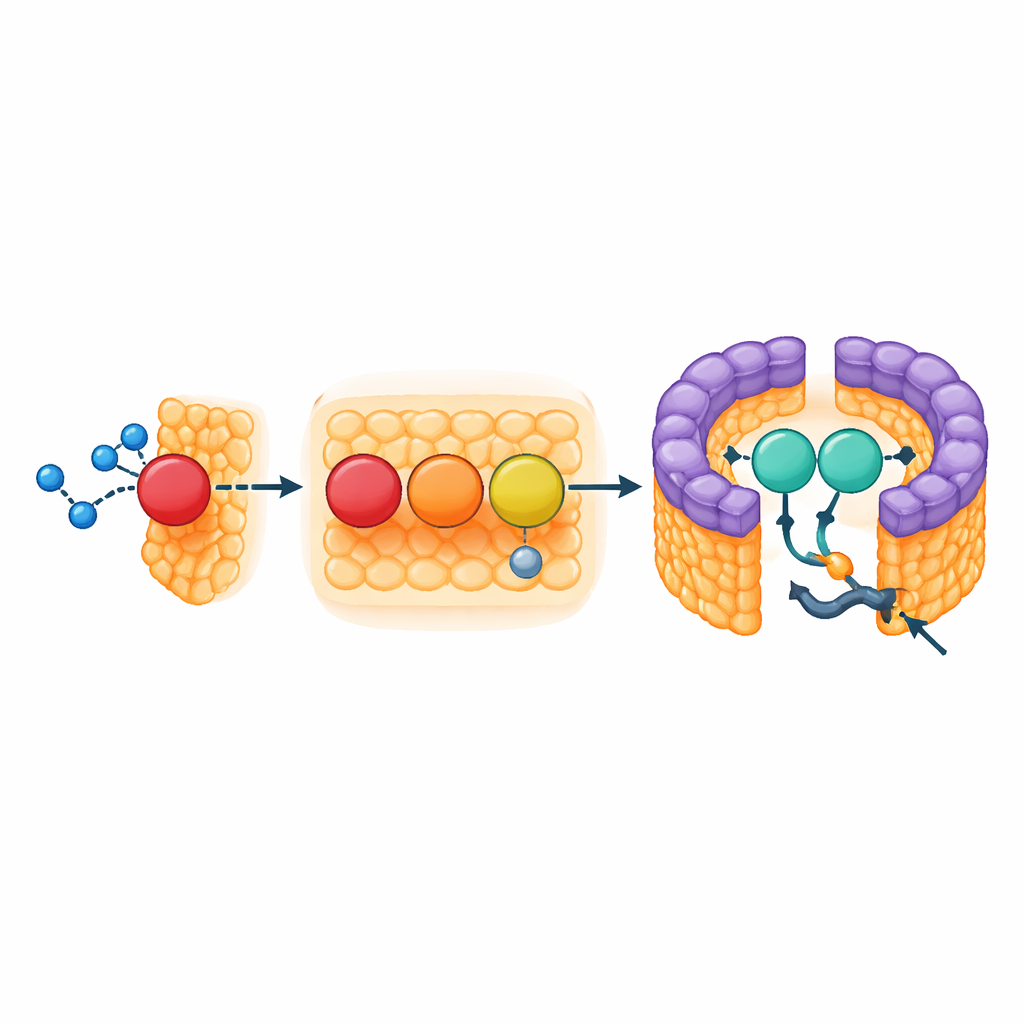
Une pièce d'appui au niveau de l'ouverture de l'anneau
La partie LH1 du complexe forme une barrière serrée et chargée en pigments qui capte la lumière et cannalise l'excitation vers le centre réactionnel, mais son anneau n'est pas complètement fermé. À l'emplacement de l'ouverture se trouvent deux éléments structurels : le début transmembranaire de la sous‑unité cytochrome et une petite protéine à trois hélices que les auteurs nomment protéine‑3h. La protéine‑3h dérive d'un gène plus large de la chaîne respiratoire de la bactérie (un pseudo‑gène connu sous le nom urf1) et semble avoir été réaffectée. Dans le complexe LH1–RC, elle s'engage dans l'ouverture et se fixe à la fois au cytochrome et aux unités de capture de lumière voisines, agissant comme une béquille qui stabilise l'orifice. Parce que les pigments caroténoïdes denses bloquent d'autres voies, cette ouverture sert probablement de seul passage pour les molécules de quinone qui emportent les électrons du centre réactionnel vers le réseau membranaire plus large.
Pourquoi cette micro‑machine est importante
Dans l'ensemble, les résultats montrent comment Rhodovulum sulfidophilum a finement adapté son matériel photosynthétique pour la vie dans des eaux côtières variables et riches en soufre. Il utilise un cytochrome triheme avec un site de liaison métallique inhabituel pour accepter les électrons de manière flexible de différents donneurs, un anneau de capture de lumière étanche pour capter et retenir l'énergie, et une petite protéine à trois hélices recyclée pour stabiliser et façonner la seule voie de sortie pour les transporteurs mobiles. Pour le grand public, le message clé est que même des organismes unicellulaires peuvent évoluer des dispositifs solaires modulaires et complexes dont les pièces sont permutées, raccourcies et réaffectées au fil du temps — offrant des principes de conception naturels pour des systèmes lumineux robustes et efficaces.
Citation: Yue, XY., Wang, GL., Kosaki, S. et al. Structural insights into the photochemistry of the LH1–RC complex from the marine purple phototrophic bacterium Rhodovulum sulfidophilum. Commun Biol 9, 502 (2026). https://doi.org/10.1038/s42003-026-09755-z
Mots-clés: photosynthèse bactérienne, complexe de capture de lumière, transfert d'électrons, cryo‑microscopie électronique, cycle du soufre