Clear Sky Science · de
Strukturelle Einblicke in die Photochemie des LH1–RC-Komplexes der marinen purpurnen phototrophen Bakterie Rhodovulum sulfidophilum
Wie ein winziges Meeresbakterium Licht und Schwefel in Energie verwandelt
In den flachen, schwefelreichen Schlammen der Küstenmeere lebt ein purpurnes Bakterium, das still Chemikalien recycelt und Sonnenlicht einfängt. Diese Studie richtet den Blick auf seine wichtigste Solarmaschine und enthüllt atomare Details dazu, wie Licht erfasst und in nutzbare Energie umgewandelt wird. Das Verständnis dieses natürlichen „Mikro-Solarmoduls“ vertieft nicht nur unser Bild vom Leben in den Ozeanen, sondern liefert auch Ideen für künftige lichtgetriebene Technologien.
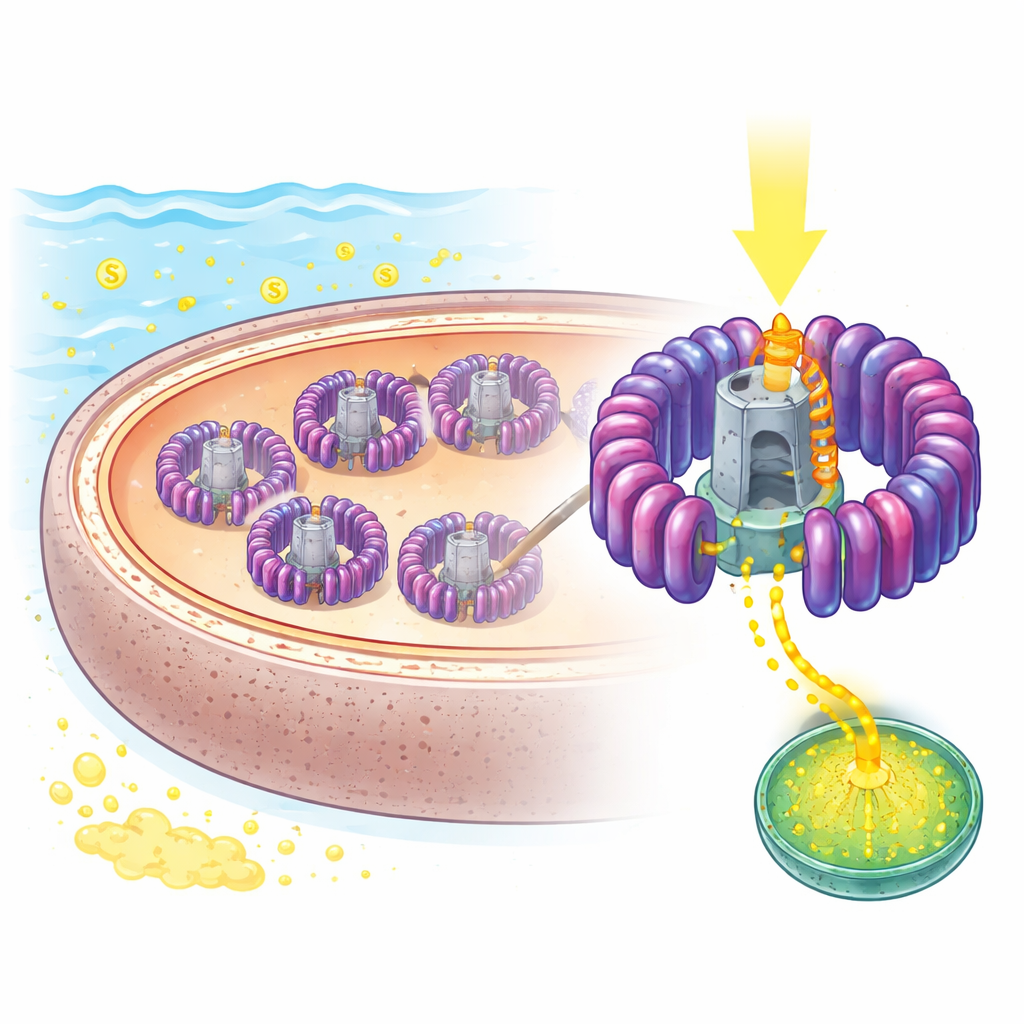
Ein genauer Blick auf die mikroskopische Solarzelle der Natur
Die Forschenden konzentrierten sich auf ein marines Mikroorganismus namens Rhodovulum sulfidophilum, das lange als Modell für bakterielle Photosynthese diente, weil es sowohl in lichtdurchfluteten, sauerstoffarmen wie auch in sauerstoffreichen Bedingungen wachsen kann und hohe Schwefelkonzentrationen toleriert. Seine zentrale lichtnutzende Maschine ist ein kombinierter Light‑Harvesting‑1–Reaktionszentrum‑Komplex, kurz LH1–RC, eingebettet in innere Membranen. Mithilfe hochauflösender Kryo‑Elektronenmikroskopie bestimmten die Autoren die Struktur dieses Komplexes bis auf 1,81 Å — so fein, dass einzelne Pigmente, Lipide und sogar Hunderte Wassermoleküle sichtbar wurden. Sie fanden einen offenen Ring aus 16 wiederkehrenden Lichteinfang‑Einheiten, der ein zentrales Reaktionszentrum umschließt, in dem Ladungstrennung stattfindet, mit einer gezielt angelegten Lücke, die offenbar der einzige Weg für wichtige Moleküle ist, hinein und heraus zu gelangen.
Ein spezieller Draht zum Transport von Elektronen
Im Zentrum des Reaktionszentrums befindet sich eine Proteinsubunit, die wie ein eingebauter Draht für den Elektronentransport wirkt, bekannt als Cytochrom. In vielen verwandten Bakterien trägt dieser Draht vier metallhaltige Häm‑Gruppen, doch bei Rhodovulum sulfidophilum sind es nur drei. Das wirft die Frage auf: Wie können Elektronen effizient fließen ohne das übliche äußerste Häm? Die neue Struktur zeigt, dass das mittlere Häm (als Häm‑2 bezeichnet) durch eine ungewöhnliche Cystein‑Aminosäure ligiert, also gehalten, wird anstelle des in anderen Arten üblichen Methionins. Dieser subtile Austausch senkt sein Redoxpotenzial deutlich und lässt es eher wie das fehlende äußere Häm in anderen Bakterien wirken. Die Oberfläche um dieses Häm ist offen und so geformt, dass lösliche, Elektronen spendende Proteine anlagern können, was darauf hindeutet, dass dies ein wichtiger Landeplatz für eintreffende Elektronen ist.
Ein zusätzliches Metall nahe dem Elektronenpfad
Unerwartet entdeckte das Team ein nicht‑hämbindendes Eisenatom, das dicht an diesem mittleren Häm liegt und von einem Histidin des Cytochroms sowie fünf Wassermolekülen koordiniert wird. Spektroskopische Messungen bestätigten seine Anwesenheit und zeigten, dass es sehr nah an Häm‑2 sitzt, aber weiter von den beiden anderen Hämen entfernt ist. Das legt nahe, dass dieses zusätzliche Eisen als Relaisstation fungieren könnte, die kurzzeitig Elektronen von löslichen Donoren aufnimmt, bevor sie an die Metallzentren des Cytochroms weitergegeben werden. Durch die Kombination von Struktur‑ und Elektronenspinmessungen argumentieren die Autoren, dass Häm‑2, unterstützt von diesem nahegelegenen Eisencluster, der wahrscheinlichste erste Empfänger von Elektronen aus den löslichen Cytochromen des Bakteriums ist und dem Organismus hilft, große Energiedifferenzen zwischen Donoren und Akzeptoren in seiner schwefelreichen Umgebung zu überbrücken.
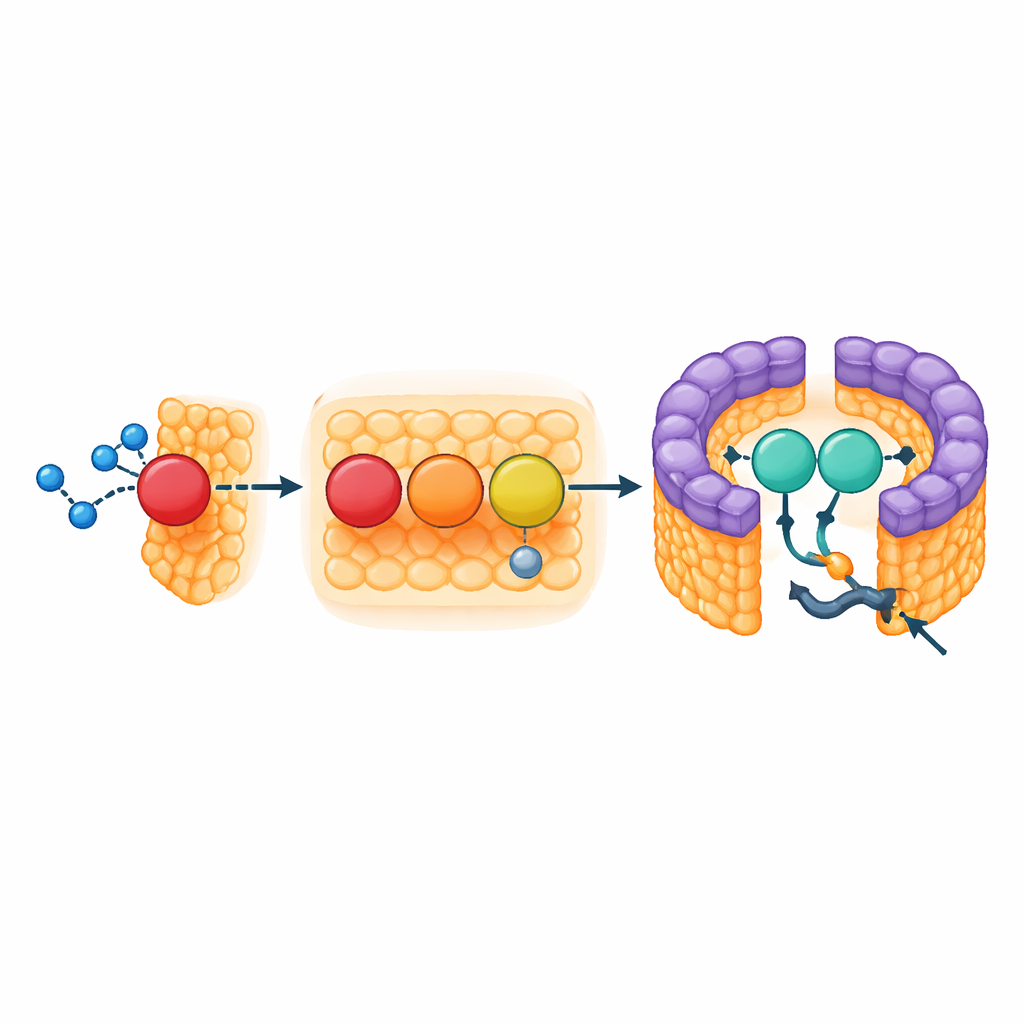
Eine stützende Verstrebung an der Ringöffnung
Der LH1‑Teil des Komplexes bildet einen dichten, pigmentreichen Zaun, der Licht einfängt und die Anregung zum Reaktionszentrum leitet, doch sein Ring ist nicht vollständig geschlossen. An der Lücke sitzen zwei strukturelle Elemente: der membranüberspannende Beginn der Cytochrom‑Subunit und ein kleines Drei‑Helix‑Protein, das die Autoren Protein‑3h nennen. Protein‑3h stammt von einem größeren Gen in der respiratorischen Kette des Bakteriums (einem Pseudogen, bekannt als urf1) und scheint umfunktioniert worden zu sein. Im LH1–RC‑Komplex klemmt es sich in die Lücke und greift sowohl das Cytochrom als auch benachbarte Lichtsammlungs‑Einheiten, wirkt damit als Verstrebung, die die Öffnung stabilisiert. Da die dichten Carotinoid‑Pigmente andere Wege blockieren, dient diese Öffnung wahrscheinlich als einziges Tor für Chinonmoleküle, die Elektronen vom Reaktionszentrum in das weitere Membrannetzwerk transportieren.
Warum diese Mikromaschine wichtig ist
In der Summe zeigen die Ergebnisse, wie Rhodovulum sulfidophilum seine photosynthetische Hardware für das Leben in variablen, schwefelreichen Küstengewässern fein abgestimmt hat. Es verwendet ein Trihämmcytochrom mit einer ungewöhnlichen Metallbindungsstelle, um Elektronen flexibel von verschiedenen Donoren aufzunehmen, einen dicht schließenden Lichtsammlungsring, um Energie einzufangen und zu halten, und ein umfunktioniertes Drei‑Helix‑Protein, das sowohl die einzige Austrittsroute für bewegliche Elektronenträger stabilisiert als auch formt. Für Nicht‑Spezialisten ist die Kernbotschaft: Selbst einzellige Organismen können komplexe, modulare Solargeräte entwickeln, deren Teile über die Zeit ausgetauscht, verkleinert und neu zugewiesen werden — und sie liefern damit natürliche Gestaltungsprinzipien für robuste, effiziente lichtgetriebene Systeme.
Zitation: Yue, XY., Wang, GL., Kosaki, S. et al. Structural insights into the photochemistry of the LH1–RC complex from the marine purple phototrophic bacterium Rhodovulum sulfidophilum. Commun Biol 9, 502 (2026). https://doi.org/10.1038/s42003-026-09755-z
Schlüsselwörter: bakterielle Photosynthese, Lichtsammlungskomplex, Elektronentransfer, Kryo-Elektronenmikroskopie, Schwefelkreislauf