Clear Sky Science · es
Perspectivas estructurales sobre la fotocatálisis del complejo LH1–RC de la bacteria fototrófica púrpura marina Rhodovulum sulfidophilum
Cómo una diminuta bacteria marina convierte la luz y el azufre en energía
En los lodos someros y ricos en azufre de las zonas costeras vive una bacteria púrpura que recicla químicos y captura la luz solar de forma silenciosa. Este estudio se centra en su principal máquina solar, revelando detalles a nivel atómico de cómo se cosecha la luz y se convierte en energía utilizable. Comprender este “micro‑panel solar” natural no solo amplía nuestra imagen de la vida en los océanos, sino que también ofrece inspiración para futuras tecnologías impulsadas por la luz.
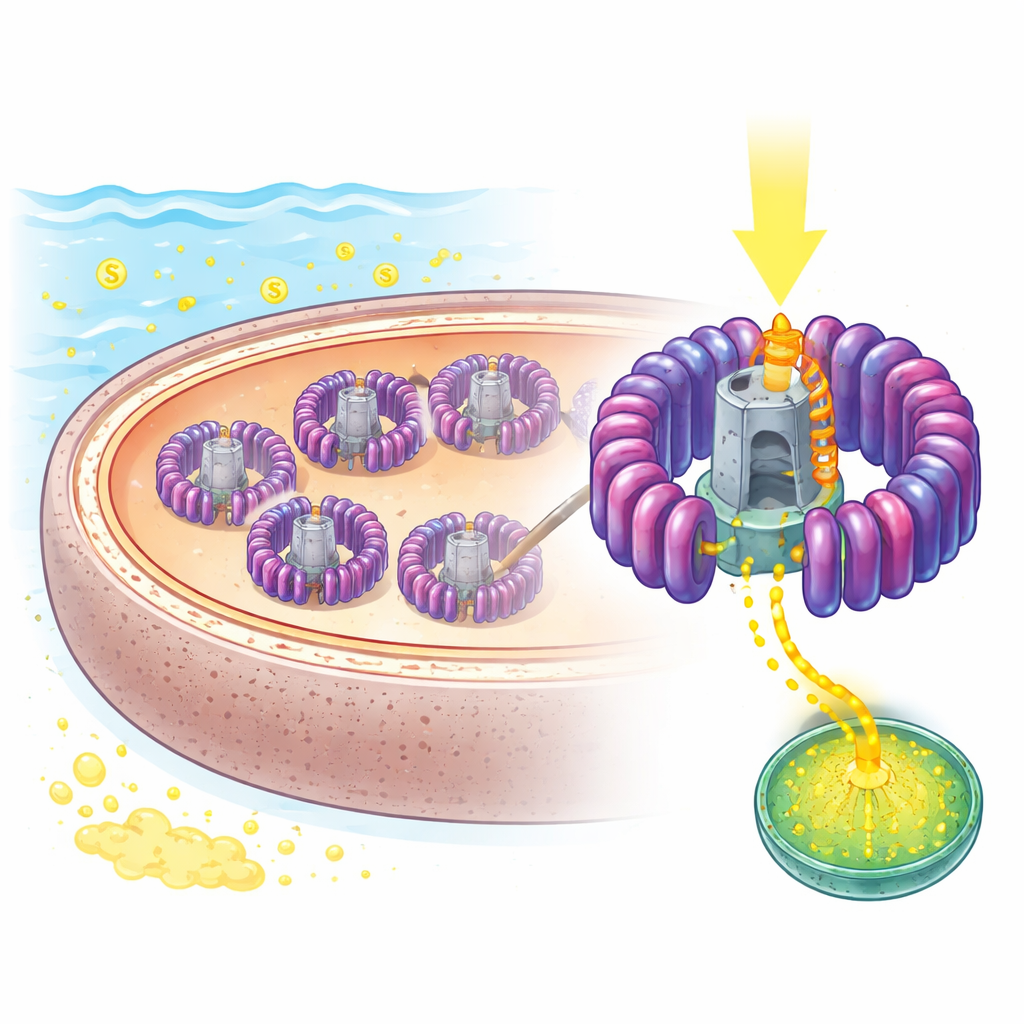
Una mirada cercana al micro panel solar de la naturaleza
Los investigadores se centraron en un microbio marino llamado Rhodovulum sulfidophilum, utilizado desde hace tiempo como modelo de fotosíntesis bacteriana porque puede crecer tanto en condiciones iluminadas pobres en oxígeno como en ambientes totalmente oxigenados, y tolera altos niveles de azufre. Su máquina central de uso de la luz es un complejo combinado de captación de luz 1 y centro de reacción, o LH1–RC, incrustado en membranas internas. Mediante crio‑microscopía electrónica de alta resolución, el equipo determinó la estructura de este complejo hasta 1,81 Å—lo suficientemente detallada para ver pigmentos individuales, lípidos e incluso cientos de moléculas de agua. Encontraron un anillo abierto de 16 unidades repetidas de captación de luz rodeando un centro de reacción central donde se produce la separación de cargas, con una abertura deliberada que parece ser la única vía para que moléculas clave entren y salgan.
Un cable especial para mover electrones
En el corazón del centro de reacción hay una subunidad proteica que actúa como un cable integrado para mover electrones, conocida como citocromo. En muchas bacterias emparentadas este cable porta cuatro grupos hemo con metal, pero en Rhodovulum sulfidophilum solo hay tres. Esto planteó un enigma: ¿cómo pueden fluir los electrones de forma eficiente sin el hemo exterior habitual? La nueva estructura muestra que el hemo medio (llamado hemo‑2) está ligado, o coordinado, por una cisteína inusual en lugar de la metionina observada en otras especies. Este sutil intercambio reduce mucho su potencial redox, haciendo que se comporte más como el hemo exterior ausente en otras bacterias. La superficie alrededor de este hemo está abierta y formada para permitir que proteínas solubles donadoras de electrones se acerquen, sugiriendo que este es un sitio clave de aterrizaje para electrones entrantes.
Un ayudante metálico adicional cerca de la vía de electrones
De forma inesperada, el equipo descubrió un átomo de hierro no‑hemo ubicado cerca de este hemo medio, coordinado por una histidina del citocromo y cinco moléculas de agua. Mediciones espectroscópicas confirmaron su presencia y mostraron que se sitúa muy cerca del hemo‑2, pero más alejado de los otros dos hemos. Esto sugiere que el hierro adicional puede actuar como una estación de retransmisión, aceptando brevemente electrones de donantes solubles antes de pasarlos a los centros metálicos del citocromo. Al combinar mediciones estructurales y de espín electrónico, los autores sostienen que el hemo‑2, ayudado por este cúmulo de hierro cercano, es el receptor más probable inicial de electrones procedentes de los citocromos solubles de la bacteria, ayudando al organismo a lidiar con grandes diferencias de energía entre donantes y aceptores en su entorno rico en azufre.
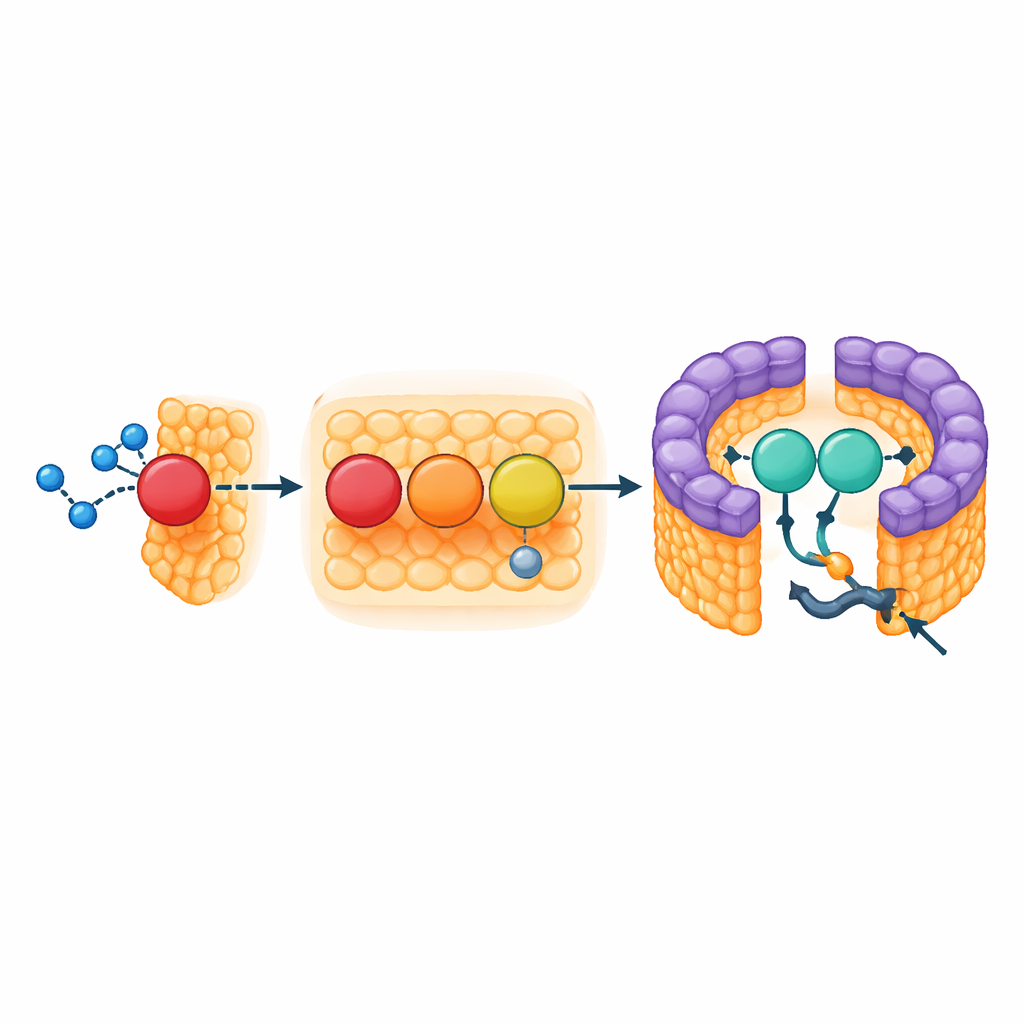
Un soporte que refuerza la abertura del anillo
La parte LH1 del complejo forma una valla compacta cargada de pigmentos que captura la luz y canaliza la excitación al centro de reacción, pero su anillo no está completamente cerrado. En la abertura se sitúan dos elementos estructurales: el inicio que atraviesa la membrana de la subunidad citocromo y una pequeña proteína de tres hélices que los autores denominan proteína‑3h. La proteína‑3h proviene de un gen mayor en la cadena respiratoria de la bacteria (un pseudo‑gen conocido como urf1) y parece haber sido reutilizada. En el complejo LH1–RC, se encaja en la abertura y se aferra tanto al citocromo como a las unidades captoras de luz vecinas, actuando como un soporte que estabiliza la apertura. Dado que los densos pigmentos carotenoides bloquean otras rutas, esta abertura probablemente sirve como la única puerta de acceso para las moléculas de quinona que transportan electrones fuera del centro de reacción hacia la red de membranas circundante.
Por qué importa esta micro máquina
En conjunto, los resultados muestran cómo Rhodovulum sulfidophilum ha afinado su hardware fotosintético para la vida en aguas costeras variables y ricas en azufre. Usa un citocromo trihemo con un sitio de unión metálica inusual para aceptar electrones de forma flexible de distintos donantes, un anillo de captación de luz compactamente sellado para capturar y retener energía, y una proteína reaprovechada de tres hélices para estabilizar y dar forma a la única salida para los portadores móviles. Para el público general, el mensaje clave es que incluso los organismos unicelulares pueden evolucionar dispositivos solares modulares e intrincados cuyos componentes se intercambian, recortan y reorientan con el tiempo—ofreciendo principios de diseño naturales para sistemas eficientes y robustos impulsados por la luz.
Cita: Yue, XY., Wang, GL., Kosaki, S. et al. Structural insights into the photochemistry of the LH1–RC complex from the marine purple phototrophic bacterium Rhodovulum sulfidophilum. Commun Biol 9, 502 (2026). https://doi.org/10.1038/s42003-026-09755-z
Palabras clave: fotosíntesis bacteriana, complejo captador de luz, transferencia de electrones, crio‑microscopía electrónica, ciclo del azufre