Clear Sky Science · pt
Insights estruturais sobre a fotossíntese do complexo LH1–RC da bactéria fototrófica marinha Rhodovulum sulfidophilum
Como uma Pequena Bactéria Marinha Converte Luz e Enxofre em Energia
Nos lodos rasos e ricos em enxofre dos mares costeiros vive uma bactéria roxa que recicla produtos químicos discretamente e captura a luz do sol. Este estudo foca sua principal máquina solar, revelando detalhes ao nível atômico de como a luz é captada e convertida em energia utilizável. Compreender esse “micro‑painel solar” natural aprofunda nossa visão da vida nos oceanos e oferece inspiração para futuras tecnologias movidas por luz.
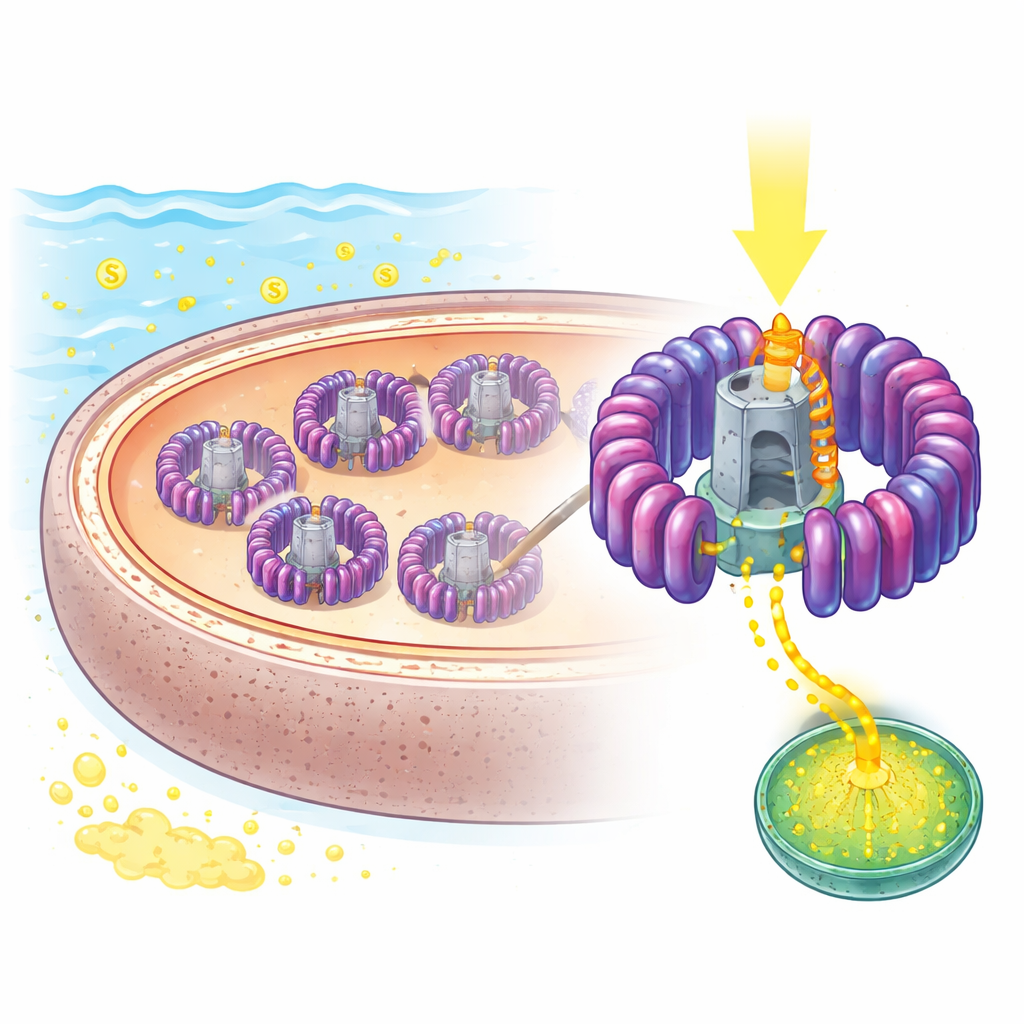
Um Olhar Detalhado no Micro Painel Solar da Natureza
Os pesquisadores se concentraram em um micro-organismo marinho chamado Rhodovulum sulfidophilum, usado há muito tempo como modelo para a fotossíntese bacteriana porque pode crescer tanto em condições iluminadas com pouco oxigênio quanto em ambientes totalmente oxigenados, além de tolerar altos níveis de enxofre. Sua máquina central de uso da luz é um complexo combinado de captação de luz 1–centro de reação, ou LH1–RC, embutido nas membranas internas. Usando crio‑microscopia eletrônica de alta resolução, a equipe determinou a estrutura desse complexo até 1,81 Å — detalhe suficiente para ver pigmentos individuais, lipídios e até centenas de moléculas de água. Eles encontraram um anel aberto com 16 unidades repetitivas de captação de luz envolvendo um centro de reação central onde ocorre a separação de cargas, com uma lacuna deliberada que parece ser o único caminho para que moléculas-chave entrem e saiam.
Um Cabo Especial para Movimentar Elétrons
No centro do centro de reação está uma subunidade proteica que atua como um fio embutido para movimentar elétrons, conhecida como citocromo. Em muitas bactérias relacionadas, esse fio carrega quatro grupos heme com metal, mas em Rhodovulum sulfidophilum há apenas três. Isso levantou um mistério: como os elétrons podem fluir eficientemente sem o heme mais externo habitual? A nova estrutura mostra que o heme do meio (chamado heme‑2) é ligado, ou mantido, por um aminoácido cisteína incomum em vez da metionina vista em outras espécies. Essa troca sutil reduz muito seu potencial redox, fazendo com que se comporte mais como o heme externo ausente em outras bactérias. A superfície ao redor desse heme é aberta e moldada para permitir que proteínas solúveis doadoras de elétrons se aproximem, sugerindo que esse é um local chave de pouso para elétrons entrantes.
Um Metal Auxiliar Extra Perto da Rota de Elétrons
De forma inesperada, a equipe descobriu um átomo de ferro não‑heme aninhado próximo a esse heme do meio, coordenado por uma histidina do citocromo e cinco moléculas de água. Medidas espectroscópicas confirmaram sua presença e mostraram que ele fica muito próximo ao heme‑2, mas mais distante dos outros dois hemes. Isso sugere que o ferro extra pode atuar como uma estação de retransmissão, aceitando brevemente elétrons de dadores solúveis antes de passá‑los para os centros metálicos do citocromo. Ao combinar dados estruturais e medições de spin eletrônico, os autores argumentam que o heme‑2, auxiliado por esse cluster de ferro próximo, é o receptor mais provável inicial dos elétrons dos citocromos solúveis da bactéria, ajudando o organismo a lidar com grandes diferenças energéticas entre dadores e aceitadores em seu ambiente rico em enxofre.
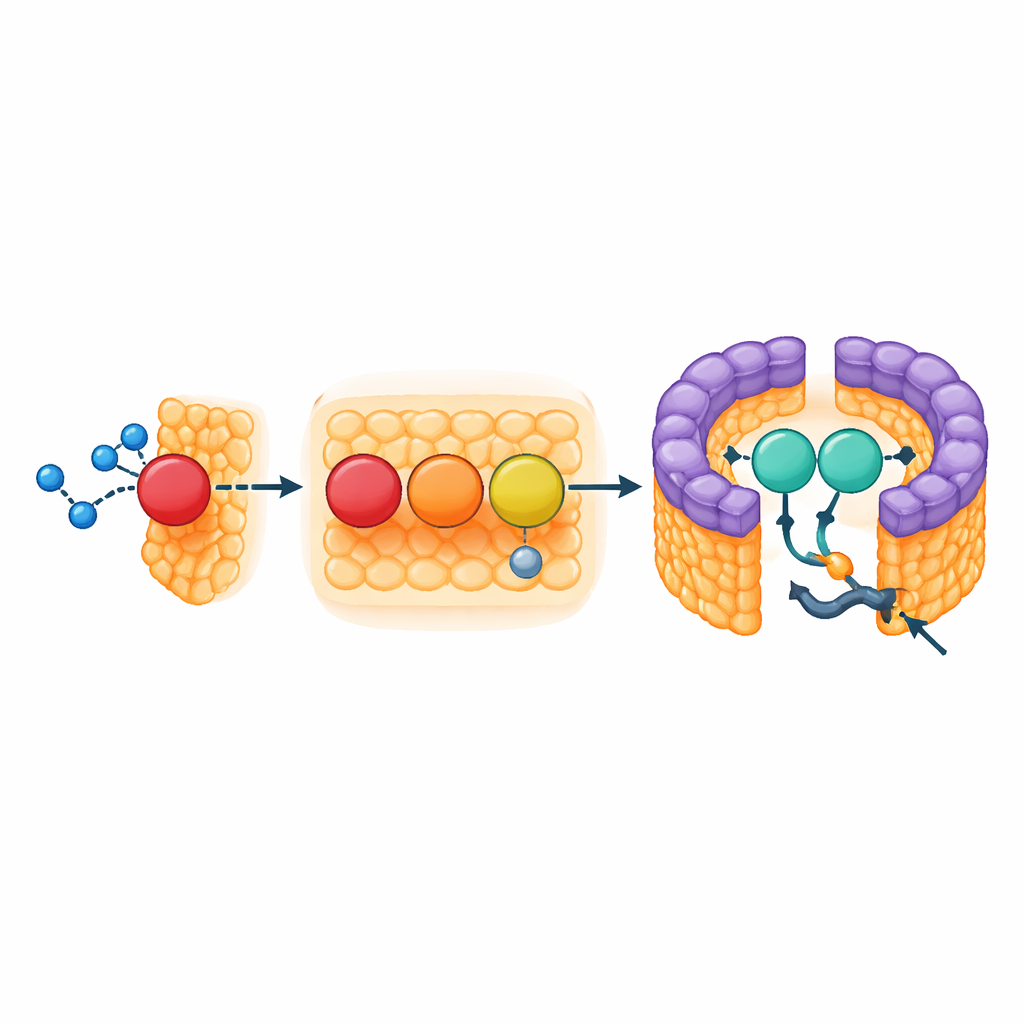
Uma Viga de Suporte na Abertura do Anel
A parte LH1 do complexo forma uma cerca compacta carregada de pigmentos que captura a luz e canaliza a excitação até o centro de reação, mas seu anel não está totalmente fechado. Na lacuna situam‑se dois elementos estruturais: o início transmembrana da subunidade do citocromo e uma pequena proteína de três hélices que os autores chamam de protein‑3h. A protein‑3h deriva de um gene maior na cadeia respiratória da bactéria (um pseudo‑gene conhecido como urf1) e parece ter sido reaproveitada. No complexo LH1–RC, ela se encaixa na abertura e se prende tanto ao citocromo quanto às unidades vizinhas de captação de luz, atuando como um escoramento que estabiliza a abertura. Como os pigmentos carotenoides densos bloqueiam outras rotas, essa abertura provavelmente serve como o único portão para moléculas de quinona que transportam elétrons para fora do centro de reação e para a rede de membrana mais ampla.
Por Que Esta Micro Máquina é Importante
Em conjunto, os resultados mostram como Rhodovulum sulfidophilum afinou seu hardware fotossintético para a vida em águas costeiras variáveis e ricas em enxofre. Ela usa um citocromo triheme com um sítio de ligação metálica incomum para aceitar elétrons de forma flexível de diferentes dadores, um anel de captura de luz hermeticamente fechado para captar e reter energia, e uma proteína de três hélices reaproveitada para estabilizar e modelar a única via de saída para transportadores móveis. Para não especialistas, a mensagem principal é que mesmo organismos unicelulares podem evoluir dispositivos solares intrincados e modulares cujas peças são trocadas, reduzidas e reatribuídas ao longo do tempo — oferecendo princípios de design natural para sistemas movidos por luz que sejam robustos e eficientes.
Citação: Yue, XY., Wang, GL., Kosaki, S. et al. Structural insights into the photochemistry of the LH1–RC complex from the marine purple phototrophic bacterium Rhodovulum sulfidophilum. Commun Biol 9, 502 (2026). https://doi.org/10.1038/s42003-026-09755-z
Palavras-chave: fotossíntese bacteriana, complexo de captação de luz, transferência de elétrons, crio microscopia eletrônica, ciclo do enxofre