Clear Sky Science · ru
Снижение индуцирования профагов, связанного с ROS, в мутанте lepA способствует увеличению персистентности к фторхинолонам у Salmonella Typhimurium
Почему некоторые бактерии переживают даже самые сильные лекарства
Когда врачи применяют мощные антибиотики для лечения тяжёлых инфекций, большинство бактерий гибнет быстро. Тем не менее крошечное меньшинство способно перейти в состояние покоя, переждать атаку и затем снова разрасти инфекцию. Эти стойкие выжившие, называемые персистентными клетками, не несут классических генов устойчивости, поэтому их трудно предсказать и ещё труднее уничтожить. В этом исследовании рассматривается, почему некоторые штаммы Salmonella с большей вероятностью образуют персистеры во время лечения широко используемым фторхинолоном ципрофлоксацином, и как крошечные выбросы химически реактивных форм кислорода и скрытые вирусы внутри бактерий могут изменить баланс между гибелью и выживанием.
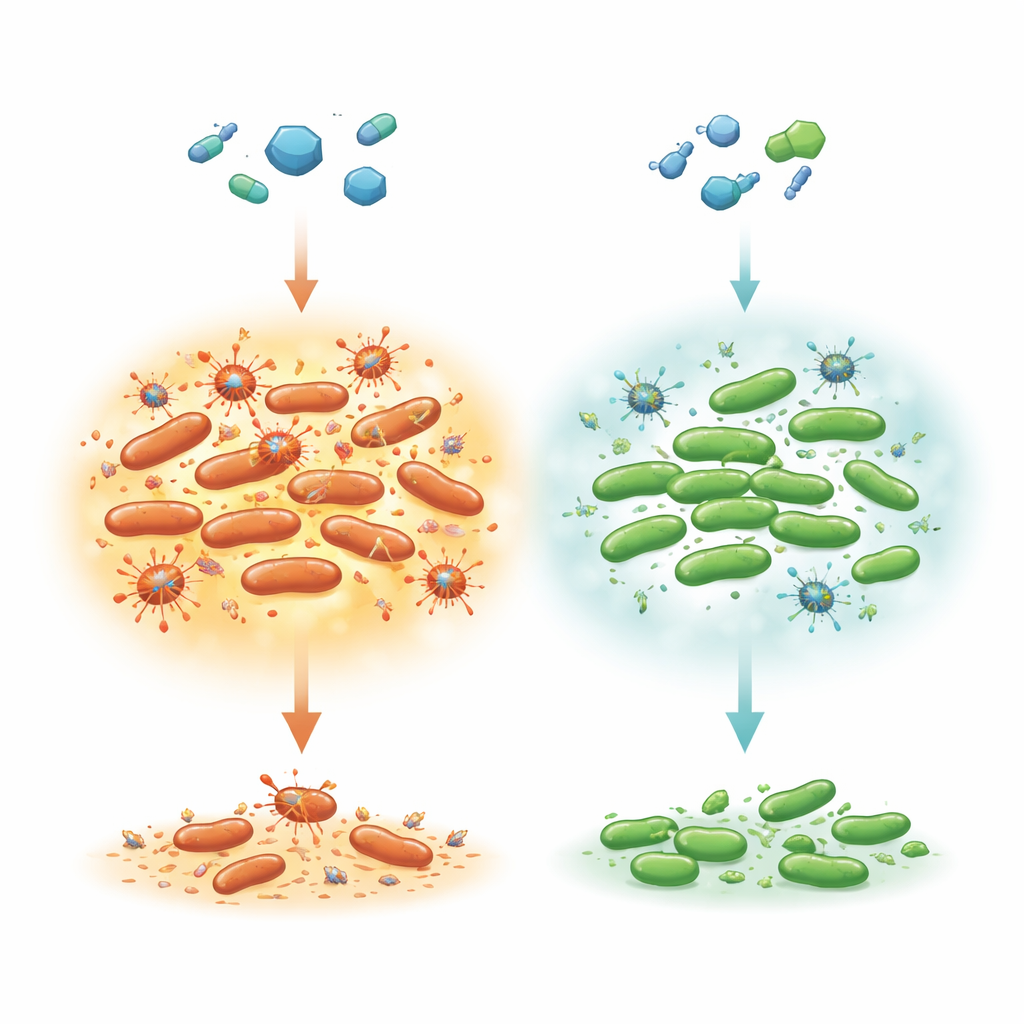
Скрытые выжившие внутри антибиотиковой атаки
Большинство бактерий в популяции быстро уничтожаются эффективным антибиотиком, но очень маленькая субпопуляция гибнет намного медленнее. Этот «двухступенчатый» профиль гибели характерен для персистентных клеток, которые просто затаиваются, пока препарат не исчезнет, а затем возобновляют нормальный рост. Авторы сосредоточились на Salmonella Typhimurium, частой причине пищевых инфекций, требующей лечения ципрофлоксацином у уязвимых пациентов. Ранее в Escherichia coli было показано, что удаление фактора трансляции LepA делает клетки необычно толерантными к нескольким антибиотикам за счёт снижения накопления реактивных форм кислорода (ROS) — химически агрессивных побочных продуктов метаболизма, которые могут повреждать ДНК и белки. Здесь исследователи спросили, играет ли LepA схожую роль в Salmonella и как это взаимодействует с вирусами (профагами), находящимися в скрытом состоянии в хромосоме бактерии.
Что изменилось в бактериях без одного белка
Команда сравнила нормальную Salmonella с вариантом, лишённым гена lepA. Они подвергли обе штамма трем главным классам бактерицидных антибиотиков: ципрофлоксацину (фторхинолон), ампициллину (бета-лактам) и канамицину (аминогликозид). При ампициллине и канамицине оба штамма вели себя похоже: наблюдалось обычное быстрое убывание большинства клеток и плато редких персистеров. Напротив, после лечения ципрофлоксацином мутант lepA стабильно оставлял больше персистентов, чем нормальный штамм. Измерения ROS с помощью флуоресцентного красителя показали, что ципрофлоксацин вызывает сильное образование ROS, особенно гидроксильных радикалов, и что эти уровни были ниже в мутанте lepA. Тесты потребления кислорода показали, что мутантные клетки наращивали дыхание — а значит и производство ROS — медленнее, что предполагает: тонкие дефекты в энергетическом аппарате клетки уменьшают окислительный стресс и способствуют выживанию под давлением препарата.
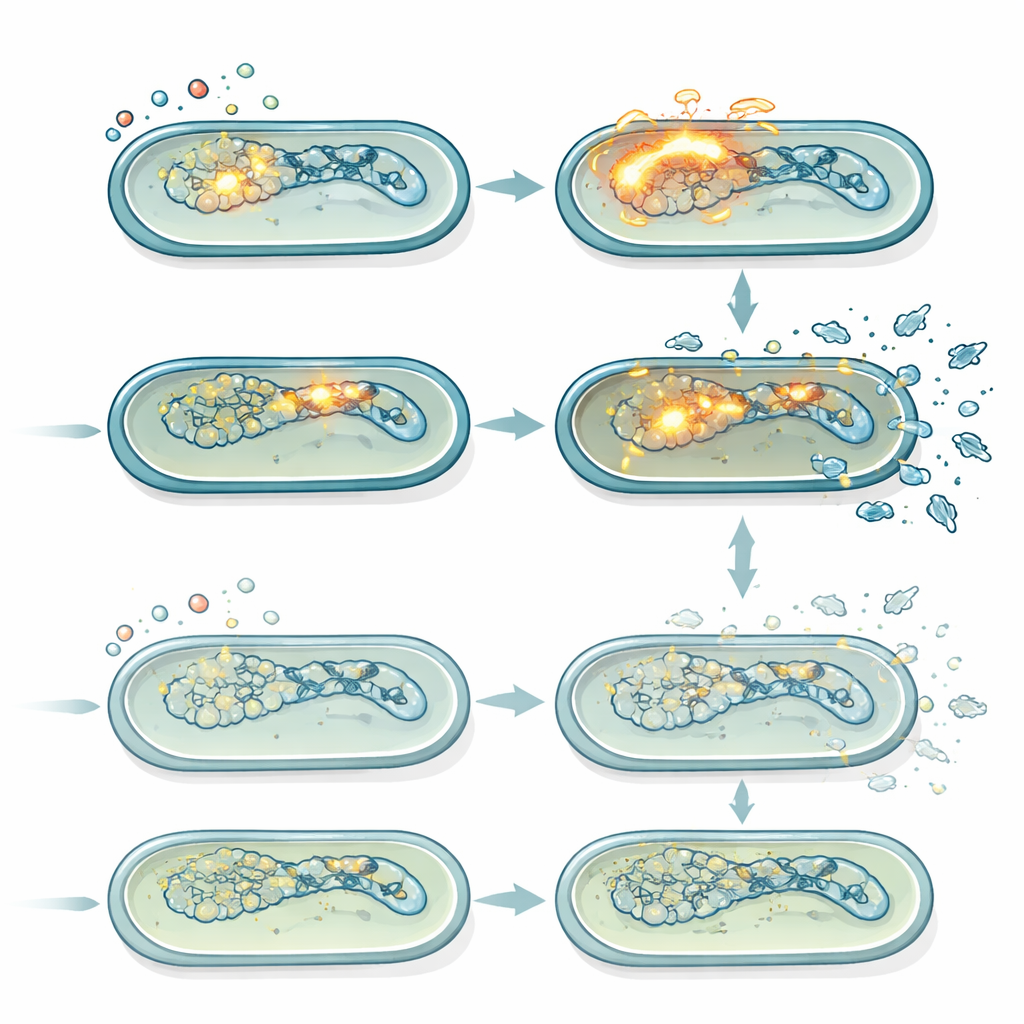
Молчащие вирусы, становящиеся летальными под стрессом
Salmonella Typhimurium несёт несколько профагов — скрытых вирусных геномов, которые могут пробудиться при повреждении бактериальной ДНК. При активации эти профаги переходят в литический цикл, реплицируются и приводят к разрыву клетки-хозяина. С помощью измерения экспрессии генов и флуоресцентных репортерных штаммов авторы показали, что ципрофлоксацин сильно активировал SOS-ответ на повреждение ДНК и в нормальных клетках вызывал мощную индукцию одного профага в частности (Gifsy-1). Эта индукция была слабее в мутанте lepA, что соответствовало его сниженным уровням ROS. Плейк-ассеи, подсчитывающие активные фаговые частицы, подтвердили, что при умеренных дозах ципрофлоксацина нормальный штамм стабильно производил больше фагов со временем, чем мутант lepA. Когда все профаги были генетически удалены, преимущество выживания мутанта lepA при умеренных дозах ципрофлоксацина в значительной мере исчезло, что показало: ключевое различие между штаммами заключалось в том, насколько сильно ROS-опосредованная индукция профагов способствовала гибели.
Понижение оксидативного стресса меняет, кто остаётся в живых
Затем исследователи использовали глутатион, природный антиоксидант, чтобы ослабить ROS во время лечения ципрофлоксацином. У нормальных Salmonella, несущих профаги, глутатион увеличивал долю клеток, не проявлявших индукцию профагов, и повышал фракцию персистеров. В фоне без профагов то же лечение замедляло раннюю гибель, но уже не увеличивало уровень персистеров, подчёркивая, что преимущество выживания было связано с подавлением профагов. При очень высоких дозах ципрофлоксацина антиоксиданты снова увеличивали выживаемость гораздо сильнее в клетках с профагами, чем в безпрофаговых, указывая на то, что ROS-индуцированная активация профагов может быть важна даже при интенсивном давлении препарата. Подобные закономерности наблюдались и в штаммах E. coli, несущих известный профаг лямбда: ципрофлоксацин, но не ампициллин, вызвал лизис, опосредованный профагом, и снизил число персистеров в нормальных клетках, тогда как мутанты lepA и штаммы без профагов избегали этого дополнительного уничтожения.
Что это значит для борьбы с упорными инфекциями
Работа поддерживает простую, но мощную идею: у бактерий, несущих скрытые профаги, антибиотик-индуцированные ROS могут подтолкнуть эти вирусы к действию, добавив дополнительную волну уничтожения, которая сокращает пул лекарственно-толерантных персистеров. У Salmonella, лишённых LepA, более низкие уровни ROS означают слабую активацию профагов и больше клеток, которые тихо переживают терапию ципрофлоксацином. Это указывает на то, что в некоторых условиях аккуратно направленное использование ROS и профагов могло бы сделать существующие антибиотики более эффективными — концепция, известная как синергия фагов и антибиотиков. В то же время повышение ROS несёт риски, поскольку профаги могут также распространять гены вирулентности и устойчивости среди других бактерий. Исследование подчёркивает, как одна бактериальная белковая составляющая, состояние метаболизма клетки и наличие скрытых вирусов совместно определяют, очистит ли курс антибиотиков инфекцию или оставит после себя выживших, которые могут вызвать проблемы позже.
Цитирование: Braetz, S., Karp, M., Nerlich, A. et al. Reduced ROS-associated prophage induction in a lepA mutant contributes to increased fluoroquinolone persistence in Salmonella Typhimurium. Sci Rep 16, 12721 (2026). https://doi.org/10.1038/s41598-026-47552-0
Ключевые слова: персистентность к антибиотикам, реактивные формы кислорода, профаги, Salmonella Typhimurium, ципрофлоксацин