Clear Sky Science · it
Ridotta induzione di profagi associata ai ROS in un mutante lepA contribuisce all'aumentata persistenza ai fluoroquinoloni in Salmonella Typhimurium
Perché alcuni germi sopravvivono anche ai nostri farmaci più potenti
Quando i medici usano antibiotici potenti per trattare infezioni gravi, la maggior parte dei batteri muore rapidamente. Eppure una piccolissima minoranza può entrare in uno stato dormiente, resistere all'attacco e poi ricrescere causando una recidiva. Questi sopravvissuti tenaci, chiamati cellule persister, non possiedono i classici geni di resistenza, perciò sono difficili da prevedere e ancora più difficili da eliminare. Questo studio indaga perché certi ceppi di Salmonella tendono a formare più persister durante il trattamento con la ciprofloxacina, un fluoroquinolone molto usato, e come piccoli scoppi di ossigeno chimicamente reattivo e virus nascosti all'interno dei batteri possano spostare l'equilibrio tra morte e sopravvivenza.
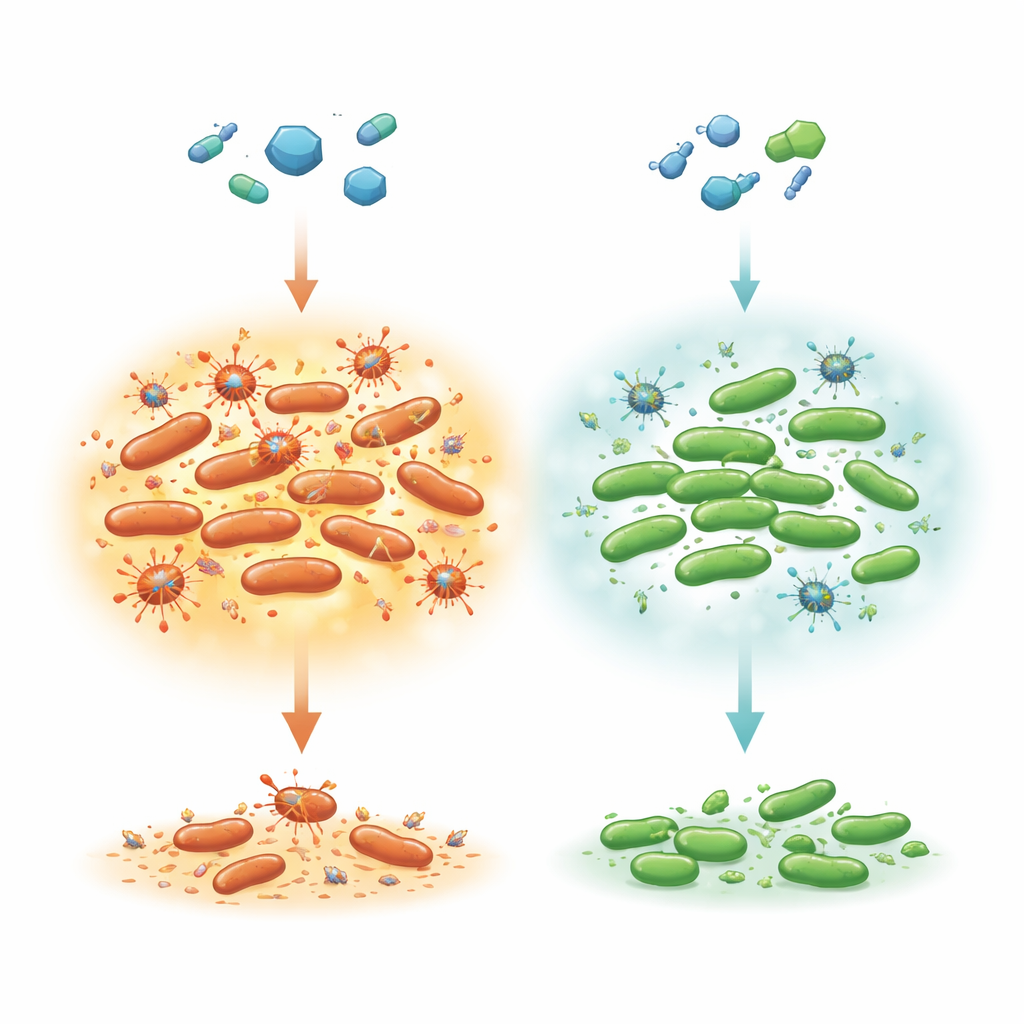
Sopravvissuti nascosti durante un attacco antibiotico
La maggior parte dei batteri in una popolazione viene rapidamente uccisa da un antibiotico efficace, ma una sottopopolazione molto piccola muore molto più lentamente. Questo schema di uccisione “in due fasi” è tipico delle cellule persister, che si rintanano fino alla scomparsa del farmaco per poi riprendere a crescere. Gli autori si sono concentrati su Salmonella Typhimurium, una causa comune di infezioni alimentari che può richiedere il trattamento con ciprofloxacina in soggetti vulnerabili. Lavori precedenti in Escherichia coli avevano suggerito che la rimozione di un fattore di traduzione chiamato LepA rendeva le cellule insolita-mente tolleranti a vari antibiotici riducendo l'accumulo di specie reattive dell'ossigeno (ROS) — sottoprodotti metabolici chimicamente aggressivi che possono danneggiare DNA e proteine. Qui i ricercatori hanno chiesto se LepA svolga un ruolo simile in Salmonella e come questo interagisca con i virus (profagi) che giacciono dormienti all'interno del cromosoma batterico.
Cosa è cambiato nei batteri privi di una singola proteina
Il gruppo ha confrontato Salmonella normale con una versione priva del gene lepA. Entrambe sono state esposte a tre principali classi di antibiotici battericidi: ciprofloxacina (un fluoroquinolone), ampicillina (un beta-lattamico) e kanamicina (un aminoglicoside). Per ampicillina e kanamicina, entrambi i ceppi si comportavano in modo simile, mostrando la consueta rapida mortalità della maggior parte delle cellule e un plateau di rari persister. Al contrario, dopo il trattamento con ciprofloxacina, il mutante lepA lasciava costantemente più cellule persister rispetto al ceppo normale. Misurazioni dei ROS tramite un colorante fluorescente hanno mostrato che la ciprofloxacina induceva una forte formazione di ROS, in particolare radicali ossidrile, e che questi livelli erano inferiori nel mutante lepA. Saggi sul consumo di ossigeno indicavano che le cellule mutanti aumentavano la respirazione — e quindi la produzione di ROS — più lentamente, suggerendo che difetti sottili nella macchina energetica cellulare mantengono lo stress ossidativo più basso e favoriscono la sopravvivenza sotto pressione farmacologica.
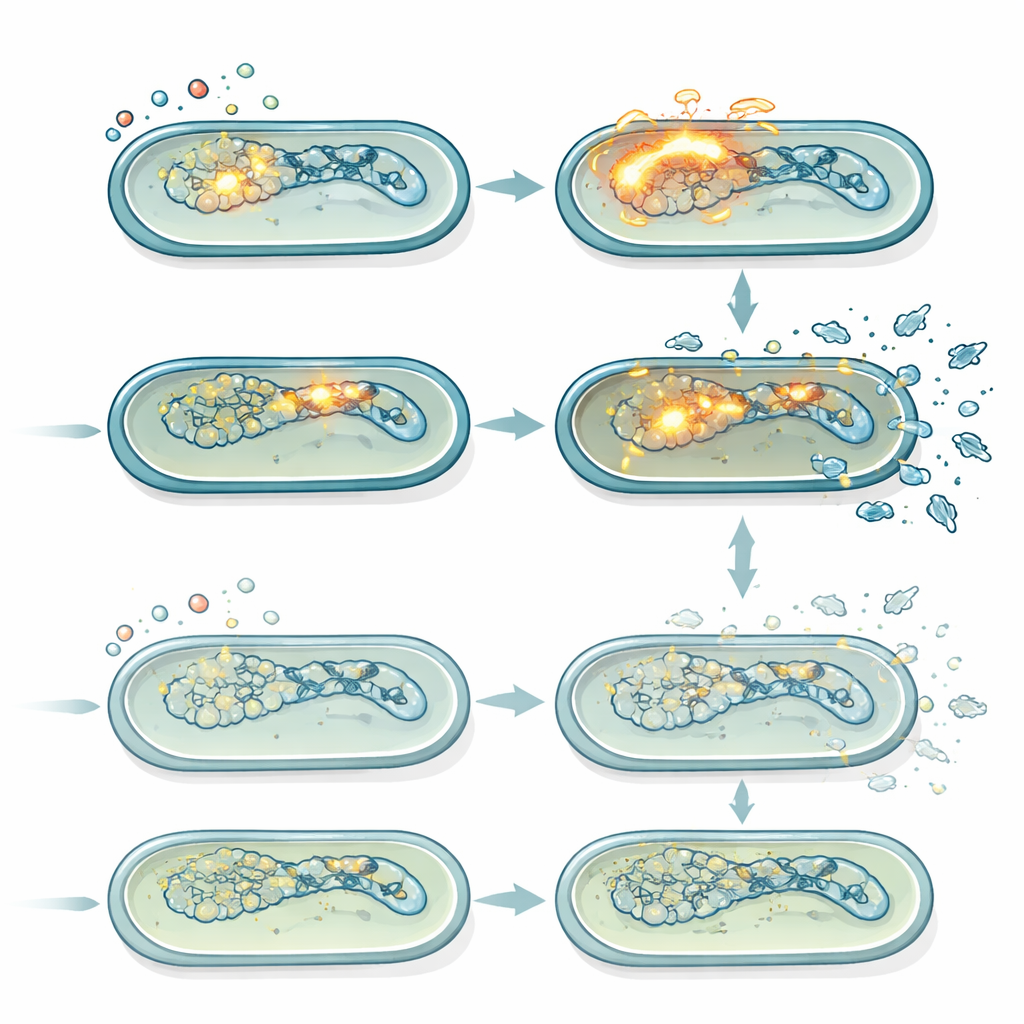
Virus silenziosi che diventano letali sotto stress
Salmonella Typhimurium ospita diversi profagi, genomi virali dormienti che possono risvegliarsi quando il DNA batterico è danneggiato. Una volta attivati, questi profagi passano a un programma litico, si replicano e provocano la lisi della cellula ospite. Usando misure di espressione genica e ceppi reporter fluorescenti, gli autori hanno mostrato che la ciprofloxacina attivava fortemente la risposta SOS al danno del DNA e, nelle cellule normali, induceva in modo robusto l'attivazione di un profago in particolare (Gifsy-1). Questa induzione era più debole nel mutante lepA, coerentemente con i suoi livelli più bassi di ROS. Saggi di placca che contano le particelle fagiche attive confermavano che, a dosi moderate di ciprofloxacina, il ceppo normale produceva progressivamente più fagi nel tempo rispetto al mutante lepA. Quando tutti i profagi venivano rimossi geneticamente, il vantaggio di sopravvivenza del mutante lepA a dosi moderate di ciprofloxacina svaniva in gran parte, rivelando che la differenza chiave tra i ceppi era quanto l'attivazione dei profagi guidata dai ROS contribuisse alla morte.
Abbassare lo stress ossidativo cambia chi sopravvive
I ricercatori hanno poi utilizzato il glutatione, un antiossidante naturale, per attenuare i ROS durante il trattamento con ciprofloxacina. Nella Salmonella normale che portava profagi, il glutatione ha ampliato la sottopopolazione di cellule che non mostravano induzione dei profagi e ha aumentato la frazione di persister. In uno sfondo privo di profagi, lo stesso trattamento ha rallentato l'uccisione iniziale ma non ha più aumentato i livelli di persister, sottolineando che il beneficio di sopravvivenza era legato alla soppressione dei profagi. A dosi molto elevate di ciprofloxacina, gli antiossidanti aumentarono nuovamente la sopravvivenza molto più nelle cellule portatrici di profagi rispetto a quelle senza profagi, indicando che l'attivazione dei profagi indotta dai ROS può essere importante anche sotto una forte pressione farmacologica. Pattern simili sono stati osservati in ceppi di E. coli portatori del noto profago lambda: la ciprofloxacina, ma non l'ampicillina, induceva lisi mediata da profagi e riduceva i persister nelle cellule normali, mentre i mutanti lepA e i ceppi privi di profagi evitavano questa uccisione aggiuntiva.
Cosa significa questo per combattere infezioni ostinate
Il lavoro sostiene un'idea semplice ma potente: per i batteri che ospitano profagi dormienti, i ROS indotti dagli antibiotici possono spingere questi virus nascosti a entrare in azione, aggiungendo un'ulteriore ondata di uccisione che riduce il serbatoio di persister tolleranti al farmaco. In Salmonella priva di LepA, livelli di ROS più bassi significano una minore attivazione dei profagi e un maggior numero di cellule che sopravvivono silenziosamente alla ciprofloxacina. Ciò suggerisce che, in alcuni contesti, sfruttare con attenzione ROS e profagi potrebbe rendere più efficaci gli antibiotici esistenti — un concetto noto come sinergia fago‑antibiotico. Allo stesso tempo, aumentare i ROS comporta rischi, perché i profagi possono anche diffondere geni di virulenza e di resistenza ad altri batteri. Lo studio mette in luce come una singola proteina batterica, lo stato del metabolismo cellulare e la presenza di virus silenziosi determinino insieme se un ciclo di antibiotici elimina un'infezione o lascia sopravvissuti che possono causare problemi in seguito.
Citazione: Braetz, S., Karp, M., Nerlich, A. et al. Reduced ROS-associated prophage induction in a lepA mutant contributes to increased fluoroquinolone persistence in Salmonella Typhimurium. Sci Rep 16, 12721 (2026). https://doi.org/10.1038/s41598-026-47552-0
Parole chiave: persistenza agli antibiotici, specie reattive dell'ossigeno, profagi, Salmonella Typhimurium, ciprofloxacina