Clear Sky Science · pt
Redução da indução de profagos associada a ROS em um mutante lepA contribui para o aumento da persistência a fluoroquinolonas em Salmonella Typhimurium
Por que alguns micróbios sobrevivem mesmo aos nossos remédios mais potentes
Quando médicos usam antibióticos potentes para tratar infecções graves, a maioria das bactérias morre rapidamente. Ainda assim, uma minoria ínfima pode entrar em estado dormente, resistir ao ataque e, mais tarde, regenerar a infecção. Esses sobreviventes resistentes, chamados de células persister, não carregam genes clássicos de resistência, por isso são difíceis de prever e mais difíceis de eliminar. Este estudo investiga por que certas bactérias Salmonella têm maior probabilidade de formar persisters durante o tratamento com a fluoroquinolona amplamente usada ciprofloxacino, e como rajadas mínimas de oxigênio quimicamente reativo e vírus ocultos dentro das bactérias podem inclinar a balança entre morte e sobrevivência.
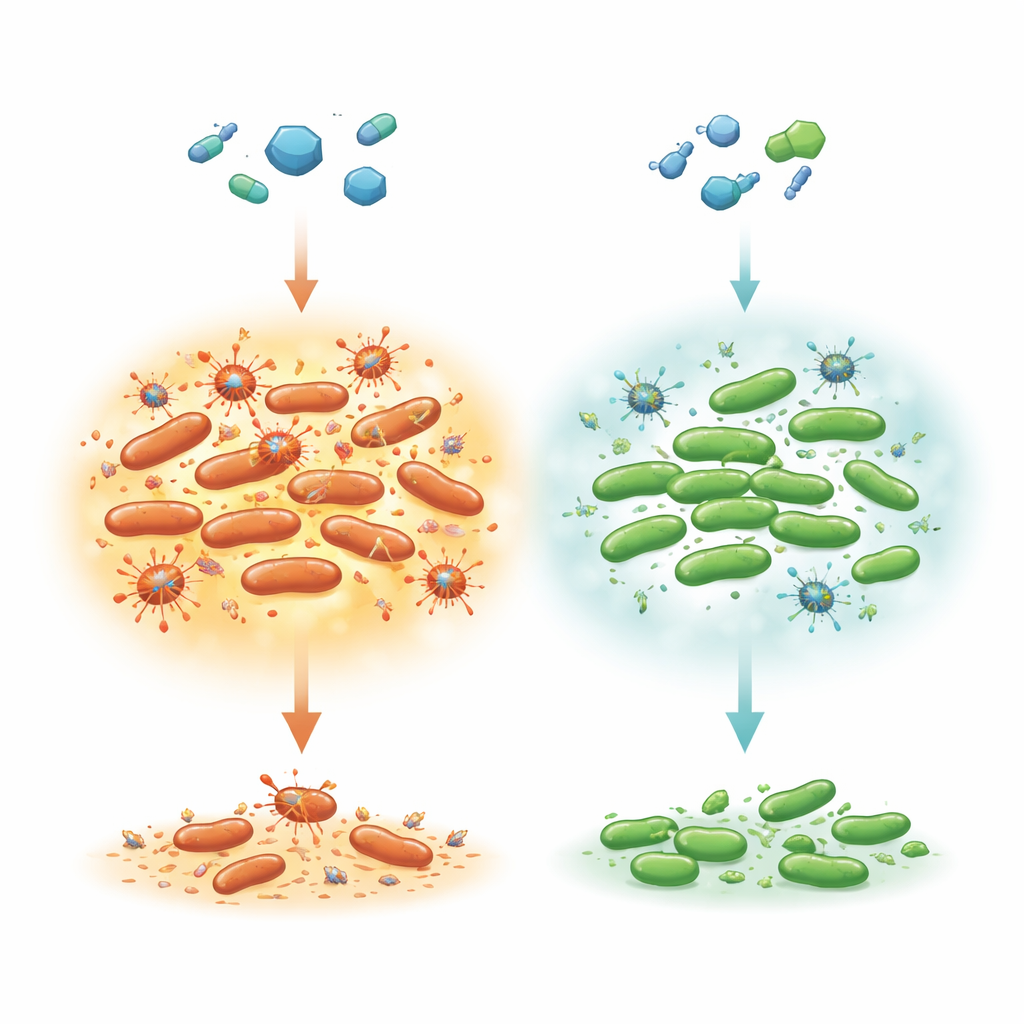
Sobreviventes ocultos durante um ataque com antibiótico
A maioria das bactérias de uma população é rapidamente eliminada por um antibiótico eficaz, mas uma subpopulação muito pequena morre muito mais lentamente. Esse padrão de morte em “dois estágios” é uma marca das células persister, que simplesmente se recolhem até o fim do fármaco e então retomam o crescimento normal. Os autores focaram em Salmonella Typhimurium, uma causa comum de doenças transmitidas por alimentos que pode exigir tratamento com ciprofloxacino em pacientes vulneráveis. Trabalhos anteriores em Escherichia coli sugeriram que remover um fator de tradução chamado LepA tornava as células incomumente tolerantes a vários antibióticos ao reduzir o acúmulo de espécies reativas de oxigênio (ROS) — subprodutos metabolicamente agressivos que podem danificar DNA e proteínas. Aqui, os pesquisadores perguntaram se LepA desempenha papel semelhante em Salmonella e como isso interage com vírus (profagos) que permanecem dormentes dentro do cromossomo bacteriano.
O que mudou em bactérias sem uma única proteína
A equipe comparou Salmonella normal com uma versão sem o gene lepA. Eles expuseram ambas a três classes principais de antibióticos bactericidas: ciprofloxacino (uma fluoroquinolona), ampicilina (uma beta-lactama) e kanamicina (uma aminoglicosídeo). Para ampicilina e kanamicina, ambas as linhagens se comportaram de forma semelhante, mostrando a queda rápida habitual da maioria das células e um platô de persisters raros. Em contraste, após o tratamento com ciprofloxacino, o mutante lepA deixou consistentemente para trás mais células persister do que a linhagem normal. Medições de ROS usando um corante fluorescente mostraram que ciprofloxacino desencadeou forte formação de ROS, especialmente radicais hidroxila, e que esses níveis eram menores no mutante lepA. Ensaios de consumo de oxigênio indicaram que as células mutantes aumentavam a respiração — e assim a produção de ROS — mais lentamente, sugerindo que defeitos sutis na maquinaria energética da célula mantêm o estresse oxidativo mais baixo e favorecem a sobrevivência sob pressão do medicamento.
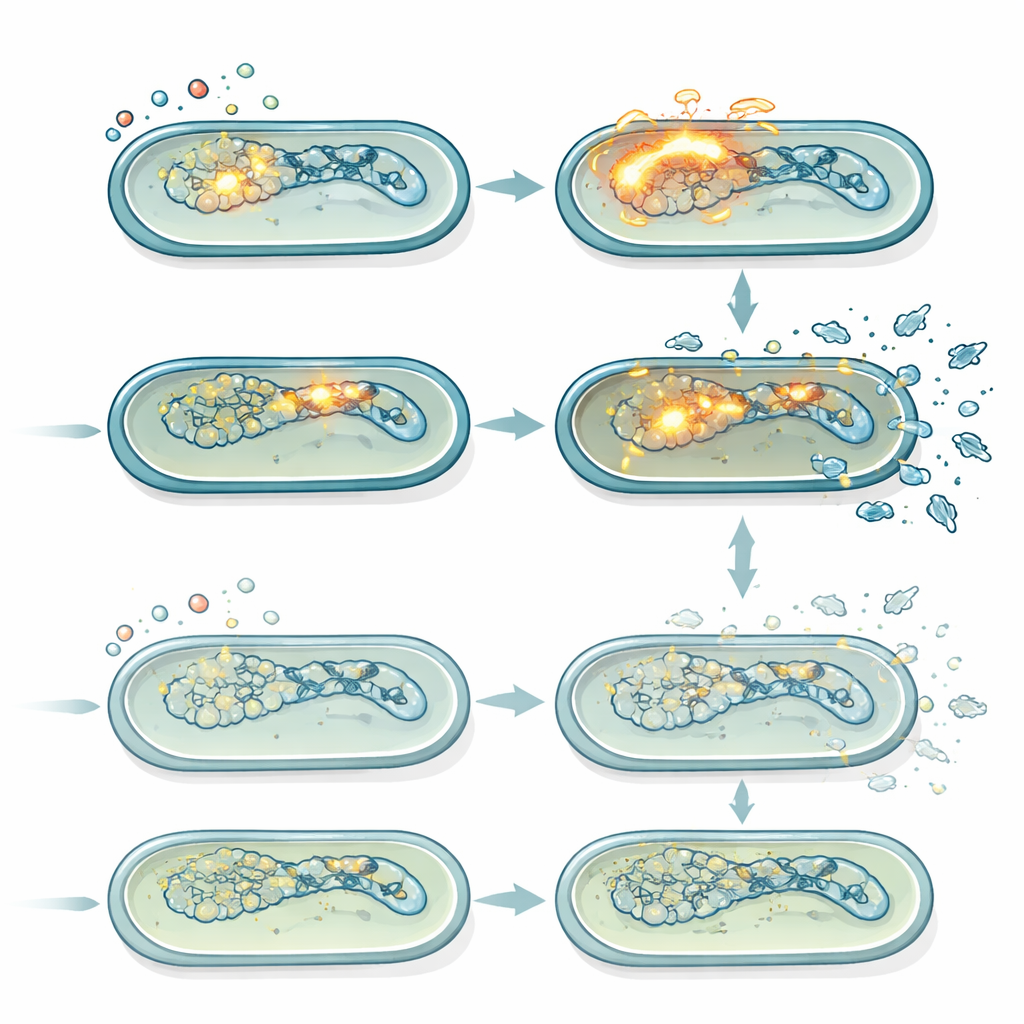
Vírus silenciosos que se tornam letais sob estresse
Salmonella Typhimurium carrega vários profagos, genomas virais dormentes que podem despertar quando o DNA bacteriano é danificado. Quando ativados, esses profagos mudam para um programa lítico, replicam-se e fazem a célula hospedeira romper. Usando medidas de expressão gênica e linhagens repórter fluorescentes, os autores mostraram que ciprofloxacino ativou fortemente a resposta SOS de dano ao DNA e, em células normais, desencadeou indução robusta de um profago em particular (Gifsy-1). Essa indução foi mais fraca no mutante lepA, em consonância com seus níveis mais baixos de ROS. Ensaios de placa que contam partículas fagais ativas confirmaram que, em doses moderadas de ciprofloxacino, a linhagem normal produzia continuamente mais fagos ao longo do tempo do que o mutante lepA. Quando todos os profagos foram removidos geneticamente, a vantagem de sobrevivência do mutante lepA em ciprofloxacino moderado desapareceu em grande parte, revelando que a diferença chave entre as linhagens era a intensidade com que a ativação de profagos impulsionada por ROS contribuía para a morte.
Reduzir o estresse oxidativo muda quem sobrevive
Os pesquisadores então usaram glutationa, um antioxidante natural, para amortecer as ROS durante o tratamento com ciprofloxacino. Em Salmonella normal que carregava profagos, a glutationa expandiu a subpopulação de células que não mostravam indução de profagos e aumentou a fração de persisters. Em um fundo sem profagos, o mesmo tratamento retardou a morte inicial, mas não aumentou mais os níveis de persisters, ressaltando que o benefício de sobrevivência estava ligado à supressão de profagos. Em doses muito altas de ciprofloxacino, os antioxidantes novamente aumentaram a sobrevivência muito mais em células com profagos do que naquelas sem profagos, indicando que a ativação de profagos desencadeada por ROS pode ser importante mesmo sob pressão intensa do fármaco. Padrões semelhantes foram observados em linhagens de E. coli que carregam o bem conhecido profago lambda: ciprofloxacino, mas não ampicilina, levou à lise mediada por profagos e reduziu persisters em células normais, enquanto mutantes lepA e linhagens livres de profagos evitaram essa morte adicional.
O que isso significa para combater infecções persistentes
O trabalho sustenta uma ideia simples, porém poderosa: para bactérias que abrigam profagos dormentes, ROS induzidas por antibióticos podem empurrar esses vírus ocultos à ação, adicionando uma onda extra de morte que reduz o reservatório de persisters tolerantes ao fármaco. Em Salmonella sem LepA, ROS mais baixas significam indução de profagos mais fraca e mais células que silenciosamente sobrevivem ao ciprofloxacino. Isso sugere que, em alguns contextos, aproveitar cuidadosamente ROS e profagos poderia tornar antibióticos existentes mais eficazes — um conceito conhecido como sinergia fago–antibiótico. Ao mesmo tempo, aumentar ROS carrega riscos, porque profagos também podem disseminar genes de virulência e resistência para outras bactérias. O estudo destaca como uma única proteína bacteriana, o estado do metabolismo celular e a presença de vírus silenciosos determinam conjuntamente se um curso de antibiótico elimina uma infecção ou deixa sobreviventes que podem causar problemas depois.
Citação: Braetz, S., Karp, M., Nerlich, A. et al. Reduced ROS-associated prophage induction in a lepA mutant contributes to increased fluoroquinolone persistence in Salmonella Typhimurium. Sci Rep 16, 12721 (2026). https://doi.org/10.1038/s41598-026-47552-0
Palavras-chave: persistência a antibióticos, espécies reativas de oxigênio, profagos, Salmonella Typhimurium, ciprofloxacino