Clear Sky Science · fr
Une induction réduite des prophages associée au ROS chez un mutant lepA contribue à une persistance accrue aux fluoroquinolones chez Salmonella Typhimurium
Pourquoi certains germes survivent même à nos médicaments les plus puissants
Lorsque les médecins utilisent des antibiotiques puissants pour traiter des infections graves, la plupart des bactéries meurent rapidement. Pourtant, une infime minorité peut entrer dans un état dormant, survivre à l'attaque et regarnir l'infection par la suite. Ces survivants résistants, appelés cellules persister, ne portent pas les gènes de résistance classiques, ce qui les rend difficiles à prévoir et encore plus difficiles à éliminer. Cette étude explore pourquoi certaines bactéries Salmonella sont plus susceptibles de former des persisters lors d'un traitement par la fluoroquinolone largement utilisée ciprofloxacine, et comment de petites poussées d'oxygène chimiquement réactif et des virus cachés à l'intérieur des bactéries peuvent faire basculer l'équilibre entre la mort et la survie.
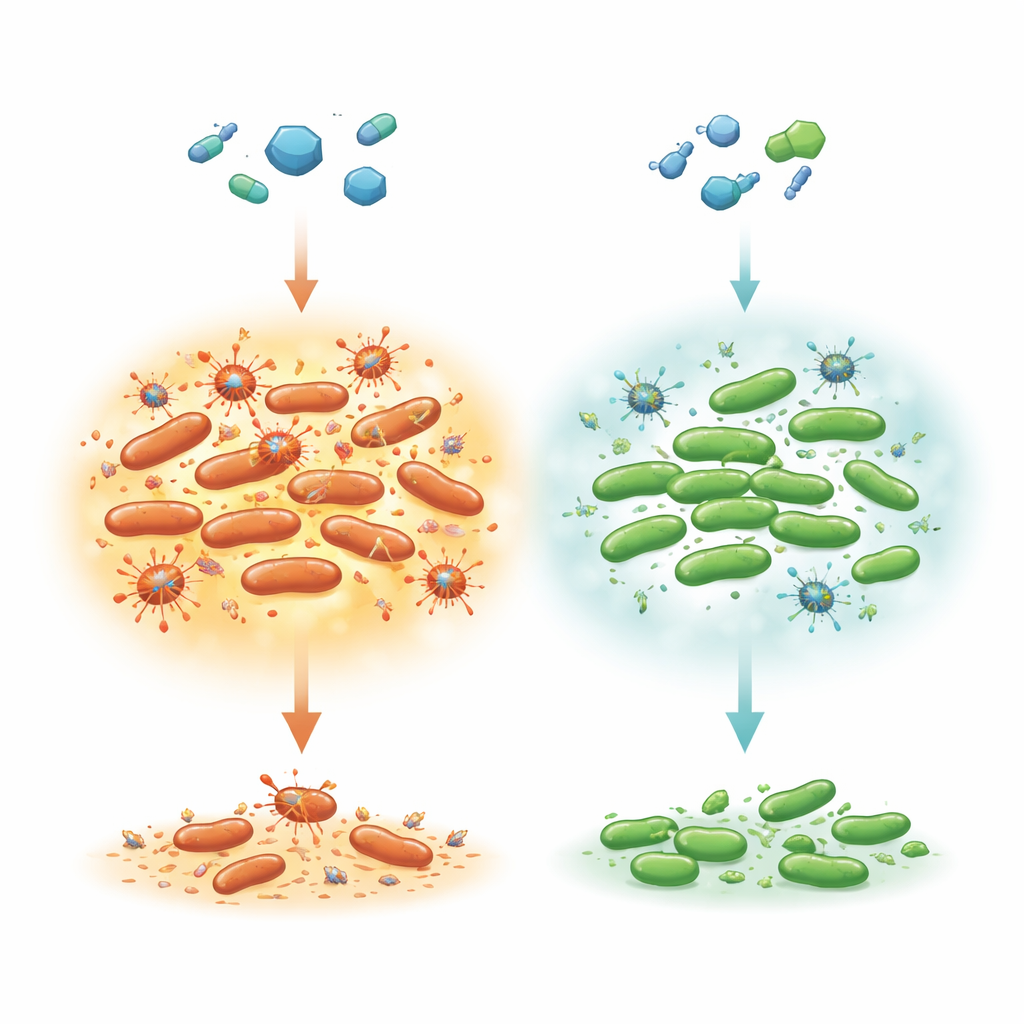
Des survivants cachés au cœur d'une attaque antibiotique
La plupart des bactéries d'une population sont rapidement tuées par un antibiotique efficace, mais une très petite sous-population meurt beaucoup plus lentement. Ce schéma de tuerie en « deux temps » est la marque des cellules persister, qui se refugiént jusqu'à la disparition du médicament, puis reprennent leur croissance normale. Les auteurs se sont concentrés sur Salmonella Typhimurium, une cause fréquente d'intoxication alimentaire qui peut nécessiter un traitement à la ciprofloxacine chez les patients vulnérables. Des travaux antérieurs sur Escherichia coli ont suggéré que la suppression d'un facteur de traduction appelé LepA rendait les cellules anormalement tolérantes à plusieurs antibiotiques en réduisant l'accumulation d'espèces réactives de l'oxygène (ROS) — des sous-produits métaboliques chimiquement agressifs pouvant endommager l'ADN et les protéines. Ici, les chercheurs ont interrogé si LepA joue un rôle similaire chez Salmonella et comment cela interagit avec des virus (prophages) qui restent dormants dans le chromosome bactérien.
Ce qui change chez des bactéries privées d'une seule protéine
L'équipe a comparé Salmonella normale à une version dépourvue du gène lepA. Ils ont exposé les deux souches à trois grandes classes d'antibiotiques bactéricides : la ciprofloxacine (une fluoroquinolone), l'ampicilline (un bêta-lactame) et la kanamycine (un aminoglycoside). Pour l'ampicilline et la kanamycine, les deux souches se comportaient de manière similaire, montrant la décroissance rapide habituelle de la plupart des cellules et un plateau de rares persisters. En revanche, après traitement à la ciprofloxacine, le mutant lepA laissait systématiquement plus de cellules persister que la souche normale. Des mesures des ROS à l'aide d'une sonde fluorescente ont montré que la ciprofloxacine déclenchait une forte formation de ROS, notamment des radicaux hydroxyles, et que ces niveaux étaient plus faibles dans le mutant lepA. Des essais de consommation d'oxygène ont indiqué que les cellules mutantes augmentaient leur respiration — et donc la production de ROS — plus lentement, ce qui suggère que des défauts subtils dans la machinerie énergétique de la cellule maintiennent le stress oxydatif plus bas et favorisent la survie sous pression médicamenteuse.
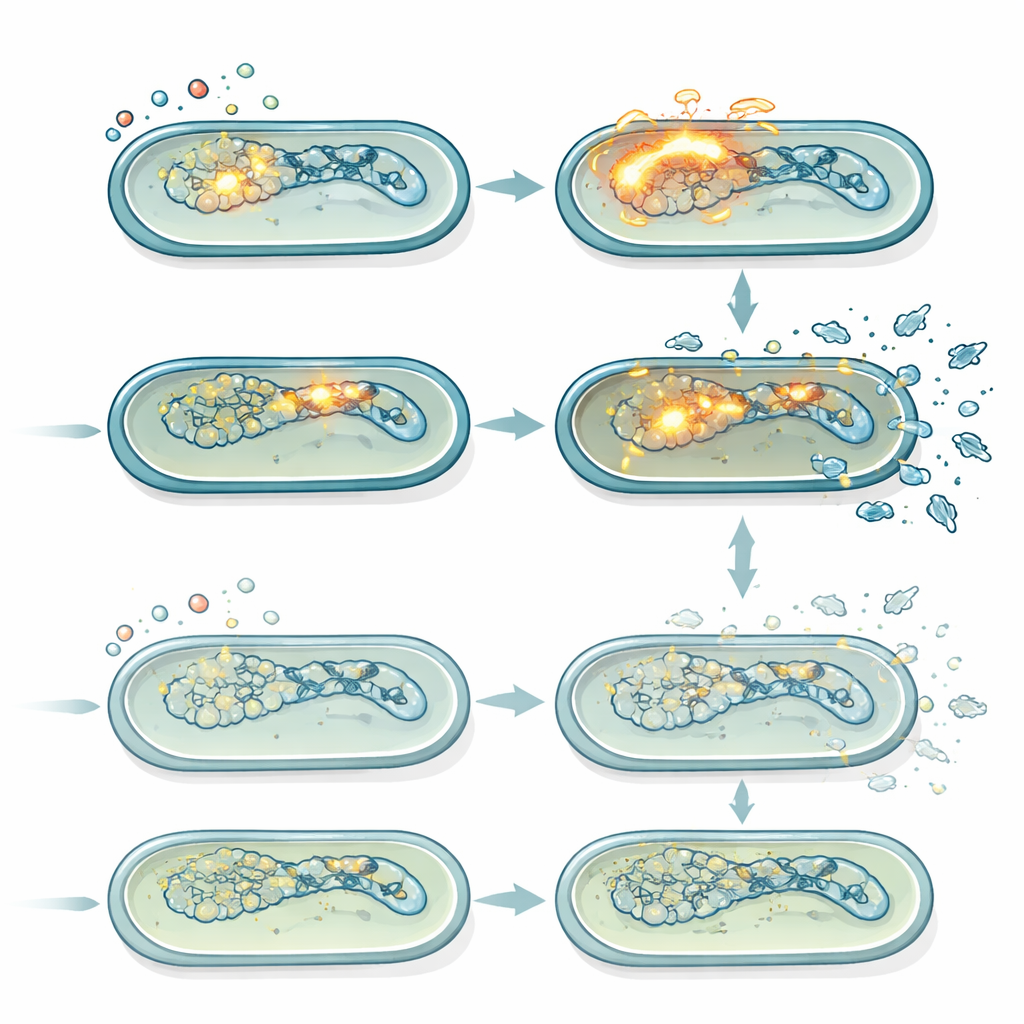
Des virus silencieux qui deviennent létaux sous stress
Salmonella Typhimurium porte plusieurs prophages, des génomes viraux dormants qui peuvent s'éveiller lorsque l'ADN bactérien est endommagé. Lorsqu'ils sont activés, ces prophages passent en programme lytique, se répliquent et provoquent la lyse de la cellule hôte. En utilisant des mesures d'expression génique et des souches rapportrices fluorescentes, les auteurs ont montré que la ciprofloxacine activait fortement la réponse SOS à l'endommagement de l'ADN et, dans les cellules normales, déclenchait une induction robuste d'un prophage en particulier (Gifsy-1). Cette induction était plus faible chez le mutant lepA, en accord avec ses niveaux de ROS réduits. Des tests de plaque comptant les particules phagiques actives ont confirmé qu'à des doses modérées de ciprofloxacine, la souche normale produisait continuellement plus de phages au fil du temps que le mutant lepA. Lorsque tous les prophages furent génétiquement supprimés, l'avantage de survie du mutant lepA à des doses modérées de ciprofloxacine disparut en grande partie, révélant que la différence clé entre les souches était l'intensité avec laquelle l'activation des prophages, entraînée par les ROS, contribuait à la mort cellulaire.
Réduire le stress oxydatif change qui survit
Les chercheurs ont ensuite utilisé la glutathion, un antioxydant naturel, pour atténuer les ROS pendant le traitement à la ciprofloxacine. Chez Salmonella normale portant des prophages, le glutathion a élargi la sous-population de cellules qui ne montraient pas d'induction prophagique et augmenté la fraction de persisters. Dans un arrière-plan sans prophages, le même traitement ralentit la tuerie initiale mais n'augmentait plus les niveaux de persisters, soulignant que l'avantage de survie était lié à la suppression des prophages. À des doses très élevées de ciprofloxacine, les antioxydants augmentèrent encore la survie beaucoup plus dans les cellules porteuses de prophages que dans les cellules sans prophages, indiquant que l'activation des prophages déclenchée par les ROS peut être importante même sous une forte pression médicamenteuse. Des schémas similaires furent observés chez des souches d'E. coli portant le prophage bien connu lambda : la ciprofloxacine, mais pas l'ampicilline, entraînait la lyse médiée par les prophages et réduisait le nombre de persisters dans les cellules normales, tandis que les mutants lepA et les souches sans prophages échappaient à cette tuerie supplémentaire.
Ce que cela signifie pour lutter contre les infections tenaces
Le travail soutient une idée simple mais puissante : pour les bactéries qui abritent des prophages dormants, les ROS induits par les antibiotiques peuvent pousser ces virus cachés à s'activer, ajoutant une vague supplémentaire de destruction qui réduit le réservoir de persisters tolérants aux médicaments. Chez Salmonella dépourvue de LepA, des niveaux de ROS plus faibles signifient une induction prophagique plus faible et davantage de cellules qui survivent silencieusement à la ciprofloxacine. Cela suggère que, dans certains contextes, exploiter avec soin les ROS et les prophages pourrait rendre les antibiotiques existants plus efficaces — un concept connu sous le nom de synergie phage–antibiotique. Dans le même temps, augmenter les ROS comporte des risques, car les prophages peuvent aussi propager des gènes de virulence et de résistance à d'autres bactéries. L'étude met en lumière comment une seule protéine bactérienne, l'état du métabolisme de la cellule et la présence de virus silencieux déterminent ensemble si un traitement antibiotique élimine une infection ou laisse des survivants qui pourraient poser problème plus tard.
Citation: Braetz, S., Karp, M., Nerlich, A. et al. Reduced ROS-associated prophage induction in a lepA mutant contributes to increased fluoroquinolone persistence in Salmonella Typhimurium. Sci Rep 16, 12721 (2026). https://doi.org/10.1038/s41598-026-47552-0
Mots-clés: persistance aux antibiotiques, espèces réactives de l'oxygène, prophages, Salmonella Typhimurium, ciprofloxacine