Clear Sky Science · pl
Zmniejszone wywoływanie profagów związane z ROS w mutancie lepA przyczynia się do zwiększonej persystencji na fluorochinolony w Salmonella Typhimurium
Dlaczego niektóre zarazki przetrwają nawet nasze najsilniejsze leki
Kiedy lekarze stosują silne antybiotyki w leczeniu poważnych zakażeń, większość bakterii ginie szybko. Jednak drobna mniejszość może wejść w stan utajenia, przeczekać atak i później odrodzić zakażenie. Ci wytrwali przetrwali, nazywani komórkami persisterowymi, nie posiadają klasycznych genów oporności, dlatego są trudni do przewidzenia i jeszcze trudniejsi do wyeliminowania. W tym badaniu analizowano, dlaczego niektóre bakterie Salmonella częściej tworzą persistery podczas leczenia powszechnie stosowaną fluorochinolonową ciprofloxaciną oraz jak krótkie wybuchy chemicznie reaktywnych form tlenu i ukryte wirusy wewnątrz bakterii mogą przesądzić o śmierci lub przetrwaniu.
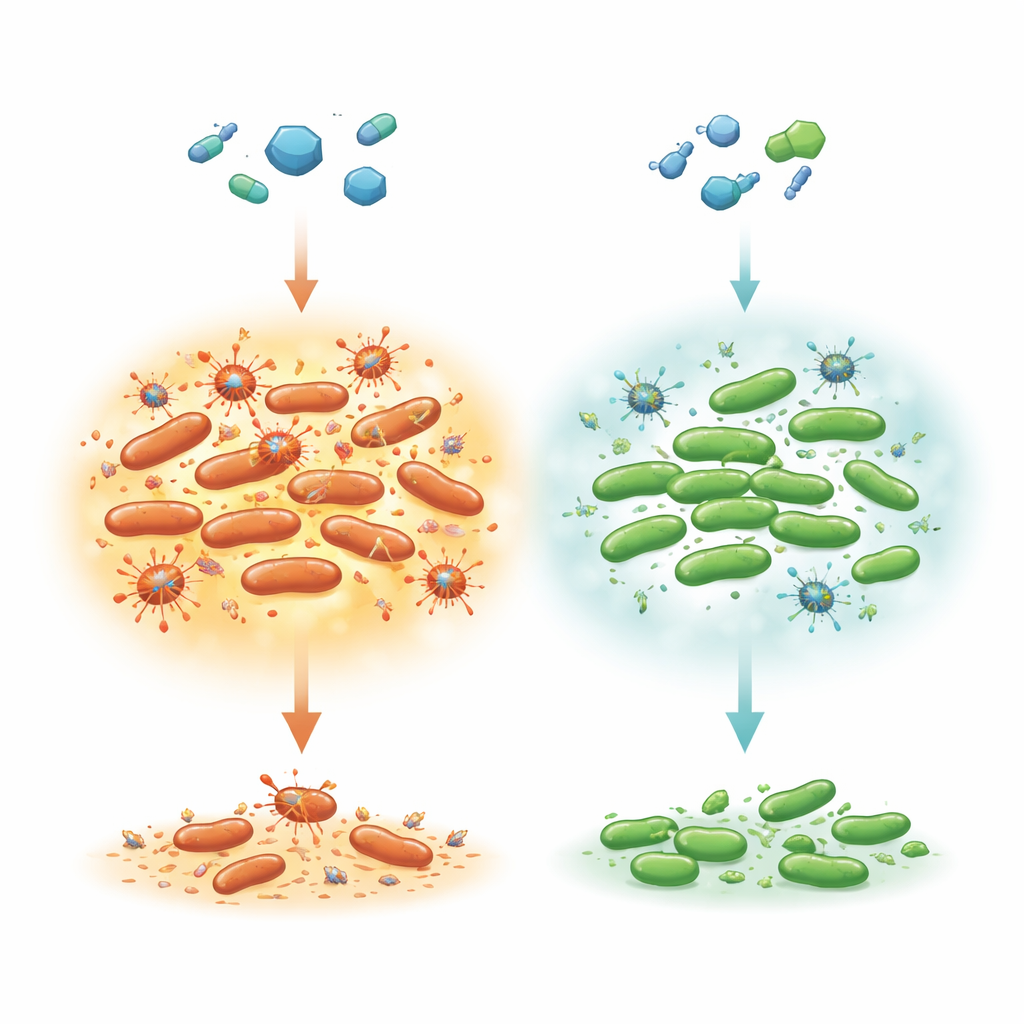
Ukryci ocaleni podczas ataku antybiotyku
Większość bakterii w populacji jest szybko zabijana przez skuteczny antybiotyk, ale bardzo mała podpopulacja ginie znacznie wolniej. Ten „dwustopniowy” wzorzec uśmiercania jest znamienny dla komórek persisterowych, które po prostu przechodzą w stan uśpienia, aż lek zniknie, a następnie wznawiają normalny wzrost. Autorzy skupili się na Salmonella Typhimurium, częstej przyczynie zatruć pokarmowych, która u pacjentów podatnych może wymagać leczenia ciprofloxaciną. Wcześniejsze prace na Escherichia coli sugerowały, że usunięcie czynnika translacyjnego LepA czyni komórki wyjątkowo tolerancyjnymi na kilka antybiotyków poprzez zmniejszenie gromadzenia się reaktywnych form tlenu (ROS) — chemicznie agresywnych produktów ubocznych metabolizmu, które mogą uszkadzać DNA i białka. W tym badaniu naukowcy sprawdzili, czy LepA pełni podobną rolę w Salmonella i jak to współgra z wirusami (profagami) drzemiącymi w chromosomie bakteryjnym.
Co się zmieniło w bakteriach pozbawionych pojedynczego białka
Zespół porównał normalne Salmonella z wersją pozbawioną genu lepA. Obie wystawiono na działanie trzech głównych klas antybiotyków bakteriobójczych: ciprofloxacyny (fluorochinolon), ampicyliny (beta-laktam) i kanamycyny (aminoglikozyd). Przy ampicylinie i kanamycynie oba szczepy zachowywały się podobnie, wykazując zwykłe szybkie wymieranie większości komórek i plateau rzadkich persisterów. W przeciwieństwie do tego po leczeniu ciprofloxaciną mutant lepA konsekwentnie pozostawiał więcej komórek persisterowych niż szczep dziki. Pomiar ROS przy użyciu barwnika fluorescencyjnego wykazał, że ciprofloxacyna silnie indukowała powstawanie ROS, zwłaszcza rodników hydroksylowych, a te poziomy były niższe w mutancie lepA. Testy zużycia tlenu wskazały, że komórki mutanta zwiększały oddychanie — a zatem produkcję ROS — wolniej, co sugeruje, że subtelne defekty w maszynerii energetycznej komórki utrzymują niższy stres oksydacyjny i sprzyjają przetrwaniu pod presją leku.
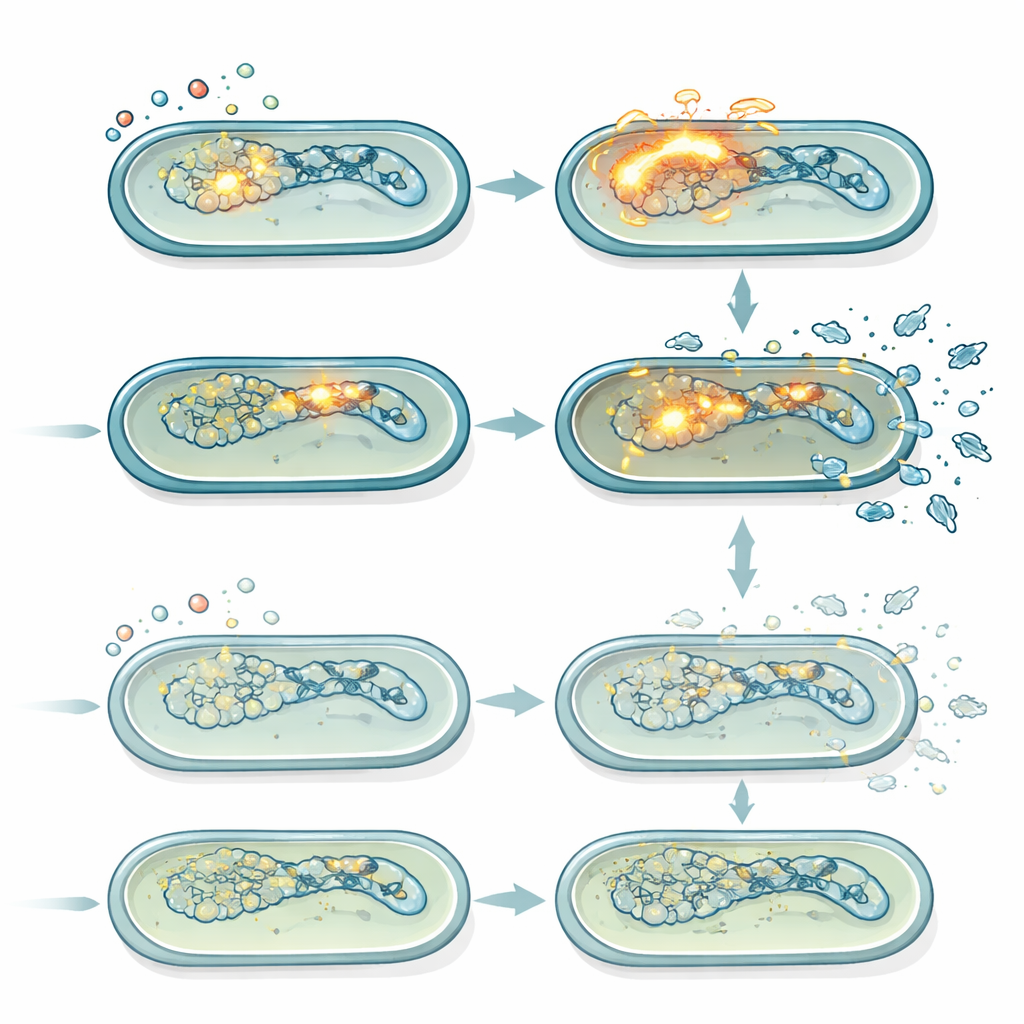
Ciche wirusy, które stają się zabójcze pod wpływem stresu
Salmonella Typhimurium nosi kilka profagów, utajonych genomów wirusowych, które mogą się obudzić, gdy DNA bakterii zostanie uszkodzone. Po aktywacji profagi przechodzą w program lityczny, replikują się i powodują pęknięcie komórki-gospodarza. Na podstawie pomiarów ekspresji genów i fluorescencyjnych szczepów reporterowych autorzy pokazali, że ciprofloxacyna silnie aktywowała odpowiedź SOS na uszkodzenie DNA i w komórkach dzikich powodowała silne indukowanie szczególnego profaga (Gifsy-1). Ta indukcja była słabsza w mutancie lepA, co korelowało z niższymi poziomami ROS. Testy plakowe liczące aktywne cząstki fagowe potwierdziły, że przy umiarkowanych dawkach ciprofloxacyny szczep dziki w czasie stale wytwarzał więcej fagów niż mutant lepA. Kiedy wszystkie profagi zostały genetycznie usunięte, przewaga przeżywalności mutanta lepA przy umiarkowanej ciprofloxacinie w dużej mierze zniknęła, ujawniając, że kluczową różnicą między szczepami było to, jak silnie aktywacja profagów napędzana przez ROS przyczyniała się do zabijania.
Zmniejszenie stresu tlenowego zmienia, kto przetrwa
Naukowcy następnie zastosowali glutation, naturalny antyoksydant, aby stłumić ROS podczas leczenia ciprofloxaciną. W normalnej Salmonella niosącej profagi glutation zwiększył podpopulację komórek, które nie wykazywały indukcji profagów, i powiększył odsetek persisterów. W tle pozbawionej profagów to samo leczenie spowolniło wczesne zabijanie, ale już nie zwiększyło poziomów persisterów, podkreślając, że korzyść z przetrwania wiązała się z tłumieniem profagów. Przy bardzo wysokich dawkach ciprofloxacyny antyoksydanty ponownie zwiększały przeżywalność znacznie bardziej w komórkach z profagami niż w komórkach bez nich, wskazując, że aktywacja profagów wywołana ROS może być ważna nawet pod silnym naciskiem leku. Podobne wzorce zaobserwowano w szczepach E. coli niosących dobrze znany profag lambda: ciprofloxacyna, ale nie ampicylina, powodowała lizy zależne od profagów i zmniejszała liczbę persisterów w komórkach dzikich, podczas gdy mutanci lepA i szczepy bez profagów unikały tego dodatkowego zabijania.
Co to znaczy dla walki z uporczywymi zakażeniami
Praca wspiera prostą, lecz silną ideę: dla bakterii posiadających utajone profagi antybiotykami indukowane ROS mogą pchnąć te ukryte wirusy do działania, dodając dodatkową falę zabijania, która zmniejsza pulę tolerancyjnych na leki persisterów. W Salmonella pozbawionej LepA niższe ROS oznaczają słabszą aktywację profagów i więcej komórek, które cicho przetrwają działanie ciprofloxacyny. To sugeruje, że w niektórych sytuacjach staranne wykorzystanie ROS i profagów mogłoby uczynić istniejące antybiotyki bardziej skutecznymi — koncepcja znana jako synergizm fag–antybiotyk. Równocześnie zwiększanie ROS niesie ryzyko, ponieważ profagi mogą także przenosić geny wirulencji i oporności na inne bakterie. Badanie podkreśla, jak pojedyncze białko bakteryjne, stan metabolizmu komórki i obecność ukrytych wirusów wspólnie decydują o tym, czy kuracja antybiotykowa wyczyści zakażenie, czy pozostawi ocalałych, którzy mogą później sprawić kłopoty.
Cytowanie: Braetz, S., Karp, M., Nerlich, A. et al. Reduced ROS-associated prophage induction in a lepA mutant contributes to increased fluoroquinolone persistence in Salmonella Typhimurium. Sci Rep 16, 12721 (2026). https://doi.org/10.1038/s41598-026-47552-0
Słowa kluczowe: utrzymanie antybiotykowe, reaktywne formy tlenu, profagi, Salmonella Typhimurium, ciprofloxacyna