Clear Sky Science · de
Verminderte ROS-assoziierte Prophageninduktion in einem lepA-Mutanten trägt zu erhöhter Fluorchinolon-Persistenz in Salmonella Typhimurium bei
Warum einige Keime selbst unsere stärksten Medikamente überleben
Wenn Ärzte starke Antibiotika zur Behandlung schwerer Infektionen einsetzen, sterben die meisten Bakterien schnell ab. Doch eine winzige Minderheit kann in einen ruhenden Zustand übergehen, die Angriffe aussitzen und später die Infektion wiederherstellen. Diese widerstandsfähigen Überlebenden, Persister-Zellen genannt, tragen keine klassischen Resistenzgene, sie sind daher schwer vorhersehbar und noch schwerer zu beseitigen. Diese Studie untersucht, warum bestimmte Salmonella-Bakterien während einer Behandlung mit dem weitverbreiteten Fluorchinolon-Antibiotikum Ciprofloxacin eher Persister bilden und wie kleine Ausbrüche chemisch reaktiver Sauerstoffspezies und verborgene Viren innerhalb der Bakterien das Gleichgewicht zwischen Tod und Überleben verschieben können.
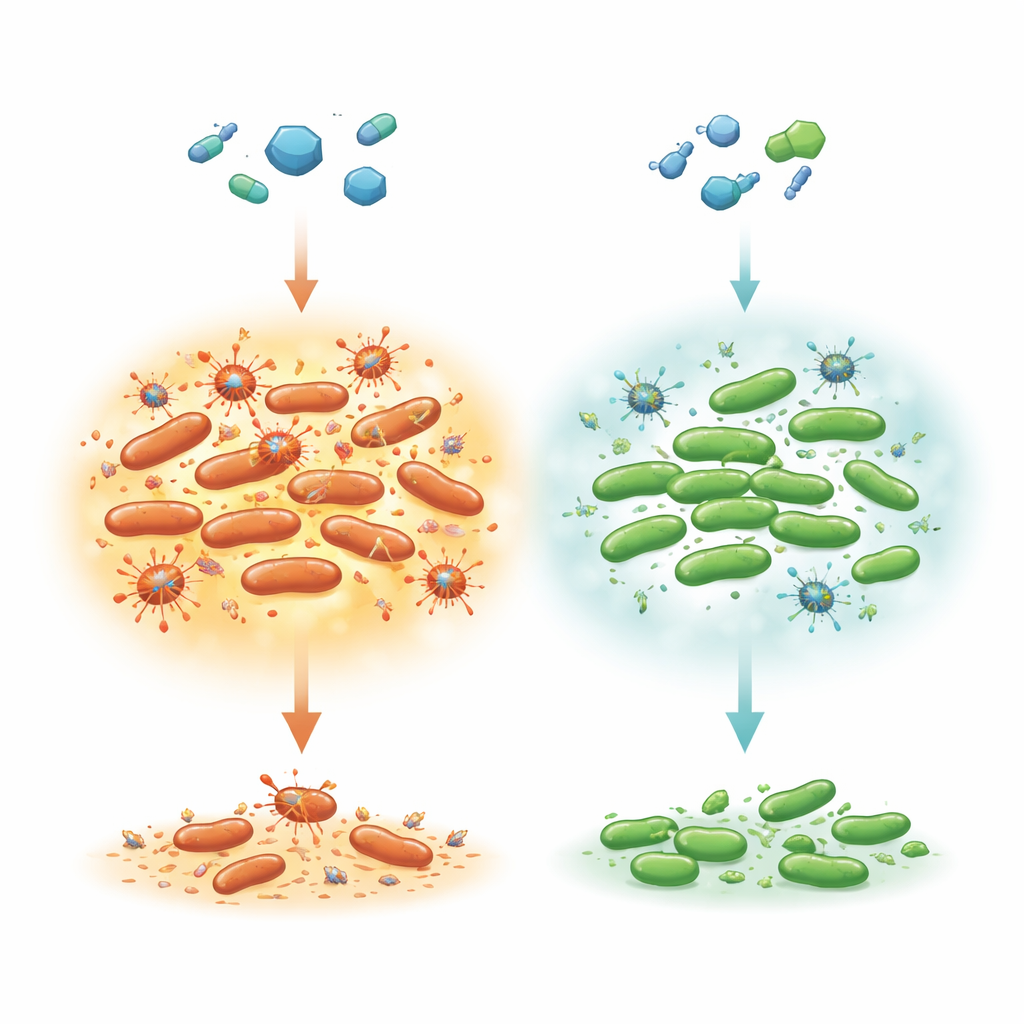
Verborgene Überlebende mitten in einem Antibiotikaangriff
Die meisten Bakterien in einer Population werden von einem wirksamen Antibiotikum rasch getötet, aber eine sehr kleine Subpopulation stirbt deutlich langsamer. Dieses „Zwei-Phasen“-Abtötungsmuster ist ein Kennzeichen von Persister-Zellen, die sich einfach einigeln, bis das Medikament weg ist, und dann wieder normal wachsen. Die Autoren konzentrierten sich auf Salmonella Typhimurium, eine häufige Ursache für lebensmittelbedingte Erkrankungen, die bei gefährdeten Patientinnen und Patienten eine Behandlung mit Ciprofloxacin erfordern kann. Frühere Arbeiten an Escherichia coli deuteten darauf hin, dass das Entfernen eines Translationsfaktors namens LepA Zellen ungewöhnlich tolerant gegenüber mehreren Antibiotika machte, indem die Anreicherung reaktiver Sauerstoffspezies (ROS) reduziert wurde — chemisch aggressive Stoffwechselnebenprodukte, die DNA und Proteine schädigen können. Hier fragten die Forschenden, ob LepA eine ähnliche Rolle in Salmonella spielt und wie dies mit Viren (Prophagen) zusammenhängt, die im bakteriellen Chromosom ruhen.
Was sich bei Bakterien ohne ein einzelnes Protein änderte
Das Team verglich normales Salmonella mit einer Variante, bei der das lepA-Gen fehlte. Beide wurden drei wichtigen Klassen bakterizider Antibiotika ausgesetzt: Ciprofloxacin (ein Fluorchinolon), Ampicillin (ein Beta-Lactam) und Kanamycin (ein Aminoglycosid). Bei Ampicillin und Kanamycin verhielten sich beide Stämme ähnlich und zeigten das übliche schnelle Absterben der meisten Zellen und ein Plateau seltener Persister. Im Gegensatz dazu hinterließ der lepA-Mutant nach Ciprofloxacin-Behandlung konstant mehr Persister-Zellen als der normale Stamm. Messungen der ROS mit einem fluoreszenten Farbstoff zeigten, dass Ciprofloxacin eine starke ROS-Bildung, insbesondere Hydroxylradikale, auslöste und dass diese Werte im lepA-Mutanten niedriger waren. Messungen des Sauerstoffverbrauchs deuteten darauf hin, dass die Mutantenzellen die Atmung — und damit die ROS-Produktion — langsamer hochfuhren, was darauf hindeutet, dass subtile Defekte in der Energiegewinnung der Zelle den oxidativen Stress geringer halten und unter Arzneidruck das Überleben begünstigen.
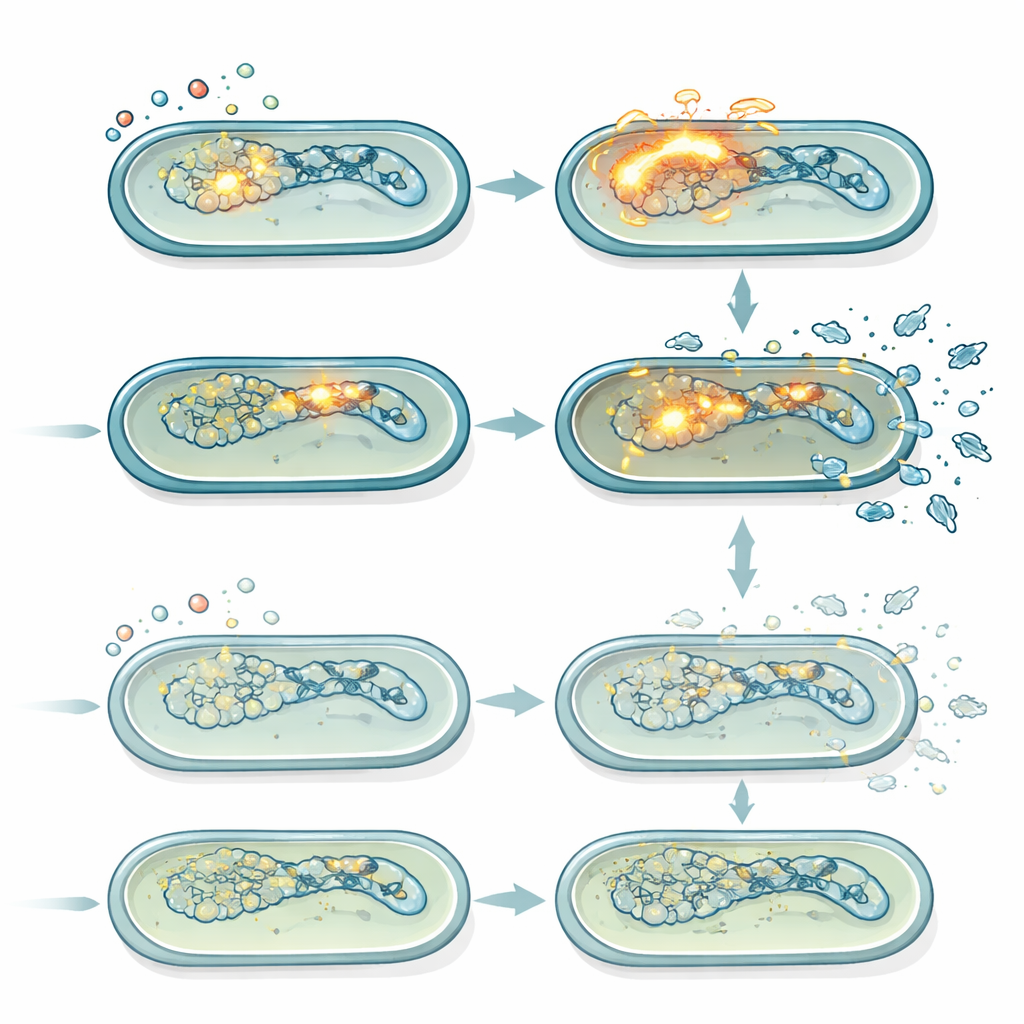
Stille Viren, die unter Stress tödlich werden
Salmonella Typhimurium trägt mehrere Prophagen, ruhende virale Genome, die erwachen können, wenn die bakterielle DNA beschädigt wird. Wenn sie aktiviert werden, schalten diese Prophagen auf ein lytisches Programm um, replizieren sich und bringen die Wirtszelle zum Platzen. Mit Genexpressionsmessungen und fluoreszenten Reporter-Stämmen zeigten die Autoren, dass Ciprofloxacin die bakterielle SOS-DNA-Schadensantwort stark aktivierte und in normalen Zellen besonders die Induktion eines Prophagen (Gifsy-1) auslöste. Diese Induktion war im lepA-Mutanten schwächer, was zu seinen niedrigeren ROS-Werten passte. Plaque-Assays, die aktive Phagenpartikel zählen, bestätigten, dass der normale Stamm bei moderaten Ciprofloxacin-Dosen über die Zeit kontinuierlich mehr Phagen produzierte als der lepA-Mutant. Wurden alle Prophagen genetisch entfernt, verschwand der Überlebensvorteil des lepA-Mutanten bei moderatem Ciprofloxacin größtenteils, was offenlegte, dass der Hauptunterschied zwischen den Stämmen darin lag, wie stark ROS-getriebene Prophagenaktivierung zum Abtöten beitrug.
Weniger Sauerstoffstress verändert, wer überlebt
Die Forschenden setzten dann Glutathion, ein natürliches Antioxidans, ein, um ROS während der Ciprofloxacin-Behandlung zu dämpfen. In normalem, Prophagen-tragendem Salmonella vergrößerte Glutathion die Subpopulation von Zellen, die keine Prophageninduktion zeigten, und erhöhte den Anteil der Persister. In einem prophagenfreien Hintergrund verlangsamte dieselbe Behandlung zwar das frühe Abtöten, steigerte aber nicht mehr die Persister-Zahlen, was unterstreicht, dass der Überlebensvorteil mit der Unterdrückung von Prophagen verknüpft war. Bei sehr hohen Ciprofloxacin-Dosen erhöhten Antioxidantien wiederum das Überleben deutlich stärker in Prophagen-positiven Zellen als in prophagenfreien, was anzeigt, dass ROS-getriggerte Prophagenaktivierung selbst unter intensivem Arzneidruck wichtig sein kann. Ähnliche Muster zeigten sich in E. coli-Stämmen mit dem bekannten Lambda-Prophagen: Ciprofloxacin, aber nicht Ampicillin, trieb prophagenvermittelte Lyse und reduzierte Persister in normalen Zellen, während lepA-Mutanten und prophagenfreie Stämme dieser zusätzlichen Tötung entgingen.
Was das für den Kampf gegen hartnäckige Infektionen bedeutet
Die Arbeit stützt eine einfache, aber potente Idee: Bei Bakterien, die ruhende Prophagen tragen, können antibiotikainduzierte ROS diese verborgenen Viren aktivieren und eine zusätzliche Abtötungswelle auslösen, die den Pool der medikamententoleranten Persister verkleinert. Bei Salmonella ohne LepA führt niedrigeres ROS zu schwächerer Prophagenaktivierung und mehr Zellen, die Ciprofloxacin still überleben. Das legt nahe, dass in manchen Situationen das gezielte Nutzen von ROS und Prophagen bestehende Antibiotika effektiver machen könnte — ein Konzept, das als Phagen–Antibiotika-Synergie bekannt ist. Gleichzeitig birgt das Verstärken von ROS Risiken, denn Prophagen können auch Virulenz- und Resistenzgene an andere Bakterien weitergeben. Die Studie zeigt, wie ein einzelnes bakterielles Protein, der Zustand des zellulären Stoffwechsels und das Vorhandensein stiller Viren zusammen bestimmen, ob eine Antibiotikatherapie eine Infektion auslöscht oder Überlebende zurücklässt, die später Probleme bereiten können.
Zitation: Braetz, S., Karp, M., Nerlich, A. et al. Reduced ROS-associated prophage induction in a lepA mutant contributes to increased fluoroquinolone persistence in Salmonella Typhimurium. Sci Rep 16, 12721 (2026). https://doi.org/10.1038/s41598-026-47552-0
Schlüsselwörter: Antibiotika-Persistenz, reaktive Sauerstoffspezies, Prophagen, Salmonella Typhimurium, Ciprofloxacin