Clear Sky Science · ja
lepA変異体で減少したROS関連のプロファージ誘導がSalmonella Typhimuriumにおけるフルオロキノロン持続性の増大に寄与する
なぜ最強の薬でも一部の細菌が生き残るのか
重症感染症の治療に強力な抗生物質を使うと、ほとんどの細菌は急速に死滅します。しかしごく一部は休眠状態に入り、攻撃をやり過ごして後に再び増殖します。これらの頑強な生存者はペルシスター(持続細胞)と呼ばれ、従来の耐性遺伝子を持たないため予測が難しく、除去も困難です。本研究は、広く使われるフルオロキノロン系抗生物質シプロフロキサシンの治療下で、なぜ特定のSalmonellaがペルシスターを形成しやすいのか、そして代謝由来の短時間の活性酸素(ROS)生成や細菌染色体に潜むウイルス(プロファージ)が死と生の境をどう左右するかを探ります。
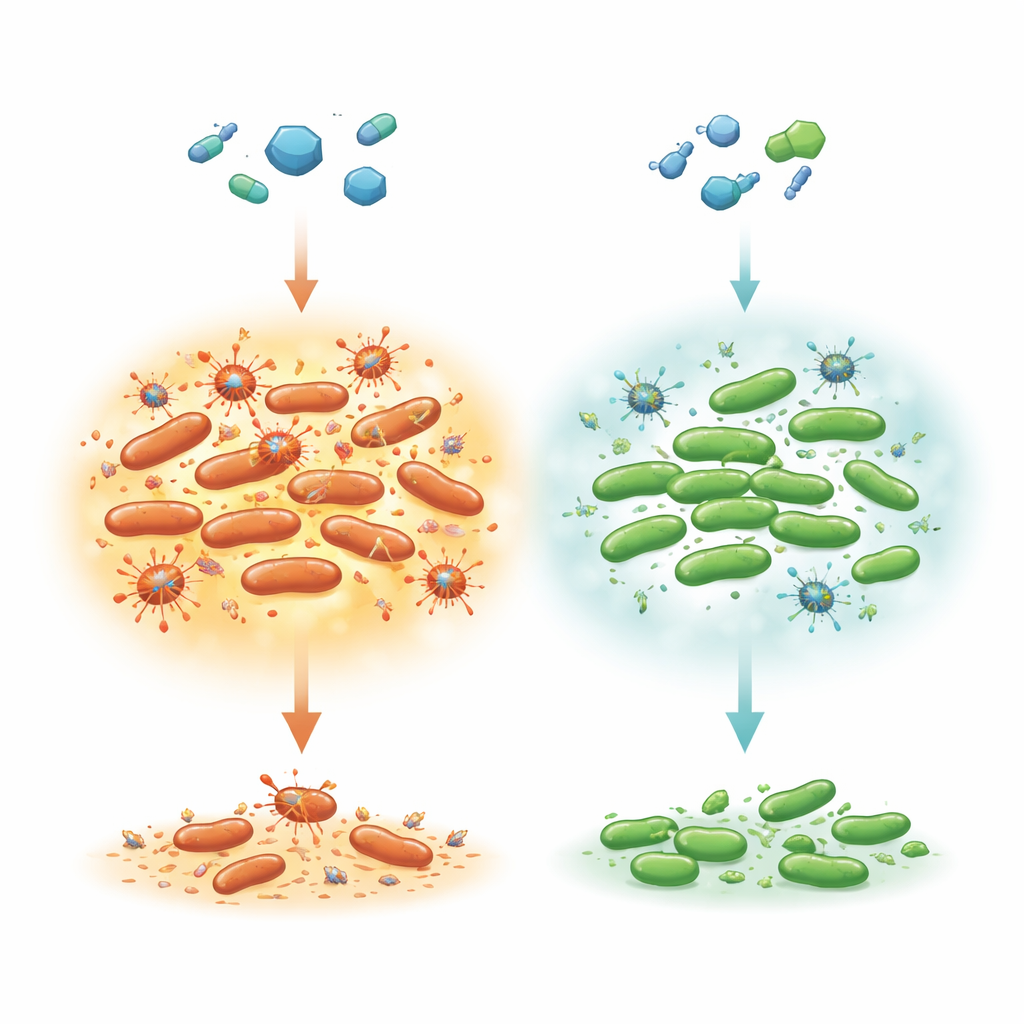
抗生物質攻撃下に潜む生存者たち
集団中の多くの細菌は有効な抗生物質で迅速に死にますが、ごく小さな亜集団ははるかに遅く死にます。この「二段階」の殺菌パターンは、薬がなくなるまでじっと耐えて成長を再開するペルシスターの特徴です。研究者らは食中毒の一般的原因で、脆弱な患者においてシプロフロキサシン治療を要することがあるSalmonella Typhimuriumに着目しました。大腸菌での先行研究は、翻訳因子タンパク質LepAを欠くと活性酸素種(ROS)の蓄積が抑えられ、複数の抗生物質に対して異常な耐性を示すことを示唆していました。ここでは、LepAがSalmonellaでも同様の役割を果たすか、そしてこれが細菌染色体に眠るプロファージとどのように相互作用するかを検証しました。
単一タンパク質欠失で細菌に何が起きたか
チームは野生型のSalmonellaとlepA遺伝子を欠く変異株を比較しました。両者をシプロフロキサシン(フルオロキノロン)、アンピシリン(ベータラクタム)、カナマイシン(アミノグリコシド)という三つの主要な殺菌性抗生物質に曝しました。アンピシリンとカナマイシンでは両株は同様の挙動を示し、大多数の細胞の急速な死滅と稀なペルシスターの定常状態という通常のパターンが見られました。対照的に、シプロフロキサシン処理後はlepA変異株が一貫して野生型より多くのペルシスターを残しました。蛍光色素を用いたROS測定では、シプロフロキサシンが特にヒドロキシルラジカルなどの強いROSを誘発し、これらのレベルはlepA変異株で低いことが示されました。酸素消費アッセイは、変異株が呼吸(したがってROS生成)をより遅く立ち上げることを示しており、細胞のエネルギー機構における微妙な欠陥が酸化ストレスを低く保ち、薬剤圧下での生存を有利にしていることを示唆します。
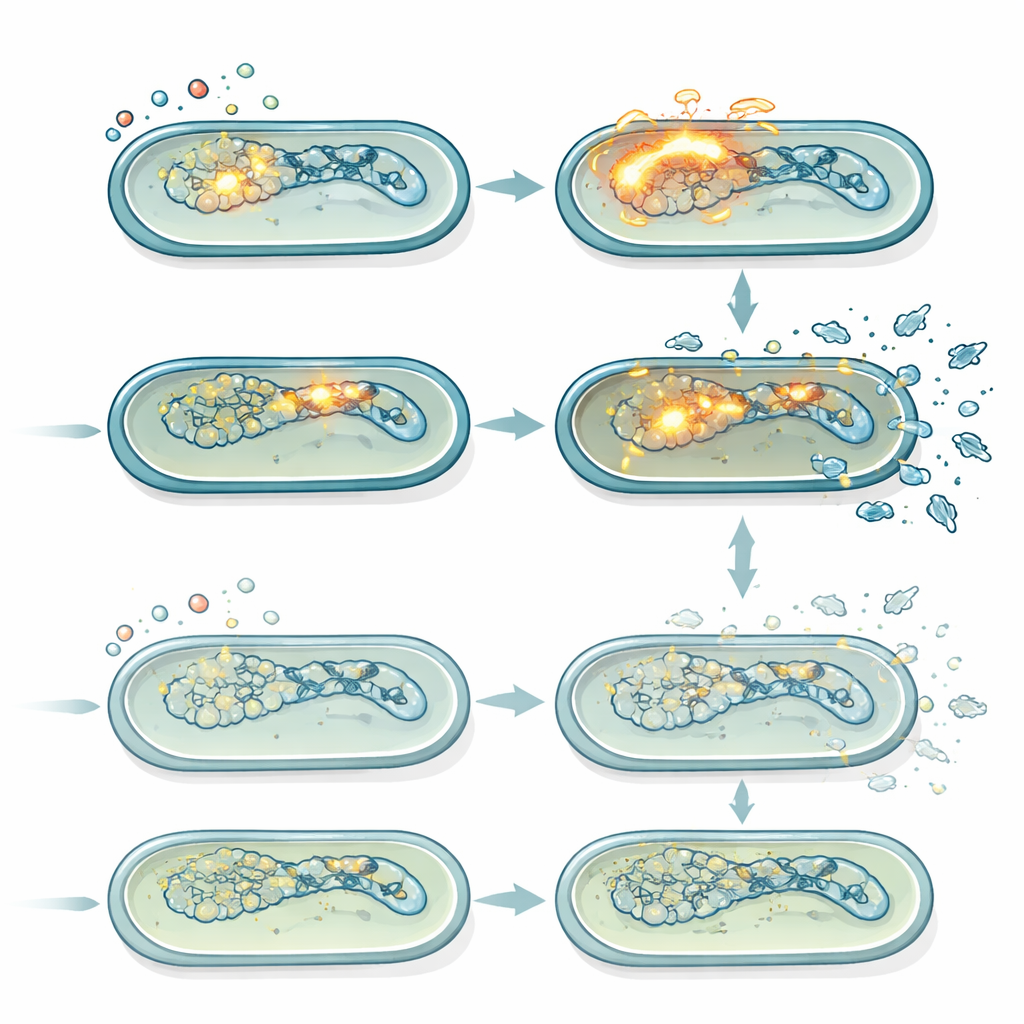
ストレス下で致死的になる沈黙のウイルス
Salmonella Typhimuriumは複数のプロファージを保有しており、細菌のDNAが損傷するとこれらの休眠するウイルスゲノムが目覚めることがあります。活性化されるとプロファージは溶菌性プログラムに入り複製して宿主細胞を破裂させます。遺伝子発現測定と蛍光レポーター株を用いて、著者らはシプロフロキサシンが強くSOS DNA損傷応答を活性化し、野生型では特に一つのプロファージ(Gifsy-1)が顕著に誘導されることを示しました。この誘導はlepA変異株では弱く、低いROSレベルと一致しました。プラークアッセイによる活性ファージ粒子の計数は、中程度のシプロフロキサシン量で野生型が時間とともにlepA変異株よりも多くのファージを生産し続けることを確認しました。全てのプロファージを遺伝学的に除去すると、中程度のシプロフロキサシンにおけるlepA変異株の生存優位はほぼ消失し、株間の主な違いがROS駆動のプロファージ活性化が致死に寄与する度合いであることを明らかにしました。
酸素ストレスを下げると生き残りが変わる
研究者らは次に天然の抗酸化物質であるグルタチオンを用いてシプロフロキサシン処理中のROSを抑えました。野生のプロファージ保持Salmonellaでは、グルタチオンはプロファージ誘導を示さない細胞の亜集団を拡大し、ペルシスターの割合を増加させました。プロファージを欠く背景では、同じ処置は初期の殺菌を遅らせたもののペルシスター数を増やさず、生存の利点がプロファージ抑制に結びついていることを強調しました。非常に高用量のシプロフロキサシンでは、抗酸化剤は再びプロファージ陽性細胞での生存をプロファージ陰性より大きく増やし、ROSによるプロファージ活性化が強い薬圧下でも重要になりうることを示しました。同様のパターンは、よく知られたラムダプロファージを持つ大腸菌株でも観察され、シプロフロキサシン(アンピシリンではなく)がプロファージ媒介の溶菌を誘導して通常株のペルシスターを減少させる一方、lepA変異株とプロファージ除去株はこの追加の殺菌を回避しました。
しつこい感染症と闘うための示唆
この研究は単純だが強力な考えを支持します。休眠するプロファージを宿す細菌では、抗生物質によるROS誘導がこれらの隠れたウイルスを活性化し、追加の殺菌波を生み出して薬剤耐性のあるペルシスターのプールを縮小する可能性があるということです。LepAを欠くSalmonellaではROSが低く、プロファージ活性化が弱いため多くの細胞がシプロフロキサシンから静かに生き残ります。これは、ある状況ではROSとプロファージを慎重に利用することで既存の抗生物質の効果を高められるかもしれないという、ファージ—抗生物質相乗効果の概念を示唆します。一方でROSを増強することはリスクも伴い、プロファージは病原因性や耐性遺伝子を他の細菌に広める可能性があります。本研究は、単一の細菌タンパク質、細胞代謝の状態、そして沈黙するウイルスの存在が、抗生物質投与が感染を一掃するか後に問題を残すかを共に決定することを浮き彫りにしています。
引用: Braetz, S., Karp, M., Nerlich, A. et al. Reduced ROS-associated prophage induction in a lepA mutant contributes to increased fluoroquinolone persistence in Salmonella Typhimurium. Sci Rep 16, 12721 (2026). https://doi.org/10.1038/s41598-026-47552-0
キーワード: 抗生物質持続性, 活性酸素種, プロファージ, Salmonella Typhimurium, シプロフロキサシン