Clear Sky Science · es
La reducción de la inducción de profagos asociada a ROS en un mutante de lepA contribuye al aumento de la persistencia frente a fluoroquinolonas en Salmonella Typhimurium
Por qué algunos gérmenes sobreviven incluso a nuestros fármacos más potentes
Cuando los médicos usan antibióticos potentes para tratar infecciones graves, la mayoría de las bacterias muere rápidamente. Sin embargo, una pequeña minoría puede entrar en un estado de latencia, resistir el ataque y posteriormente regenerar la infección. Estos supervivientes resistentes, denominados células persister, no portan los genes de resistencia clásicos, por lo que son difíciles de prever y aun más difíciles de eliminar. Este estudio explora por qué ciertas bacterias Salmonella tienen más probabilidades de formar persisters durante el tratamiento con la fluoroquinolona ampliamente usada ciprofloxacino, y cómo pequeñas ráfagas de oxígeno químicamente reactivo y virus ocultos dentro de las bacterias pueden inclinar la balanza entre la muerte y la supervivencia.
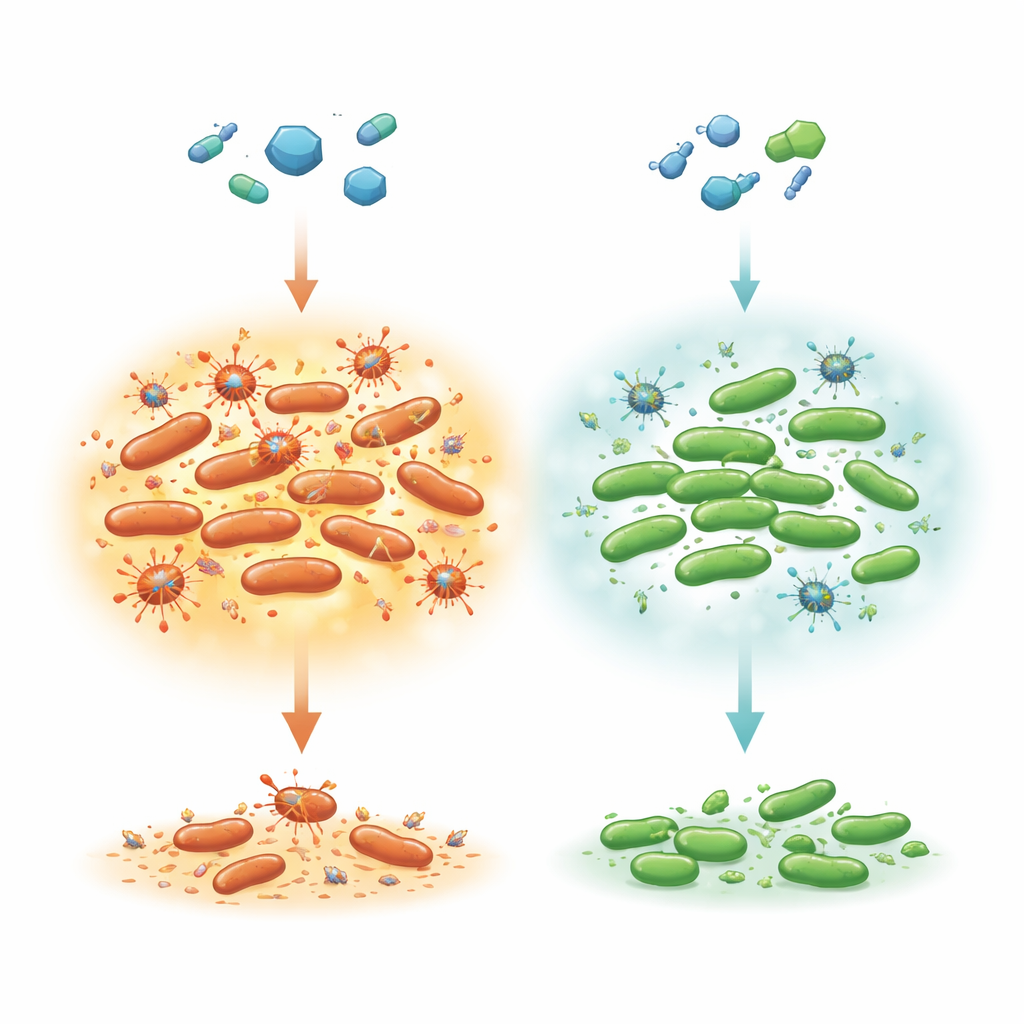
Supervivientes ocultos dentro de un ataque antibiótico
La mayoría de las bacterias de una población son eliminadas rápidamente por un antibiótico eficaz, pero una subpoblación muy pequeña muere mucho más lentamente. Este patrón de eliminación en "dos fases" es una característica de las células persister, que simplemente se acallan hasta que el fármaco desaparece y luego reanudan el crecimiento normal. Los autores se centraron en Salmonella Typhimurium, una causa común de intoxicación alimentaria que puede requerir tratamiento con ciprofloxacino en pacientes vulnerables. Trabajos previos en Escherichia coli sugirieron que eliminar un factor de traducción llamado LepA hacía que las células fueran inusualmente tolerantes a varios antibióticos al reducir la acumulación de especies reactivas de oxígeno (ROS): subproductos metabólicos químicamente agresivos que pueden dañar el ADN y las proteínas. Aquí, los investigadores preguntaron si LepA desempeña un papel similar en Salmonella y cómo esto interactúa con virus (profagos) que yacen latentes dentro del cromosoma bacteriano.
Qué cambió en bacterias a las que les falta una sola proteína
El equipo comparó Salmonella normal con una versión carente del gen lepA. Exponieron ambas a tres clases principales de antibióticos letales para células: ciprofloxacino (una fluoroquinolona), ampicilina (una beta-lactama) y kanamicina (una aminoglucósido). Para ampicilina y kanamicina, ambas cepas se comportaron de forma similar, mostrando la habitual muerte rápida de la mayoría de las células y una meseta de persisters raros. En contraste, tras el tratamiento con ciprofloxacino, el mutante lepA dejó sistemáticamente más células persister que la cepa normal. Medidas de ROS usando un tinte fluorescente mostraron que el ciprofloxacino provocó una fuerte formación de ROS, especialmente radicales hidroxilo, y que estos niveles eran más bajos en el mutante lepA. Ensayos de consumo de oxígeno indicaron que las células mutantes aumentaban la respiración —y por tanto la producción de ROS— más lentamente, lo que sugiere que defectos sutiles en la maquinaria energética de la célula mantienen el estrés oxidativo a niveles más bajos y favorecen la supervivencia bajo presión del fármaco.
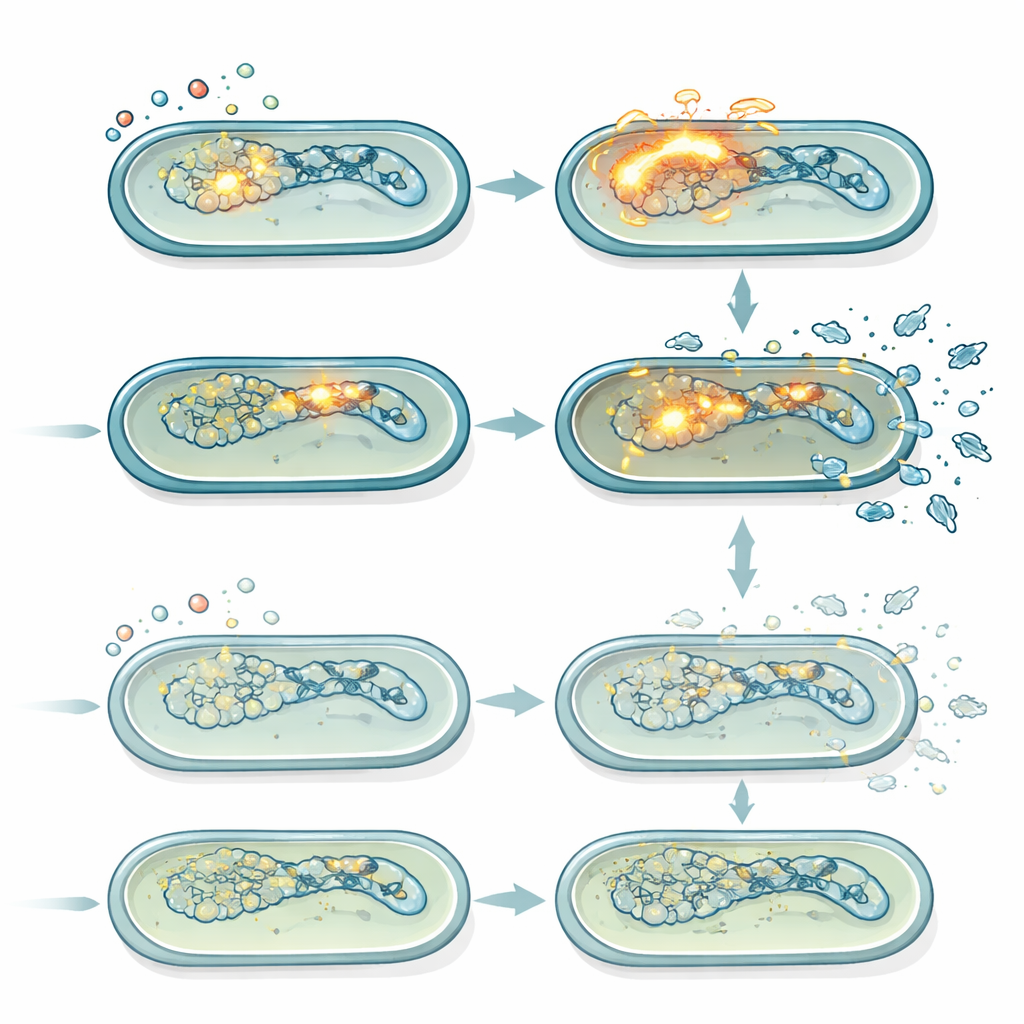
Virus silenciosos que se vuelven letales bajo estrés
Salmonella Typhimurium porta varios profagos, genomas virales latentes que pueden despertarse cuando el ADN bacteriano está dañado. Cuando se activan, estos profagos cambian a un programa lítico, se replican y causan la lisis de la célula hospedadora. Mediante mediciones de expresión génica y cepas reporteras fluorescentes, los autores mostraron que el ciprofloxacino activó fuertemente la respuesta SOS al daño del ADN y, en las células normales, disparó la inducción robusta de un profago en particular (Gifsy-1). Esta inducción fue más débil en el mutante lepA, en consonancia con sus niveles más bajos de ROS. Ensayos de placas que cuentan partículas fagicas activas confirmaron que, con dosis moderadas de ciprofloxacino, la cepa normal producía continuamente más fagos a lo largo del tiempo que el mutante lepA. Cuando se eliminaron genéticamente todos los profagos, la ventaja de supervivencia del mutante lepA frente a dosis moderadas de ciprofloxacino desapareció en gran medida, revelando que la diferencia clave entre las cepas era cuánto contribuía la activación de profagos impulsada por ROS a la muerte celular.
Reducir el estrés oxidativo cambia quién sobrevive
Los investigadores usaron entonces glutatión, un antioxidante natural, para atenuar las ROS durante el tratamiento con ciprofloxacino. En Salmonella portadora de profagos normal, el glutatión amplió la subpoblación de células que no mostraban inducción de profagos e incrementó la fracción de persisters. En un contexto libre de profagos, el mismo tratamiento ralentizó la muerte temprana pero ya no aumentó los niveles de persisters, subrayando que el beneficio de supervivencia estaba ligado a la supresión de profagos. A dosis muy altas de ciprofloxacino, los antioxidantes aumentaron nuevamente la supervivencia con mayor magnitud en células positivas para profagos que en las libres de profagos, lo que indica que la activación de profagos desencadenada por ROS puede ser importante incluso bajo una fuerte presión del fármaco. Patrones similares se observaron en cepas de E. coli que portan el conocido profago lambda: ciprofloxacino, pero no ampicilina, impulsó la lisis mediada por profagos y redujo los persisters en células normales, mientras que los mutantes lepA y las cepas sin profagos evitaron esta muerte adicional.
Qué significa esto para combatir infecciones persistentes
El trabajo respalda una idea sencilla pero poderosa: para las bacterias que albergan profagos latentes, las ROS inducidas por antibióticos pueden empujar a estos virus ocultos a la acción, añadiendo una ola adicional de muerte que reduce la reserva de persisters tolerantes al fármaco. En Salmonella sin LepA, niveles más bajos de ROS implican una activación de profagos más débil y más células que silenciosamente sobreviven al ciprofloxacino. Esto sugiere que, en ciertos contextos, aprovechar con cuidado las ROS y los profagos podría hacer que los antibióticos existentes sean más eficaces —un concepto conocido como sinergia fago–antibiótico. Al mismo tiempo, aumentar las ROS conlleva riesgos, porque los profagos también pueden dispersar genes de virulencia y resistencia a otras bacterias. El estudio destaca cómo una sola proteína bacteriana, el estado del metabolismo celular y la presencia de virus silenciosos determinan conjuntamente si un curso de antibiótico elimina una infección o deja supervivientes que pueden causar problemas más adelante.
Cita: Braetz, S., Karp, M., Nerlich, A. et al. Reduced ROS-associated prophage induction in a lepA mutant contributes to increased fluoroquinolone persistence in Salmonella Typhimurium. Sci Rep 16, 12721 (2026). https://doi.org/10.1038/s41598-026-47552-0
Palabras clave: persistencia frente a antibióticos, especies reactivas de oxígeno, profagos, Salmonella Typhimurium, ciprofloxacino